Servicio Nacional de Sanidad y Calidad Agroalimentaria
SANIDAD ANIMAL
Resolución 1540/2000
Apruébanse los Procedimientos de Aprobación y Control de Series de
Tuberculina P.P.D. Bovina.
Bs.
As., 25/9/2000
VISTO
el expediente N° 6270/99 del registro del SERVICIO NACIONAL DE SANIDAD Y
CALIDAD AGROALIMENTARIA, la Resolución N° 1 de fecha 3 de enero de 1983 del
registro del ex-SERVICIO NACIONAL DE SANIDAD ANIMAL, la Resolución N° 115 de fecha 1° de marzo de 1999 de la SECRETARIA DE AGRICULTURA, GANADERIA, PESCA Y ALIMENTACION, la Resolución N° 274 de fecha 9 de junio de 1983 de la
ex-SECRETARIA DE AGRICULTURA Y GANADERIA y la Resolución N° 205 de fecha 17 de abril de 1996 del ex-SERVICIO NACIONAL DE SANIDAD ANIMAL, y
CONSIDERANDO:
Que
por la Resolución N° 1/83 del registro del ex-SENASA se establecen los
procedimientos de aprobación de Tuberculina P.P.D. Bovina.
Que
por la Resolución N° 115/99 de la SECRETARIA DE AGRICULTURA, GANADERIA, PESCA Y ALIMENTACION, se impone el Programa Nacional de Control y Erradicación de la Brucelosis y Tuberculosis Bovina.
Que
la implementación del mencionado Programa Nacional, incrementará sensiblemente
la disponibilidad del número de series de Tuberculina P.P.D. Bovina
intradérmica.
Que
el éxito del programa depende, entre otras cosas, de la sensibilidad y
especificidad de las pruebas diagnósticas y de la calidad de los reactivos
utilizados.
Que
el principal costo del Programa lo constituye la segregación de los animales
reactores, siendo por lo tanto imprescindible asegurar la calidad adecuada de la Tuberculina que se libere al mercado.
Que
por todo lo expuesto, la certificación de aprobación de las series de
Tuberculina constituye un asunto que involucra intereses nacionales de importancia
y que por lo tanto, deben asegurarse mecanismos transparentes, auditables y
verificables.
Que
la Dirección Nacional de Sanidad Animal y la Comisión Nacional de Brucelosis y Tuberculosis fueron puestas en conocimiento, teniéndose en
cuenta las observaciones realizadas.
Que
la Dirección de Asuntos Jurídicos ha tomado la intervención que le compete
(fojas 119), no encontrando reparos de orden legal que formular.
Que
el suscripto es competente de acuerdo a lo establecido en los artículos 8°,
inciso h) y 9°, inciso a) del Decreto N° 1585 del 19 de diciembre de 1996 y el
artículo 4° de la Resolución N° 115 de fecha 1° de marzo de 1999 de la SECRETARIA DE AGRICULTURA, GANADERIA, PESCA Y ALIMENTACION.
Por
ello,
EL
VICEPRESIDENTE EJECUTIVO DEL SERVICIO NACIONAL DE SANIDAD Y CALIDAD
AGROALIMENTARIA
RESUELVE:
Artículo 1° —
Apruébanse las series de Tuberculina P.P.D. Bovina, una vez cumplimentados
todos los seguimientos mencionados en la presente resolución, a través de la Coordinación General de Laboratorio Animal de la Dirección de Laboratorios y Control Técnico
(DILACOT) del SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA.
Art. 2° —
Las pruebas de potencia dispuestas en el Anexo que forma parte integrante de la
presente resolución, deberán realizarse en la Dirección de Laboratorios y Control Técnico del SERVICIO NACIONAL DE SANIDAD Y CALIDAD
AGROALIMENTARIA, o en los lugares que la Dirección de Laboratorios y Control Técnico determine.
Art. 3° —
Se realizarán por sorteo, ensayos de potencia interlaboratorios y de eficacia
sobre animales de la especie bovina, según protocolos que forman parte
integrante de la presente y que a tales efectos estableció la Coordinación General de Laboratorio Animal, de manera independiente de los procedimientos de
aprobación de series de Tuberculina P.P.D. Bovina establecidos en el Anexo de
la presente resolución.
Art. 4° —
Comuníquese, publíquese, dése a la Dirección Nacional del Registro Oficial y archívese. — Víctor E. Machinea.
ANEXO
PROCEDIMIENTOS
DE APROBACION Y CONTROL DE SERIES DE TUBERCULINA P.P.D. BOVINA
Reconocimientos:
El
presente Anexo fue extractado del "Manual de Procedimientos Técnicos de
Producción y Control de Tuberculina Bovina —Derivado Proteico Purificado—
P.P.D." del SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA, normas
de Organismos Internacionales de referencia y el INSTITUTO PANAMERICANO DE
PROTECCION DE ALIMENTOS Y ZOONOSIS (INPPAZ).
Determinación
de la Potencia Biológica:
Se
realiza en cobayos previamente sensibilizados.
Con
la suspensión del Anexo VI (página 51 Manual de Procedimientos Técnicos -
Producción y Control de Tuberculina Bovina - Derivado Proteico Purificado -
P.P.D. - DILACOT - SENASA 1998), inocular a cada cobayo con CERO CON CINCO
MILILITROS (0,5 ML) por vía intramuscular utilizando jeringas con camisa y
émbolo de vidrio de UN MILILITRO (1 ml), adaptador de rosca tipo Luerlock y
aguja VEINTE (20) SWG x DIECIOCHO MILIMETROS (18 mm).
Después
de realizado este procedimiento, autoclavar todo el material utilizado a CIENTO
VEINTE GRADO CENTIGRADOS (120°C) durante TREINTA (30) minutos.
Dejar
transcurrir TREINTA (30) días hasta su utilización.
Los
cobayos así sensibilizados se pueden utilizar hasta SEIS (6) meses posteriores
a la inoculación.
Estándar
Internacional:
Basado
en un ensayo colaborativo internacional en cobayos y bovinos en el año 1986, la ORGANIZACION MUNDIAL DE LA SALUD (OMS) entregó oficialmente el estándar internacional de
Tuberculina P.P.D. Bovina: TREINTA Y DOS MIL QUINIENTAS UNIDADES INTERNACIONALES
POR MILIGRAMO POR MILILITRO (32.500 UI/mg/ml), corresponden a UN MILIGRAMO (1
mg) de Tuberculina PPD Bovina.
La
potencia estimada de Tuberculina Bovina deberá ser no inferior al SESENTA Y
SEIS POR CIENTO (66%) ni mayor del CIENTO CINCUENTA POR CIENTO (150%).
A
los fines de no utilizar en forma continua este reactivo biológico, es
necesario que los países establezcan su propio patrón de referencia nacional
calibrado contra el estándar internacional en cobayos y bovinos.
Para
los sucesivos controles en los lotes de tuberculinas producidos por la
actividad privada u oficial, los mismos serán realizados con la serie
establecida de referencia nacional.
Procedimiento:
En
cobayos sensibilizados en la cepa AN de Mycobacterium bovis, realizar la
depilación mediante afeitadora y crema depilatoria de ambos flancos de cada
animal, CUATRO (4) horas antes de la prueba de potencia.
Diluciones
de la Tuberculina:
|
DOS
CON CINCO MILILITROS (2,5 ml) de P.P.D
|
QUINIENTOS
MILILITROS (500 ml) diluyente buffer
|
UNO
EN DOSCIENTOS (1/200)
|
|
VEINTE
MILILITROS (20 ml) (UNO EN DOSCIENTOS (1/200))
|
CIEN
MILILITROS (100 ml) diluyente buffer
|
UNO
EN UN MIL (1/1000)
|
|
VEINTE
MILILITROS (20 ml) (UNO EN MIL (1/1000))
|
CIEN
MILILITROS (100 ml) diluyente buffer
|
UNO
EN CINCO MIL (1/5000)
|
Realizar
este esquema con la tuberculina de referencia y con la serie en control.
Mezclar
bien los matraces aforados, pasar a tubo de ensayo con tapón de goma reversible
para poder llenar las jeringas. Enjuagar cada jeringa con la dilución DOS (2) o
TRES (3) veces antes de llenarlas, finalmente enrasarlas y colocarlas numeradas
en una bandeja. Se inyecta CERO CON DOS MILILITROS (0,2 ml) por dilución. TRES
(3) diluciones a cada lado del cobayo. Se numeran de UNO (1) a TRES (3) para la
preparación de referencia y de CUATRO (4) a (SEIS) (6) para la tuberculina de
prueba.
Ensayo
de las Tuberculinas de referencia y en Prueba:
Inoculaciones.
Prueba de actividad relativa. Potencia:
SEIS
(6) sitios a usar en cada cobayo (TRES (3) en cada flanco) son denominados, en
sentido oral a caudal, con las letras "a", "b",
"c" para el costado izquierdo y "e", "f",
"g" para el derecho. La dilución de la tuberculina a ser aplicada en
cada sitio se determina mediante el empleo de números aleatorios. Este
procedimiento se sigue para cada animal y se preparará el protocolo de trabajo
(Tabla I) dejando un espacio al lado del número de la dilución para anotar la
respuesta. En un ensayo de SEIS (6) puntos usando NUEVE (9) cobayos, las
diluciones son asignadas en forma conveniente en los sitios de inyección,
empleando el sistema de cuadrado latino. Transcurridas VEINTICUATRO (24) horas
se realiza la lectura de la pápula, induración y eritema, mediante una
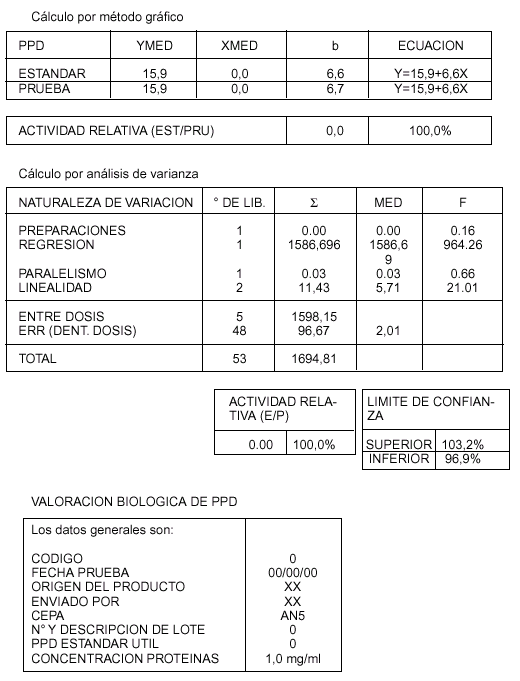
plantilla plástica y/o regla plástica milimetrada. Los datos consignados en la Tabla I se vuelcan a un programa informático de Cálculo numérico de la actividad relativa en
el sistema operativo WINDOWS 95’, producido por el INSTITUTO PANAMERICANO DE
PROTECCION DE ALIMENTOS Y ZOONOSIS (INPPAZ), en colaboración con la DILACOT-SENASA.

Esterilidad:
El
producto debe estar libre de toda contaminación, para ello es controlado en
medios de cultivos para aero-anaerobios y para el desarrollo de hongos.
Esto se realizará según el "Test for sterility and
freedom contamination of biological material, Chapter 1.4, pág. 16 y 17, Manual
of Standards for Diagnostic Tests and Vacines - 1996 – OFFICE INTERNATIONAL DES
EPIZOOTIES.
Ausencia
de gérmenes:
Se
centrifuga una muestra de QUINCE MILILITROS (15 ml) de la Tuberculina P.P.D. en control, con el sedimento se preparan DOS (2) frotis: UNO (1) para
colaboración de ácido - alcohol resistencia de Ziehl-Neelsen y UNO (1) para
coloración de Gram.
No
se debe observar la presencia de gérmenes en ninguno de los preparados.
Control
de toxicidad:
Se
inoculan CERO CON CINCO MILILITROS (0,5 ml) de la tuberculina en control, por
vía subcutánea, a CUATRO (4) cobayos que no han sido tratados previamente con
material antigénico. Al cabo de CUATRO (4) días los animales no deben presentar
alteración alguna.
Potencial
de hidrógeno (pH):
Debe
estar comprendido en el rango de SIETE CON CERO MAS MENOS CERO CON TRES (7.0
+,- 0.3).
Control
químico:
La
concentración proteica será determinada por métodos químicos, tales como
Biuret, Kjeldhal, semi micro Kjeldhal, etc., que permitan establecer el
nitrógeno proteico.
Reacción
del biuret: Es positiva para las proteínas y sus productos de hidrólisis
parcial, siendo propia aunque "no específica" de la unión peptídica,
y es presentada por moléculas que contienen DOS (2) grupo — CO-NH (carbamilo)
unidos directamente por UN (1) átomo de carbono o de nitrógeno.
El
biuret es la ureída (amida de la urea) del ácido carbónico:
H
2 N — CO — NH — CO – NH 2
Las
proteínas con largas cadenas peptídicas dan coloración azul violeta, y a medida
que la cadena se acorta, la coloración tiende hacia el rojo.
Es
probable que el desarrollo de color se deba a la formación de complejos de
coordinación con el cobre del tipo de:

Los
péptidos y las proteínas originan una coloración azul debida a los grupos NH 2
libres y amarilla o roja por los grupos: NH — CO — NH, la resultante es una
coloración violeta.
Método
del Biuret (modificado): De acuerdo a la concentración estimada entre CERO CON
CINCO MILIGRAMOS POR MILILITRO (0,5 mg/ml) a CUATRO MILIGRAMOS POR MILILITRO (4
mg/ml), realizar la siguiente distribución:
|
Concentración
aproximada:
|
2
mg/ml
|
0,5
mg/ml
|
|
Volumen
de la muestra:
|
2
ml
|
5
ml
|
|
Volumen
de la tuberculina de referencia:
|
2
ml
|
5
ml
|
|
Volumen
de agua destilada
|
3
ml
|
-
|
|
Volumen
de reactivo del biuret
|
5
ml
|
5
ml
|
Blanco
de reactivos: CINCO MILILITROS (5 ml) de agua destilada más CINCO MILILITROS (5
ml) de reactivo de Biuret.
Mezclar
los componentes y dejar a temperatura ambiente durante DIEZ (10) minutos para
el desarrollo de color.
Leer
en un espectrofotómetro a SEISCIENTOS VEINTICINCO NANOMETROS (625 nm)
La
concentración proteica de la muestra sera:
Absorbancia
de la muestra x concentración de la tuberculina de referencia en =
Absorbancia
de la tuberculina de referencia mg/ml y el factor de dilución.
Método
semimicro de Kjeldahl: Por la digestión en Acido Sulfúrico, el Nitrógeno en la Tuberculina es convertido en Sulfato de Amonio. En la alcanilización y destilación al vapor,
el amoníaco es llevado a una solución de Acido Bórico. El Nitrógeno es
determinado por titulación con solución estándar de SO 4 H 2
. La multiplicación del valor Nitrógeno por un factor SIETE (7) expresa la
cantidad de proteína en la muestra.
Todas
las determinaciones son de P.P.D. de Tuberculina precipitable.
Las
muestras se realizan por cuadriplicado y se incluyen DOS (2) controles.
No
se deberá conservar o usar amoníaco en ningún lugar cercano al área donde se
efectúa esta determinación.
Método.
Colocar
cada muestra y cada control en un tubo cónico de centrífuga de DIEZ MILILITROS
(10 ml), numerándose cada tubo para su identificación:

(*)
Se puede utilizar en su lugar agua destilada
Colocar
en el tubo de centrífuga, según el orden indicado. Después del mezclado del
contenido dejar los tubos en reposo (cubiertos) a temperatura ambiente durante
TREINTA (30) minutos.
Centrifugar
a DOS MIL REVOLUCIONES POR MINUTO (2.000 rpm) durante QUINCE (15) minutos.
Decantar
cuidadosamente y separar el sobrenadante.
Disolver
la proteína precipitada de cada tubo en CERO CON CINCO MILILITROS (0,5 ml) de
solución CINCO NORMAL (5N) de OHNa, lavando los costados del tubo por rotación
en posición caso horizontal.
Una
pequeña cantidad de proteína se adhiere en el lateral del tubo formando un
anillo sobre el mismo en la superficie del líquido.
Cuando
está completamente disuelto, lavar la solución de tuberculina de cada tubo en
un matraz de Kjeldahl correspondiente a la numeración, usando SEIS (6);
transferir cada muestra con UN MILILITRO (1 ml) de agua destilada.
A
la solución de cada Kjeldahl, añadir:
- H2 SO 4 concentrado: UN
MILILITRO (1 ml) aproximadamente.
- TRES (3) esferitas de vidrio.
Digerir
sobre un mechero de gas. Después que ha hervido el agua, continuar calentando
hasta la aparición de un depósito marrón.
Clarificar
por agregado a cada recipiente (incluidos los controles que no muestran
depósito marrón) de CERO CON CINCO MILILITROS (0,5 ml) de H 2 O 2
(CIEN (100) volúmenes).
Continuar
calentando. Si aparece un depósito, añadir otros CERO CON CINCO MILILITROS (0,5
ml) de H 2 O 2 a cada recipiente de manera que cada uno
reciba la misma cantidad.
Continuar
calentando hasta que el SO 4 H 2 comienza a destilar en
el cuello del matraz, mantener el calentamiento durante DIEZ (10) minutos. Se
produce una conversión de NOVENTA Y OCHO POR CIENTO (98%) de Nitrógeno a
Sulfato de Amonio. El color del líquido en los matraces de Kjeldahl deberá ser
verde claro antes de retirar la llama de gas.
La
etapa siguiente es la destilación por calor en el aparato de Markman. El agua
del generador de vapor estará ligeramente acidificada con Acido Fosfórico.
Cargar DIEZ MILILITROS (10 ml) de Acido Bórico al DOS POR CIENTO (2%)
conteniendo indicador de Conway en la cámara de destilación y destilar al vapor
durante CINCO (5) minutos.
Retirar
esta carga y reemplazar con una nueva carga y destilar como antes. Si hubiera
cualquier cambio en el color de la misma, repetir este procedimiento hasta que
el color rojo de la solución de Acido Bórico permanezca invariable. Destilar
por vapor durante CINCO (5) minutos con una carga de agua destilada. El aparato
de Markman está ahora listo para ser usado.
Colocar
un frasco cónico de CINCUENTA MILILITROS (50 ml) conteniendo CINCO MILILITROS
(5 ml) de una solución al DOS POR CIENTO (2%) de Acido Bórico e indicador de
Conway debajo de la salida del condensador.
Usar
CINCO (5) veces, UN MILILITRO (1 ml) de agua destilada, lavar los contenidos de
un matraz de Kjeldahl en la cámara de destilación de Markman.
Con
cuidado agregar CINCO MILILITROS (5 ml) de una solución al CINCUENTA POR CIENTO
(50%) de OHNa para formar una capa profunda. Acomodar el tapón de la cámara.
Levantar
el frasco cónico colector de modo que la salida del condensador gotee debajo de
la superficie de la solución de Acido Bórico.
Destilar
al vapor la muestra durante TRES (3) minutos. Después de la destilación,
inmediatamente bajar el recipiente colector de modo que la superficie del
líquido esté apartada de la salida del condensador en el frasco colector usando
unos DOS MILILITROS (2 ml) de agua destilada.
El
proceso de destilación deberá haber triplicado aproximadamente el volumen del
líquido en el frasco colector.
El
destilado debe estar frío, para ello, hacer pasar gran cantidad de agua fría a
través del condensador.
Con
una muestra de P.P.D. de tuberculina, el contenido del frasco colector será
ahora verde, pero con un testigo el color será generalmente ligeramente rojo.
Titular
de inmediato con solución ONCE CON DOS NORMAL (11.2 N) SO 4 H 2
en una microbureta de CINCO MILILITROS (5 ml) hasta que el color original rojo
justo reaparezca.
Observe
el volumen de solución de SO 4 H 2 usado.
Cargar
la cámara de destilación del aparato de Markman con unos DIEZ MILILITROS (10
ml) de agua destilada y destilar al vapor durante DOS O TRES (2 o 3) minutos
antes de introducir la muestra siguiente.
Tratar
todas las muestras y controles tal lo descripto anteriormente.
Observe
que después de cada destilación, la condensación del vapor separa al líquido de
la cámara de destilación.
Cuando
esto ha sucedido, la llave de remoción del vapor debe abrirse antes de
introducir otra muestra, de otro modo la muestra se perderá.
Colocar
el nitrógeno estándar por el pipeteado de UN MILILITRO (1 ml) de solución de
Sulfato de Amonio directamente en la cámara de Markman, lavando con unos CINCO
MILILITROS (5 ml) de agua destilada, añadiendo CINCO MILILITROS (5 ml) de
solución al CINCUENTA POR CIENTO (50%) de OHNa y destilar al vapor tal como
para las muestras y controles. Esto debería titularse con OCHO MILILITROS (8
ml) de una solución ONCE CON DOS NORMAL (11.2 N) de SO 4 H 2
.
El
ejemplo siguiente muestra el orden en el cual las destilaciones y las
titulaciones se efectúan y en la forma en que se obtienen los resultados en
términos de miligramos de P.P.D. de Tuberculina/ mililitro. Se trabajó sobre
DOS MILILITROS (2 ml) de muestra.

NOTA:
Estas titulaciones del control son valores altos. Normalmente no deberían
exceder de CERO CON UN MILILITRO (0,1 ml). En los casos como el descripto, el
color del Acido Bórico será definitivamente verde.
Muy
a menudo los controles son tan bajos como CERO CON CERO UN MILILITROS (0,01
ml); CERO CON CERO CINCO MILILITROS (0,05 ml) o aún CERO (0) y entonces, por
supuesto el color del Acido Bórico permanece rojo.
Aunque
el Nitrógeno estándar está indicado en el frasco N° 2, es aconsejable destilar
este al finalizar, evitando con ello pasar posible Nitrógeno a muestras
subsiguientes.
Con
este método los resultados son exactos en un MAS MENOS CINCO POR CIENTO +,-
5%).
Cálculos:
|
Título
promedio:
|
4,74
ml
|
|
Promedio
control:
|
0,095
ml
|
|
Titulación
corregida:
|
4,645
ml
|
Dividir
por la cantidad de mililitros de SO 4 H 2 estándar
equivalente a 1 mg de Nitrógeno = 0,580.
Multiplicar
por el factor de conversión 7 = 4,060
Dividir
por la cantidad de mililitros empleados en cada muestra = 2,03
Por
lo tanto, contenido de P.P.D. = 2,03 mg/ml
Reacción:
H
3 Bo 3 + 3 NH 4 OH ———— (NH 4 ) 3
Bo 3 + H 2 O + exceso de Bo 3 H 3
2
(NH 4 ) 3 Bo 3 + 3 H 2 SO 4 ——— 3
(NH 4 ) 2 SO 4 + 2 H 3 Bo 3
1
ml N/11.2 H 2 SO 4 = 0.125 mg Nitrógeno.
Por
lo tanto, 1 mg. Nitrógeno = 8.0 ml N/11.2 H 2 SO 4
Multiplicar
el valor del Nitrógeno por factor P.P.D. = 7
Expresar
el resultado en mg P.P.D./ml de solución.
Contenido
de fenol y de otros agentes conservadores:
Si
se ha utilizado fenol, la concentración deberá estar en QUINIENTOS MILIGRAMOS
POR CIENTO (500 mg%).
El
método usado para su determinación es mediante el reactivo de Folin-Ciocalteau.
El
complejo de ácido fosfotúngstico, en medio alcalino, es reducido a un coloide
de color azul.
Técnica:
En
matraz aforado de CIEN MILILITROS (100 ml), colocar DOS MILILITROS (2 ml) de la Tuberculina P.P.D., en control y de la utilizada como referencia, con el fin de que la
concentración inicial de CERO CON CINCO POR CIENTO (0,5%) se reduzca a CERO CON
CERO UN POR CIENTO (0,01%), para que la coloración posterior que se produzca,
pueda ser determinada en la escala habitual de los espectrofotómetros.
Colocar
en DOS (2) matraces aforados de CINCUENTA MILILITROS (50 ml), lo siguiente:

Llevar
a volumen con agua destilada mezclar e incubar a TREINTA Y SIETE GRADOS
CENTIGRADOS (37°C) durante UNA (1) hora.
Leer
en espectrofotómetro a SEISCIENTOS OCHO NANOMETROS (608 nm.).
Absorbancia
de la muestra x 0,5% =
Absorbancia
de la
Tuberculina
de referencia
Coloración
de las Tuberculinas:
A
los efectos de diferenciar visualmente la tuberculina aviar de la bovina, se
colorea a la primera con Rojo Ponçeau 2R.
Conservación:
Las
tuberculinas P.P.D. deberán conservarse constantemente a una temperatura de
CINCO GRADOS CENTIGRADOS MAS MENOS TRES GRADOS CENTIGRADOS (5°C+,-3°C).
Plazo
de validez:
Las
tuberculinas P.P.D. serán consideradas aptas por un plazo de DOS (2) años.
Cumplidos
estos requisitos se otorgará a los laboratorios productores el respectivo
certificado de uso y comercialización.






