Resolución Conjunta
470/92 y 268/92
Reglamentación del
Decreto Nº 150/92
Las especialidades
medicinales autorizadas a la fecha de vigencia del Decreto Nº 150/92 serán
incorporadas al registro especial al que se refiere el Artículo 2º del
mencionado Decreto mediante la presentación por parte del titular del
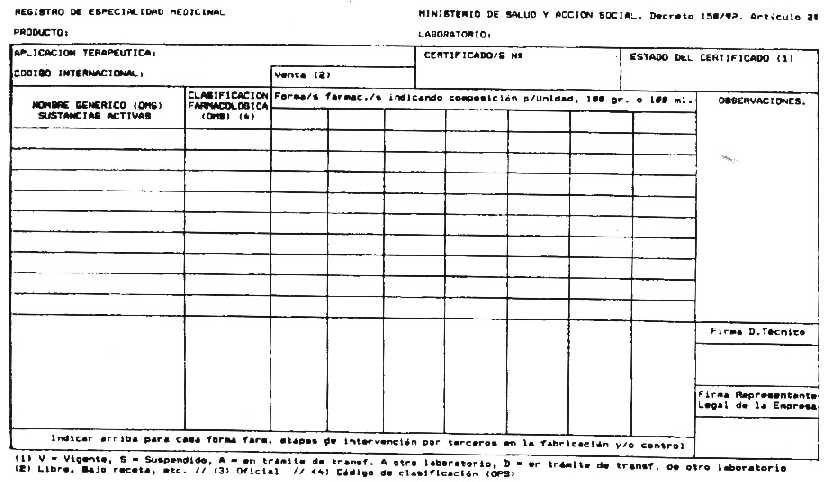
certificado vigente del formulario que como Anexo I forma parte de la presente
Resolución. La incorporación será automática. Cualquiera fuera el número de
formas farmacéuticas que estén actualmente autorizadas para una especialidad
medicinal les corresponderá un único certificado.
Bs. As., 10/4/92
VISTO el Decreto Nº 150
del 20 de enero de 1992, reglamentario de la Ley 16.463, y
CONSIDERANDO:
Que es necesario
reglamentar el citado Decreto según lo establecido en el Artículo 22 del mismo.
Que se deben establecer
los procedimientos administrativas para el registro de los medicamentos en la
SECRETARIA DE SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL que el mencionado
Decreto actualiza tomando en cuenta la experiencia acumulada desde la vigencia
de la Ley Nº 16.463 en 1964.
Que se hace necesario
establecer los requisitos técnicos para la calidad, distribución, depósito y
transporte de los medicamentos tomando como base las recomendaciones de la Organización
Mundial de la Salud.
Que igualmente deben
establecerse los requisitos necesarios para asegurar la eficacia, inocuidad y
calidad de los productos farmacéuticos importados mediante la realización de
los controles necesarios antes de su liberación al mercado.
Que es necesario informar
tanto a los profesionales autorizados a prescribir medicamentos como a la
población, sobre los nombres genéricos y sus correspondientes marcas
comerciales.
Que deben darse las
debidas garantías al fraccionamiento de los medicamentos, tanto en el proceso
de elaboración como durante la dispensación en las farmacias, siendo en este
último caso el farmacéutico responsable de la integridad y calidad del producto
que entrega.
Que las garantías
previamente descriptas aseguran que los medicamentos incluidos en el Registro
cumplen con las condiciones de eficacia, inocuidad y calidad que justifican su
utilización en medicina humana y su correspondiente comercialización.
Que teniendo en cuenta la
experiencia en la utilización de los medicamentos que prescribe, el profesional
autorizado a dar cumplimiento a lo establecido en el Artículo 10 del Decreto Nº
150/92 respecto al uso del o de los nombres genéricos que identifican el
medicamento prescripto podrá, cuando así lo estime necesario, seleccionar UNA
(1) o más marcas comerciales entre los productos equivalentes existentes en el
Registro de la SECRETARIA DE SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL.
Que, en observancia de lo
dispuesto en la Ley 17.565/67 respecto de dar cumplimiento estricto de lo
prescripto por el profesional autorizado, el farmacéutico dispensará el
medicamento prescripto entregando una especialidad medicinal entre las que
figuren en el Listado a que hace referencia el inciso b) del Artículo 6º del Decreto
Nº 150/92 o una de las marcas comerciales que haya indicado el profesional
autorizado.
Que para asegurar la
calidad de los medicamentos importados, es necesario quienes realicen esta
actividad sean responsables de la calidad de los productos que ellos
comercialicen.
Que deben establecerse
plazos para la intervención de los organismos estatales, con el fin de agilizar
la comercialización de los medicamentos.
Que es necesario arancelar
las tramitaciones relacionadas con la solicitud de inscripción en el Registro,
para fortalecer el Instituto Nacional del Medicamento.
Que diversos sectores
científicos, técnicos, gremiales, industriales y del área comercial de
medicamentos tuvieron la oportunidad de dar a conocer sus posiciones sobre esta
reglamentación a las autoridades de ambos Ministerios en reuniones públicas
destinadas a su discusión.
Que también se tomaron en
cuenta las opiniones de diversas entidades dadas a conocer en forma muy amplia
y con diversidad de criterios a través de la prensa, tanto escrita como
televisiva y radial.
Que los Servicios
Jurídicos Permanentes de los MINISTERIOS DE ECONOMIA Y OBRAS Y SERVICIOS
PUBLICOS Y DE SALUD Y ACCION SOCIAL han tomado la intervención que les compete.
Que la presente Resolución
se dicta en función de lo establecido en el Artículo 22 del Decreto Nº 150/92.
Por ello,
LOS MINISTROS DE ECONOMIA
Y OBRAS Y SERVICIOS PUBLICOS Y DE SALUD Y ACCION SOCIAL
RESUELVEN:
Artículo 1º — Las
especialidades medicinales autorizadas a la fecha de vigencia del Decreto Nº 150/92
serán incorporadas al registro especial al que se refiere el Artículo 2º del
mencionado Decreto mediante la presentación por parte del titular del
certificado vigente del formulario que como Anexo I forma parte de la presente
Resolución. La incorporación será automática. Cualquiera fuera el número de
formas farmacéuticas que estén actualmente autorizadas para una especialidad
medicinal les corresponderá un único certificado.
El plazo de incorporación
será de QUINCE (15) días a partir de la vigencia de la presente Resolución. La
SECRETARIA DE SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL determinará
posteriormente otros plazos para la incorporación de las especialidades
medicinales para las que no se haya efectuado presentación dentro del plazo
indicado.
Las excepciones a la
prohibición a las que se refiere el Artículo 2º del Decreto mencionado son las
especialidades medicinales que:
a) estén destinadas a los
estudios e investigaciones clínicas que hayan sido autorizadas de acuerdo con
las normas vigentes;
b) determine el MINISTERIO
DE SALUD Y ACCION SOCIAL para afrontar situaciones de emergencia sanitaria y
aceptar donaciones internacionales;
c) importen los
particulares para su uso personal sobre la base de una receta médica
específica;
d) traigan, en cantidades
razonables, los viajeros del exterior para su uso personal.
Art. 2º — Quedan
comprendidas en los alcances del Artículo 3º del Decreto Nº 150/92 las
especialidades medicinales constituidas por un único principio activo o
asociaciones de dos o más principios activos internacionalmente reconocidos
para las que exista previamente registrado en el país un producto similar o que
no constituya una novedad en los términos del Artículo 5º del citado decreto.
Para cumplimentar la
información requerida por el referido Artículo 3º, las solicitudes de
inscripción en el registro deberán estar acompañadas por la documentación
técnica establecida en la Resolución Nº 3784 del 4 de setiembre de 1991 del
MINISTERIO DE SALUD Y ACCION SOCIAL o la que en su reemplazo disponga la
SECRETARIA DE SALUD de dicho ministerio.
El plazo a que hace
referencia el Artículo 3º será interrumpido en todos los casos en que, a
requerimiento de un funcionario de jerarquía no inferior a Director, el
solicitante deba incorporar información adicional y hasta tanto la misma se
considere debidamente cumplimentada. En todos los casos la suspensión de los
plazos deberá estar fundamentada. Una vez vencido el mismo y no existiendo
objeciones, la SECRETARIA DE SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL
deberá extender el certificado en un plazo no mayor a VEINTE (20) días.
A las solicitudes de
registro en trámite a la fecha de vigencia del Decreto Nº 150/92 que
correspondan al régimen del Artículo 3º se le aplicará el procedimiento establecido
en el párrafo anterior.
Art. 3º — La certificación
de origen a que se refiere el Artículo 4º del Decreto Nº 150/92 deberá estar
conformada de acuerdo con las recomendaciones de la Organización Mundial de la
Salud para el comercio internacional de productos farmacéuticos y documentación
probatoria de su consumo en el país de origen, con indicación de los datos de
formulación, control de calidad y bases farmacológicas, toxicológicas y
clínicas que fundamentaron su aprobación en ese país. Los rótulos y prospectos
deberán reproducir en idioma nacional las indicaciones, contraindicaciones,
efectos adversos, posología, advertencias y recomendaciones de uso autorizadas
en el país de origen.
Cuando se trate de
solicitudes de registro presentadas por solicitantes que no sean los titulares
o representantes del titular del registro en el país de origen, la
certificación oficial vigente de medicamentos a que se refiere el Artículo 4º
del Decreto Nº 150/92 podrá reemplazarse por una evidencia de comercialización
en cualquiera de los países mencionados en el Anexo I del Decreto a la que
deberá agregarse también la documentación a que se refieren los incisos a) y b)
del Artículo 3º del Decreto Nº 150/92.
Para el registro de
productos a importarse de países que no figuren en el Anexo I del Decreto Nº
150/92 pero autorizados en los mismos, la SECRETARIA DE SALUD del MINISTERIO DE
SALUD Y ACCION SOCIAL requerirá al importador la presentación de un certificado
de registro y comercialización en el país de origen de acuerdo con las
recomendaciones de la Organización Mundial de la Salud y documentación
aprobatoria de su consumo en el mercado interno del país pertinente.
A los efectos del registro
automático que establece el Artículo 4º del Decreto Nº 150/92 la SECRETARIA DE
SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL dispondrá de VEINTE (20) días
para la verificación de la documentación presentada. Vencido el plazo y no
existiendo objeciones, el certificado de inscripción será expedido en un plazo
máximo de DIEZ (10) días. Igual procedimiento se aplicará a las solicitudes de
registro en trámite a la fecha de vigencia de esta resolución que a
requerimiento del solicitante puedan considerarse amparadas en el Artículo 4º.
La solicitud de registro
de un producto será denegada cuando se compruebe que una solicitud similar fue
denegada, o el registro del producto se haya suspendido o cancelado en alguno
de los países del Anexo I.
Las condiciones del
registro podrán ser modificadas o ampliadas, así como también suspendidas o
canceladas, cuando tales cambios o medidas se hayan producido en el registro de
alguno de los países del Anexo I. El titular del registro queda obligado a
notificar a la SECRETARIA DE SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL
cualquier novedad de este tipo.
Para la realización de los
controles que sean necesarios, el Instituto Nacional de Medicamentos
dependiente de la SECRETARIA DE SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL
podrá requerir los métodos de control y demás datos técnicos para tal fin.
Art. 4º — Las solicitudes
de registro de especialidades medicinales a las que se refiere el Artículo 5º
del Decreto Nº 150/92, deberán incluir los datos identificatorios del producto
indicados en el Artículo 3º del decreto mencionado y suficiente información
química, farmacéutica, de control de calidad, estabilidad y elaboración, así
como documentación farmacológica, toxicológica y clínica que demuestre su
eficacia e inocuidad requeridas por las Normas Técnicas establecidas por la
SECRETARIA DE SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL.
Quedan comprendidas en los
alcances de este artículo las nuevas indicaciones de especialidades medicinales
ya inscriptas.
Art. 5º — La SECRETARIA DE
SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL y la SECRETARIA DE INDUSTRIA Y
COMERCIO del MINISTERIO D ECONOMIA Y OBRAS Y SERVICIOS PUBLICOS publicarán el
Listado Terapéutico por clasificación farmacológica e índice alfabético de
nombres genéricos con sus correspondientes marcas comerciales en las distintas
formas farmacéuticas agrupadas según dosis y concentración. Este Listado se
actualizará trimestralmente y contendrá los precios sugeridos de venta al
público. Esta información deberá estar disponible en todos los lugares donde se
dispensen medicamentos y al alcance de todos los profesionales autorizados a
prescribirlos.
Art. 6º — La producción y
fraccionamiento de medicamentos y especialidades medicinales a que se refiere
el Capítulo III del Decreto Nº 150/92 deberá realizarse bajo la dirección
técnica de un profesional farmacéutico.
Las actividades
relacionadas con drogas o principios activos de medicamentos podrán realizarse
bajo la dirección técnica de un profesional farmacéutico, químico u otros
profesionales con títulos habilitantes.
Las condiciones higiénico
sanitarias de los procesos de producción, fraccionamiento, control de calidad,
distribución, depósito y transporte se ajustarán como mínimo a las
recomendaciones de la Organización Mundial de la Salud sobre buenas prácticas
de fabricación o a las que establezca la SECRETARIA DE SALUD del MINISTERIO DE
SALUD Y ACCION SOCIAL.
Art. 7º — En el caso del
Artículo 10, inciso d) del Decreto Nº 150/92, el profesional autorizado a
prescribir medicamentos, que considere que existan motivos fundados para que se
utilicen productos de marca de laboratorios determinados, podrá agregar al
nombre genérico, el nombre de uno o más laboratorios o marcas comerciales
requiriéndose para esto una segunda firma del profesional.
El MINISTERIO DE SALUD Y
ACCION SOCIAL hará conocer amplia y fehacientemente a la opinión pública y a
todas las instituciones públicas y privadas involucradas, el alcance de las
reglamentaciones que disponen el uso del nombre genérico en la prescripción
médica. Para tal fin promoverá también acuerdos con las universidades para su
uso en la enseñanza médica, odontológica y farmacéutica.
Art. 8º — El farmacéutico
deberá dispensar una especialidad medicinal salvo que el profesional indique
que se trata de una receta magistral.
El farmacéutico que
dispense un medicamento a partir de la correspondiente receta deberá agregar a
su rúbrica y sello el nombre comercial del medicamento entregado al usuario,
excepto en aquellos casos que el profesional haya indicado una marca comercial
o laboratorio. En los casos de recetas de la Seguridad Social se adosará el
correspondiente troquel.
Art. 9º — El
fraccionamiento en farmacias, tal como lo prevé el Artículo 13 del Decreto Nº
150/92, sólo se permitirá a partir de productos registrados en el MINISTERIO DE
SALUD Y ACCION SOCIAL para las formas farmacéuticas sólidas envasadas en
blister o tiras conformadas de material adecuado para su conservación,
granulados o polvos en envases monodosis y ampollas o frascos ampollas.
En el rótulo del envase
entregado al usuario deberá figurar el nombre del farmacéutico responsable del
fraccionamiento y otros datos que permitan la identificación del medicamento y
su uso correcto, según lo determine la SECRETARIA DE SALUD del MINISTERIO DE
SALUD Y ACCION SOCIAL.
El farmacéutico
responsable del fraccionamiento deberá tener a disposición del paciente
prospectos en cantidad suficiente para el caso de serle requeridos.
Art. 10. — Las actividades
de comercio exterior previstas en el Capítulo V del Decreto Nº 150/92 quedan
sujetas a las estipulaciones del presente artículo.
A los efectos de las
definiciones del 1er. párrafo del Artículo 14 del mencionado decreto, se
adoptarán las siguientes expresiones aclaratorias:
a) se entiende por
laboratorio a los que producen especialidades medicinales y se hallan
debidamente autorizados;
b) se entiende por entes
prestadores de servicios de salud y públicos y privados a los hospitales
nacionales, provinciales y municipales y a los hospitales, sanatorios y
clínicas privadas inscriptas en las respectivas jurisdicciones sanitarias.
Los establecimientos
importadores contarán con un director técnico profesional farmacéutico.
Las actividades de
importación de productos farmacéuticos están sujetas a los mismos requisitos
higiénicos sanitarios que la autoridad sanitaria establezca para los productos
elaborados y/o fraccionados en el país, siendo el importador responsable de la
calidad del producto farmacéutico.
En todos los casos el
control de calidad deberá realizarse en forma completa en el país, en
laboratorios de control de calidad del importador o de terceros autorizados por
la SECRETARIA DE SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL.
Deberán conservarse en el
establecimiento importador muestras representativas en cantidad suficiente para
su análisis por la autoridad sanitaria.
La importación de
medicamentos se efectuará bajo el régimen de despacho a plaza sin autorización
de uso. La autoridad sanitaria inspeccionará en función del riesgo sanitario
las partidas importadas dentro de los CINCO (5) días de su despacho a plaza,
obligándose el importador a comunicar a la SECRETARIA DE SALUD del MINISTERIO
DE SALUD Y ACCION SOCIAL en forma inmediata el ingreso del producto a sus
depósitos. La autoridad sanitaria deberá expedirse en el término de TREINTA
(30) días corridos; vencido dicho plazo el importador podrá comercializar el
producto.
Cuando el importador se
provea de un vendedor extranjero que no sea el fabricante del producto, deberá
acreditar mediante documentación fehaciente el origen de fabricación. La autoridad
sanitaria verificará en el plazo de CINCO (5) días que la partida importada
corresponde a un registro vigente.
En los rótulos de los
productos importados deberá indicarse el nombre del laboratorio productor y del
importador, su dirección y nombre del Director Técnico. Se aceptará la
sobreimpresión de los datos del importador.
Art. 11. — El rótulo de la
unidad de reempaque a la que se refiere el Artículo 15 del Decreto Nº 150/92
deberá contener los datos indicados en el inciso c) del Artículo 3º del mismo
decreto.
Art. 12. — A efectos del
ejercicio de las actividades conjuntas que determina el Artículo 20 del Decreto
Nº 150/92 se establece que:
a) la SECRETARIA DE SALUD
del MINISTERIO DE SALUD Y ACCION SOCIAL remitirá mensualmente a la SECRETARIA
DE INDUSTRIA Y COMERCIO del MINISTERIO DE ECONOMIA Y OBRAS Y SERVICIOS PUBLICOS
un listado que contenga los registros autorizados y denegados de medicamentos;
b) la SECRETARIA DE
INDUSTRIA Y COMERCIO del MINISTERIO DE ECONOMIA Y OBRAS Y SERVICIOS PUBLICOS remitirá
quincenalmente a la SECRETARIA DE SALUD del MINISTERIO DE SALUD Y ACCION SOCIAL
un listado de los despachos a plaza de los medicamentos importados.
Art. 13. — La
incorporación al registro de las especialidades medicinales a las que se
refieren los Artículos 2º y 3º de la presente Resolución devengará un arancel
de MIL PESOS ($ 1000).
La incorporación al
registro de las especialidades medicinales a las que se refiere el Artículo 4º
de la presente Resolución devengará un arancel de TRES MIL PESOS ($ 3000).
Art. 14. — El
mantenimiento en el registro de las especialidades medicinales a que se refiere
la presente Resolución devengará un arancel anual de MIL PESOS ($ 1000) que se
hará efectivo por año vencido.
Art. 15. — Los recursos
provenientes de los aranceles establecidos en los Artículos 13 y 14 de la
presente Resolución ingresarán al Fondo Nacional de la Salud con destino al
Instituto Nacional de Medicamentos de la SECRETARIA DE SALUD del MINISTERIO DE
SALUD Y ACCION SOCIAL.
Art. 16. — Deróganse los
ítems 1.2, 1.5, 1.13, 1.18, y 1.19 del Anexo I de la Resolución Nº 3480 del 26
de agosto de 1991 del MINISTERIO DE SALUD Y ACCION SOCIAL.
Art. 17. — Comuníquese,
publíquese, dése a la Dirección Nacional del Registro Oficial y archívese. —
Domingo F. Cavallo. — Julio C. Aráoz.