Disposición 1108/1999
Establécense normas
técnicas para la admisión automática de productos de Higiene Personal,
Cosméticos y Perfumes.
Bs. As., 15/3/99
VISTO el artículo 8° de la
Resolución (M.S. y A.S.) N° 155/98 por el cual se faculta a esta Administración
Nacional a dictar disposiciones reglamentarias de la misma; y
CONSIDERANDO:
Que para cumplir con este
objetivo se debe proceder al dictado de normas técnicas para reglamentar la
admisión de Productos de Higiene Personal, Cosméticos y Perfumes, sobre la base
de los lineamientos establecidos en la Resolución precitada.
Que el Instituto Nacional
de Medicamentos y la Dirección de Asuntos Jurídicos han tomado la intervención
de su competencia.
Que se actúa en virtud de
las facultades conferidas por el artículo 3°, inciso c) y el artículo 8°,
inciso II) del Decreto N° 1490/92.
Por ello,
EL DIRECTOR NACIONAL DE LA
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
DISPONE:
Artículo 1° — Para la
admisión automática de Productos de Higiene Personal, Cosméticos y Perfumes,
definidos en el Artículo 2° de la Resolución (M.S. y A.S.) N° 155/98 se
requiere que previamente la/las empresa/s estén habilitadas por esta
Administración Nacional.
Las solicitudes deberán
cumplimentar con los requisitos establecidos en los Anexos I, II y III de la
presente Disposición, de acuerdo a la forma cosmética, fase etaria, uso y área
de aplicación.
En el caso de solicitud de
admisión de productos de una misma línea y fórmula básica, que difieran
únicamente en aroma y/o color, como fragancias, tinturas para el cabello,
maquillaje, esmaltes de uñas, etc. se realizará una única presentación
detallando las diferencias enunciadas.
Art. 2° — Los Titulares de
inscripción de productos deberán disponer de la metodología analítica utilizada
en los análisis de los productos que se indican en el Anexo I de la presente
Disposición, determinando los métodos, técnicas y procedimientos
fehacientemente validados a fin de asegurar la calidad de los productos de
higiene personal, cosméticos y perfumes que elabora y/o importa.
La metodología empleada
deberá asegurar el cumplimiento de la especificación prefijada, en la totalidad
de los lotes fabricados.
En el caso de productos importados
se aceptarán protocolos de análisis emitidos en el país de origen siendo
responsabilidad del importador y de su director técnico el cumplimiento de las
especificaciones prefijadas.
Art. 3° — Se determina que
los controles de calidad que deben efectuarse de acuerdo con el tipo de
productos, sus usos y fase etaria son los siguiente:
Control físico-químico
(A.F.Q.)
Todos los productos de
higiene personal, cosméticos y perfumes requieren del desarrollo de controles
físico-químicos para determinar que los mismos cumplen con sus propias
especificaciones.
Control Higiénico (C.H.)
Los productos de higiene
personal, cosméticos y perfumes que tienen como requerimiento el control
higiénico, deben cumplir con los parámetros microbiológicos establecidos que
forman parte del Anexo II de la presente Disposición.
Indices de irritación
primaria dérmica y ocular (I.D. e I.O.): Los Titulares de inscripción de
producto, Establecimientos Productores / Elaboradores o Importadores deberán
disponer de los protocolos de análisis de aquellos productos que elaboren o
importen y que le permitieron establecer los índices de irritación dérmica y
ocular.
Para los productos que así
lo requieran estos ensayos deberán realizarse en forma previa a la solicitud de
admisión de venta de los productos de higiene personal, cosméticos y perfumes.
Toda vez que se realice un
cambio de materia prima o modificación de su calidad perderán validez los
ensayos realizados, debiéndose realizar nuevamente, excepto en aquellos casos
en que la modificación introducida no incremente en absoluto los índices de
irritación dérmica y ocular.
Art. 4° — Comprobación de
propiedades específicas: Aquellos productos que anuncien propiedades
específicas, por ejemplo:
— Dermatológicamente
testeado
— No irritante
— No sensibilizante
— No fototóxico (F.T.)
— Hipoalergénico
— Su seguridad de uso ha
sido comprobada Clínicamente
— Oftalmológicamente
testeado
— Factor de protección
solar (F.P.S.)
— Resistencia al agua (si
corresponde)
— Repelencia
— Otros casos en que se
proclamen propiedades específicas testeadas
Deberán adjuntar ensayos
que lo demuestren o bien literatura científica-técnica que avale el beneficio
específico.
Art. 5° — Cuando la
titularidad del producto a inscribir recaiga en una persona física y/o jurídica
distinta del elaborador y/o importador habilitados solicitantes de la
inscripción, estos deberán acompañar el contrato que los vincula con el titular
del producto a los fines de gestionar la inscripción por su cuenta y orden, en
el que deberá constar el nombre o denominación social del titular, el domicilio
constituido ante la autoridad sanitaria y su número de C.U.I.T.
En ese caso el titular del
producto inscripto, tanto como su elaborador y/o importador serán
solidariamente responsables ante la autoridad registrante por la aptitud
sanitaria del producto.
Art. 6° — Los Productos de
Higiene Personal, Cosméticos y Perfumes, deberán cumplir con las Disposiciones
que dicte ésta Administración Nacional determinando las condiciones y
limitaciones de las materias primas como así también las Normas de Rotulado.
Art. 7° — Para la
solicitud de modificaciones referentes a cambio de: nombre, marca, rótulo,
titular y fórmula se realizará presentando la documentación que forma parte del
Anexo IV de la presente.
Art. 8° — A los fines de
observar el cumplimiento de la presente norma y sus complementarias, la
Autoridad Sanitaria efectuará inspecciones con o sin retiro de muestras en los
establecimientos productores o importadores, los depósitos de los mismos y
bocas de expendio.
Art. 9° — Los productos de
Higiene Personal, Cosméticos y Perfumes inscriptos con anterioridad a la
vigencia de la presente Disposición conservarán el número de la Resolución bajo
la cual fueron inscriptos. Cualquier modificación introducida se hará mediante
la presentación del Anexo IV de la presente y en ese caso deberá hacerse
referencia a la Resolución N° 155/98.
Art. 10. — Toda violación
a las obligaciones y deberes establecidos en la presente y demás normas hará
pasible a quien resultare responsable, de las sanciones establecidas en el
Decreto N° 141/53 y sus actualizaciones (Decreto N° 341/92), sin perjuicio de
las que pudieren aplicar los órganos jurisdiccionales de ser aplicable el
Código Penal.
Art. 11. — Comuníquese a
la Asociación Argentina de Químicos Cosméticos, a la Cámara Argentina de la
Industria de Productos de Higiene y Tocador y demás entidades relacionadas.
Art. 12. — Anótese;
notifíquese a quienes corresponda. Dése a la Dirección Nacional del Registro
Oficial, para su publicación. Cumplido, archívese PERMANENTE. — Pablo M. Bazerque.
ANEXO I
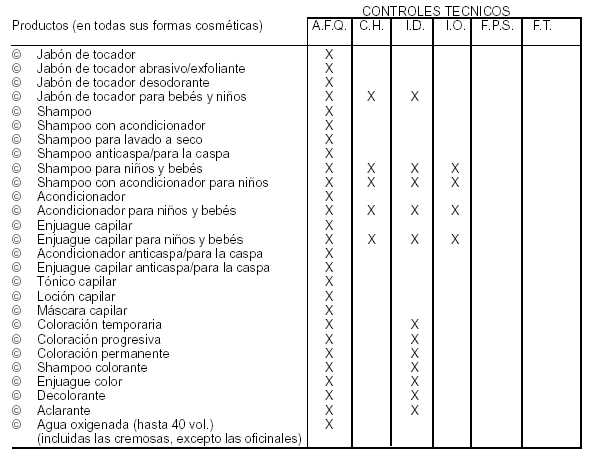
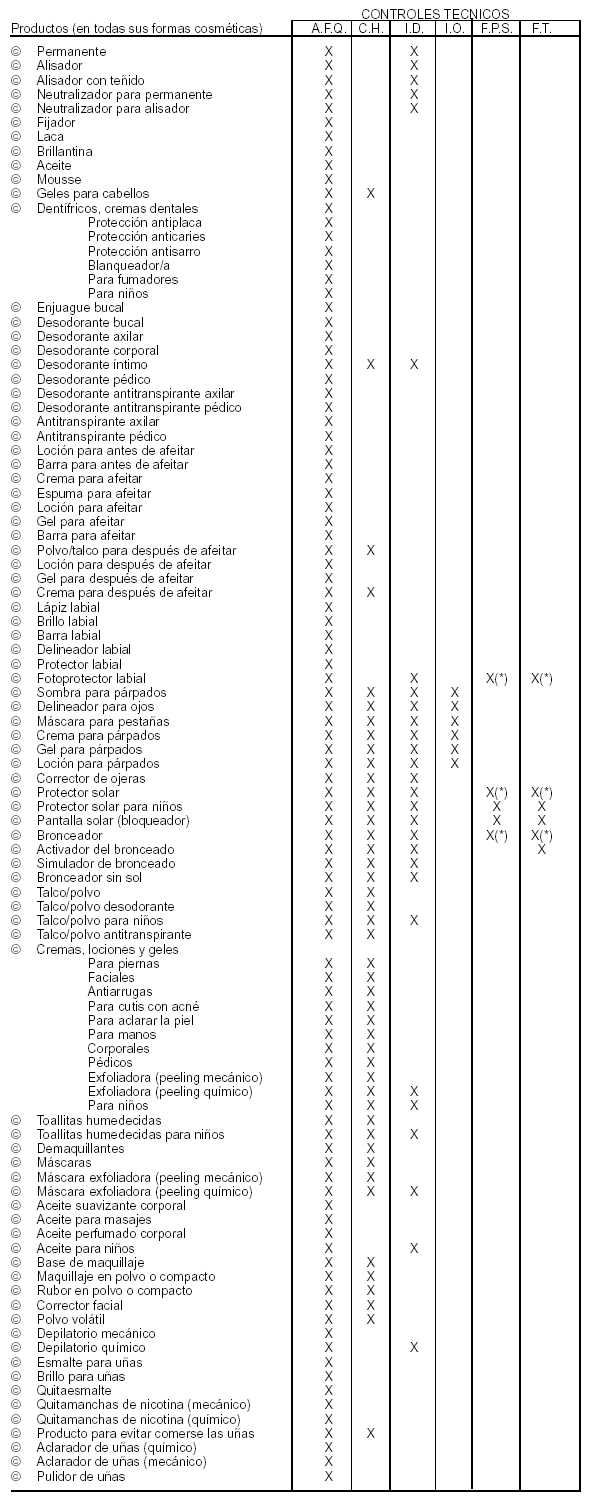
LISTA DE PRODUCTOS DE
HIGIENE PERSONAL, COSMETICOS Y PERFUMES Y SUS REQUERIMIENTOS TECNICOS
|
A.F.Q.
|
Análisis fisicoquímicos
|
|
C.H.
|
Control Higiénico
|
|
I.D.
|
Indice de Irritación
Primaria dérmica
|
|
I.O.
|
Indice de irritación
ocular
|
|
F.P.S.
|
Factor de protección
Solar
|
|
F.T.
|
Fototoxicidad
|

ANEXO II
PARAMETROS DE CONTROL
MICROBIOLOGICO PARA PRODUCTOS DE HIGIENE PERSONAL, COSMETICOS Y PERFUMES
Los límites están
establecidos en función del área de aplicación y fase etaria.
|
|
AREA DE APLICACIÓN Y
FASE ETARIA
|
LIMITES DE ACEPTABILIDAD
|
|
TIPO - I
|
• PRODUCTOS PARA USO
INFANTIL
• PRODUCTOS PARA AREA
OCULAR
• PRODUCTOS QUE ENTRAN
EN CONTACTO CON MUCOSAS
|
a- Recuento de
microorganismos mesófilos aerobios, totales, no más de 102 UFC/g
o ml
Limite máximo 5 x 102 UFC/g
o ml
b- Ausencia de
Pseudomonas aeruginosa en 1 g o ml
c- Ausencia de
Staphylococcus aureus en 1 g o ml
d- Ausencia de
Coliformes totales y fecales en 1 g o ml
e- Ausencia de
Clostridios sulfito Reductores en 1 g (exclusivamente para talcos)
|
|
TIPO - II
|
• DEMAS PRODUCTOS
SUSCEPTIBLES DE CONTAMINACION MICROBIOLOGICA
|
a- Recuento de
microorganismos mesófilos aerobios totales, no más de 103 UFC/g
o ml
Límite máximo 5 x 103 UFC/g
o ml
a- Ausencia de
Pseudomonas aeruginosa en 1 g o ml
b- Ausencia de
Staphylococcus aureus en 1 g o ml
c- Ausencia de
Coliformes totales y fecales en 1 g o ml
d- Ausencia de
Clostridios sulfito reductores en 1 g (exclusivamente para talcos)
|
ANEXO III
FORMULARIO DE PRESENTACION
PARA LA ADMISION DE PRODUCTOS DE HIGIENE PERSONAL, COSMETICOS Y PERFUMES
La presentación se hará en
Mesa de Entradas del Instituto Nacional de Medicamentos, con el arancel
correspondiente, entregándose copia sellada de la misma que habilitará la
comercialización del producto.
Fecha:................................................
Expte.
Nº...........................................
1.— TITULAR DE INSCRIPCION
DEL PRODUCTO: (*)
|
1.1—
|
Nombre o denominación
Social:
|
|
1.2—
|
Domicilio Legal
constituido ante la autoridad sanitaria a los efectos de la registración:
|
|
1.3—
|
Localidad:
|
Código Postal:
|
|
1.4—
|
Teléfono:
|
Fax:
|
|
1.5—
|
Número de Clave Unica de
Identificación Tributaria:
|
(1) Nota: cuando el
titular denunciado en el formulario sea una persona física o jurídica distinta
que el elaborador y/o importador solicitante del registro, se deberá acompañar
copia del certificado de inscripción ante la AFIP y del contrato impuesto por el
artículo 7º de la Resolución (M.S. y A.S.) Nº 155/98 y artículo 5º de la
presente Disposición.
2.— DATOS DEL
ESTABLECIMIENTO PRODUCTOR / ELABORADOR; ENVASADOR / ACONDICIONADOR y/o
IMPORTADOR:
|
2.1—
|
Nombre:
|
|
|
2.2—
|
Actividad (marcar la que
corresponda):
|
|
|
|
|
Productor/Elaborador
|
|
|
|
Envasador/Acondicionador
|
|
|
|
Importador
|
|
2.3—
|
Director Técnico:
|
|
|
2.4—
|
Domicilio Legal del
establecimiento:
|
|
|
2.5.—
|
Localidad:
|
Código Postal:
|
|
2.6.—
|
Teléfono:
|
Fax:
|
|
2.7—
|
Nº de Disposición
Habilitante:
|
|
|
Adjuntar copia de
habilitación del establecimiento. La copia deberá estar firmada por el
Representante Legal y el Director Técnico.
|
|
2.8.—
|
Nº de Legajo:
|
|
|
2.9.—
|
Disposición Habilitante:
|
|
|
Adjuntar copia de la
disposición habilitante del establecimiento. La copia deberá estar firmada
por el Director Técnico.
|
3.— DATOS DEL
ESTABLECIMIENTO CONTRATADO PARA LA ELABORACION Y/O ENVASADO DEL PRODUCTO:
|
3.1—
|
Nombre:
|
|
|
3.2—
|
Actividad: (tachar la
que no corresponde)
|
|
|
|
|
Productor:
|
|
|
|
Envasador:
|
|
3.3—
|
Domicilio Legal:
|
|
|
3.4.—
|
Localidad:
|
Código Postal:
|
|
3.5—
|
Teléfono:
|
Fax:
|
|
3.6—
|
Nº de Disposición
Habilitante:
|
|
|
3.7—
|
Nº de Legajo:
|
|
|
3.8—
|
Director Técnico:
|
|
4.— DATOS DE
ESTABLECIMIENTO CONTRATADO PARA CONTROL DE CALIDAD (si corresponde)
|
4.1.—
|
Nombre:
|
|
|
4.2.—
|
Tipos de Controles:
(tachar la que no corresponde)
|
|
|
4.2.1.—
|
Análisis fisicoquímicos
|
|
|
4.2.2.—
|
Control Higiénico
|
|
|
4.2.3.—
|
Indice de irritación
primaria dérmica.
|
|
|
|
Indice de irritación
ocular.
|
|
|
4.3—
|
Domicilio Legal:
|
|
|
4.4.—
|
Localidad:
|
Código Postal:
|
|
4.5—
|
Teléfono:
|
Fax:
|
|
4.6.—
|
Nº de Legajo:
|
|
|
4.7.—
|
Responsable Técnico:
|
|
|
4.8.—
|
Nº de Disposición
Habilitante:
|
|
5.— DATOS DEL PRODUCTO
|
5.1.—
|
Denominación:
|
|
|
5.2.—
|
Marca:
|
|
|
5.3.—
|
Origen: (tachar el que
no corresponde):
|
|
|
|
|
Nacional
|
|
|
|
Importado
|
|
5.3.1.—
|
País de Origen:
|
|
|
5.4.—
|
Forma Cosmética:
|
|
|
5.5.—
|
Definición Técnica:
|
|
|
5.6.—
|
Función:
|
|
|
5.7.—
|
Indicaciones de Uso:
|
|
|
5.8.—
|
Frecuencia de Uso
Recomendada:
|
|
|
5.9.—
|
Advertencias:
|
|
6.— FORMULA
CUALICUANTITATIVA EXPRESADA EN FORMA CENTISIMAL PESO/PESO
Las concentraciones de
materias primas deben expresarse en % de activos. En los colorantes debe
indicarse el Color Index.
En los productos
importados se deberá adjuntar la fórmula original emitida a nombre del
importador por el laboratorio elaborador en país de origen, consularizada y
legalizada por el Ministerio de Relaciones Exteriores, Comercio Internacional y
Culto o apostillada. Se deberá adjuntar también el Certificado de Libre Venta
emitido en el país de origen, igualmente consularizada y legalizado o
apostillado.
En el caso de que el país
de origen no otorgue el Certificado de Libre Venta, se aceptará la
Certificación por la autoridad sanitaria la que deberá ser igualmente
consularizada y legalizada o apostillada.
|
NOMBRE COMUN
|
NOMENCLATURA INCI
|
%
|
7.— ESPECIFICACIONES
TECNICAS DEL PRODUCTO:
|
1.—
|
Físico-químicos:
|
(dato y
especificaciones):
|
|
|
pH:
|
densidad:
|
|
|
viscosidad:
|
otros:
|
|
2.—
|
Microbiológicos:
|
|
|
|
Tipo I:
|
Tipo II:
|
|
3.—
|
Biológicos (Definir el
grado y mencionar el ensayo empleado)
|
|
|
Irritación Dérmica:
|
|
|
|
Indice de irritación
Ocular:
|
|
|
|
Factor de Protección
Solar:
|
|
|
|
Fototoxicidad:
|
|
|
|
Otros:
|
|
8.— ROTULO Y/O SOBRE
ROTULO
El rótulo y/o sobre rótulo
tanto en el embalaje externo como en el de uso expuesto al consumidor deberá
cumplimentar la Resolución Nº 155/98 en lo referente a la definición de
Productos de Higiene Personal, Cosméticos y Perfumes no pudiendo proclamar actividad
terapéutica alguna, incluso en aquellos casos en que por tratarse de productos
importados se encuentren en otro idioma. Deberá también cumplir con la
Disposición correspondiente de Rotulado.
Adjuntar los textos de
todos los rótulos tal como quedará luego del acondicionamiento (en original,
copia o proyecto de los mismos)
|
...................................................
|
........................................
|
.............................................
|
|
Firma y Aclaración
del Titular del Producto
o Representante Legal
|
Firma y Aclaración
del Director Técnico
|
Firma y Aclaración del
Representante Legal
del Estab. Productor
|
ANEXO IV
FORMULARIO DE SOLICITUD DE
MODIFICACION DE PRODUCTOS DE HIGIENE PERSONAL, COSMETICOS Y PERFUMES A FIN DE
CUMPLIMENTAR el Artículo 7º de la Presente Disposición:
Esta presentación consta
de original y dos copias y reviste el carácter de declaración jurada. Se deberá
acompañar copia firmada por el representante legal y el director técnico de la
autorización vigente.
Fecha:..........................................
Original Expte.
Nº....................................
Modificación Expte.
Nº.....................................
DATOS DEL PRODUCTO
Producto:
Marca:
|
CAMBIO SOLICITADO:
|
VIGENTE
|
PROPUESTO
|
|
—————————————————————————————————————————————
|
|
1. Nombre
|
|
|
|
—————————————————————————————————————————————
|
|
2. Marca
|
|
|
|
—————————————————————————————————————————————
|
|
3. Rótulo y/o sobre
rótulo
|
|
|
|
—————————————————————————————————————————————
|
|
4. Establecimiento
Productor/Elaborador (*)
|
|
|
|
nacional o extranjero
|
|
|
|
Legajo Nº (cuando
corresponda)
|
|
|
|
—————————————————————————————————————————————
|
|
5. Establecimiento
envasador
|
|
|
|
—————————————————————————————————————————————
|
|
6. Fórmula
|
|
|
|
—————————————————————————————————————————————
|
(*) Para cambio de origen
de producto importado deberá presentar fórmula cualicuantitativa y certificado
de libre venta del país de origen.
|
..................................................
|
..........................................................
|
|
Firma y Aclaración
del Titular del Producto
o Representante Legal
|
Firma y Aclaración
Director Técnico
|
Autorización de la
Modificación: .....................................................................................……………………………….
.................................................................................................................................................………………………..
Ciudad de Buenos Aires:.................................................................................………………………………………….