Decreto 1271/2013
Apruébase
estructura organizativa de primer nivel operativo. Decreto Nº 1490/1992 y
Decisión Administrativa Nº 22/2003. Modificaciones.
Bs. As., 29/8/2013
VISTO el Expediente Nº
1-47-18464/11-0 del registro de la ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS Y TECNOLOGIA MEDICA, organismo descentralizado en la órbita de la
SECRETARIA DE POLITICAS, REGULACION E INSTITUTOS del MINISTERIO DE SALUD, el Decreto
Nº 1490 del 20 de agosto de 1992, sus normas complementarias y reglamentarias,
la Decisión Administrativa Nº 22 del 14 de marzo de 2003, y
CONSIDERANDO:
Que por el Decreto Nº
1490 del 20 de agosto de 1992, se creó la ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS Y TECNOLOGIA MEDICA, como organismo descentralizado en la órbita de
la actual SECRETARIA DE POLITICAS, REGULACION E INSTITUTOS del MINISTERIO DE
SALUD.
Que por la Decisión
Administrativa Nº 22 del 14 de marzo de 2003, se aprobó la estructura
organizativa del primer nivel operativo del citado organismo.
Que el crecimiento
cuantitativo del universo de fiscalización, regulación y control de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA requiere
el fortalecimiento de la organización, a fin de dotarla de los instrumentos de
gestión que posibiliten el logro de los objetivos asignados.
Que promover y garantizar
las acciones del sector público dirigidas a la prevención, resguardo y atención
de la salud de la población es una de las políticas prioritarias establecidas
por el Gobierno Nacional.
Que, con el fin de
fortalecer el rol protagónico que cabe cumplir al Sector Público Nacional, es
necesario arbitrar las disposiciones conducentes para permitir a la ADMINISTRACION
NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA ejercer en las
condiciones más adecuadas las funciones de contralor y vigilancia sobre
importantes materias que se encuentran sujetas a la órbita de su competencia.
Que las acciones referidas
al control y fiscalización de la sanidad y calidad de los productos,
substancias, elementos, procesos, tecnologías y materiales que se consumen o
utilizan en la medicina, alimentación y cosmética humanas configuran un campo
de acción muy específico, caracterizado por un elevado nivel de complejidad y
diversidad, tanto técnico como científico.
Que asimismo, para lograr
resultados sostenibles en el tiempo, es necesario acordar políticas sanitarias
comunes entre la Nación, las provincias y por su intermedio con los municipios.
Que sobre la base de lo
que antecede, corresponde reformular la estructura organizativa de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA con el
fin de posibilitar a dicho organismo el desarrollo de las líneas estratégicas
de transformación, fortalecer su capacidad para el análisis de riesgos, la
educación, la vigilancia, la regulación, la fiscalización y el control a los
efectos de garantizar una efectiva acción sanitaria en todo el territorio
nacional, con especial atención a las acciones de prevención y protección.
Que asimismo resulta
necesario establecer un mecanismo de selección para las autoridades superiores
del organismo que garantice su idoneidad.
Que la SECRETARIA DE
GABINETE Y COORDINACION ADMINISTRATIVA de la JEFATURA DE GABINETE DE MINISTROS
y el MINISTERIO DE SALUD aprobarán conjuntamente el Régimen para la Selección
de las Autoridades de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA.
Que en este marco, a
efectos de garantizar el desarrollo de las funciones encomendadas a la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, en
virtud de la criticidad de las mismas y hasta tanto se sustancie el sistema de
selección correspondiente, es menester proceder a la designación del
Administrador Nacional y del Subadministrador.
Que han tomado la
intervención que les compete los servicios jurídicos permanentes de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA y del
MINISTERIO DE SALUD.
Que han tomado la
intervención de su competencia la SECRETARIA DE GABINETE Y COORDINACION
ADMINISTRATIVA de la JEFATURA DE GABINETE DE MINISTROS y la SECRETARIA LEGAL Y
TECNICA de la PRESIDENCIA DE LA NACION, expidiéndose favorablemente.
Que la presente medida se
dicta en uso de las facultades conferidas por el artículo 99, inciso 1, de la
CONSTITUCION NACIONAL.
Por ello,
LA PRESIDENTA DE LA
NACION ARGENTINA
DECRETA:
TITULO I.- DE LA
CONDUCCION
Artículo 1° — Sustitúyese
el artículo 9° del Decreto Nº 1490 de fecha 20 de agosto de 1992 por el
siguiente:
“ARTICULO 9°.- La
dirección, administración y representación de la ADMINISTRACION NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA estará a cargo de un Administrador
Nacional, el que percibirá una remuneración equivalente a la Categoría
Profesional Superior, con Suplemento por Función Directiva de Nivel I, del
Convenio Colectivo de Trabajo Sectorial del Personal Profesional de los
Establecimientos Hospitalarios y Asistenciales e Institutos de Investigación y
Producción dependientes del MINISTERIO DE SALUD homologado por Decreto Nº 1133
de fecha 25 de agosto de 2009.
El Administrador Nacional
será asistido por un Subadministrador Nacional el que percibirá una
remuneración equivalente a la Categoría Profesional Superior, con Suplemento
por Función Directiva de Nivel II, del Convenio Colectivo de Trabajo Sectorial
del Personal Profesional de los Establecimientos Hospitalarios y Asistenciales
e Institutos de Investigación y Producción dependientes del MINISTERIO DE SALUD
homologado por Decreto Nº 1133 de fecha 25 de agosto de 2009.”
Art. 2° — Los cargos de
Administrador Nacional y Subadministrador Nacional serán ejercidos por
profesionales pertenecientes, o que hayan pertenecido, a la carrera profesional
de establecimientos hospitalarios y asistenciales e institutos de investigación
y producción dependientes del MINISTERIO DE SALUD, pertenecientes al Régimen
establecido mediante el Decreto Nº 1133 de fecha 25 de agosto de 2009, quienes
serán designados por el PODER EJECUTIVO NACIONAL de entre una terna resultante
de un proceso de selección llevado a cabo por un Comité de Selección integrado
por: el titular de la SECRETARIA DE POLITICAS, REGULACION E INSTITUTOS del
MINISTERIO DE SALUD, UN (1) representante designado por el MINISTERIO DE SALUD,
UN (1) representante de la SECRETARIA DE GABINETE Y COORDINACION ADMINISTRATIVA
de la JEFATURA DE GABINETE DE MINISTROS, y TRES (3) expertos representantes del
sector académico universitario argentino con incumbencia profesional afín a las
competencias de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA o personalidades de reconocido prestigio en la materia.
La SECRETARIA DE GABINETE
Y COORDINACION ADMINISTRATIVA de la JEFATURA DE GABINETE DE MINISTROS, y el
MINISTERIO DE SALUD aprobarán conjuntamente el Régimen para la Selección de las
autoridades superiores de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS
Y TECNOLOGIA MEDICA.
El Administrador Nacional
y el Subadministrador Nacional se desempeñarán en sus cargos por el término de
CINCO (5) años, pudiendo renovar una sola vez por otro término a propuesta del
Titular de la SECRETARIA DE POLITICAS, REGULACION E INSTITUTOS.
TITULO II.- DE LAS
ATRIBUCIONES
Art. 3° — El Administrador
Nacional y el Subadministrador Nacional de la ADMINISTRACION NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA mantendrán las atribuciones,
obligaciones y las facultades establecidas por los artículos 10 y 14 del
Decreto Nº 1490 de fecha 20 de agosto de 1992 para el ex - Director Nacional y
el ex - Subdirector de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA, respectivamente.
TITULO III.- DE LA
ESTRUCTURA ORGANIZATIVA
Art. 4° — Derógase la Decisión
Administrativa Nº 22 de fecha 14 de marzo de 2003.
Art. 5° — Apruébase la
estructura organizativa de primer nivel operativo de la ADMINISTRACION NACIONAL
DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, organismo descentralizado que
funciona en la órbita de la SECRETARIA DE POLITICAS, REGULACION E INSTITUTOS
del MINISTERIO DE SALUD, de acuerdo con el Organigrama, Responsabilidad
Primaria y Acciones, que como Anexos I y II, respectivamente, forman parte
integrante del presente acto.
Art. 6° — Facúltase al
Administrador Nacional de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS
Y TECNOLOGIA MEDICA a aprobar y/o modificar el Anexo de Dotación de la
estructura organizativa, de conformidad con los créditos y cargos establecidos
por las Leyes de Presupuesto de Gastos y Recursos de la Administración Nacional
vigentes, previa intervención de la SECRETARIA DE GABINETE Y COORDINACION
ADMINISTRATIVA de la JEFATURA DE GABINETE DE MINISTROS.
Art. 7° — La
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA deberá
aprobar en un plazo de SESENTA (60) días, a partir de la publicación del
presente Decreto, la estructura organizativa de nivel inferior a la aprobada,
la que deberá prever un máximo de DIEZ (10) Direcciones y CUARENTA Y NUEVE (49)
Departamentos del CONVENIO COLECTIVO DE TRABAJO SECTORIAL DEL PERSONAL
PROFESIONAL DE LOS ESTABLECIMIENTOS HOSPITALARIOS Y ASISTENCIALES E INSTITUTOS
DE INVESTIGACION Y PRODUCCION DEPENDIENTES del MINISTERIO DE SALUD homologado
por el Decreto Nº 1133/09, y SIETE (7) Direcciones y SEIS (6) Coordinaciones
del SISTEMA NACIONAL DE EMPLEO PUBLICO (SINEP), aprobado por el CONVENIO
COLECTIVO DE TRABAJO SECTORIAL DEL PERSONAL homologado por el Decreto Nº
2098/08. La aprobación de la misma deberá realizarse previa intervención de la
SECRETARIA DE GABINETE Y COORDINACION ADMINISTRATIVA de la JEFATURA DE GABINETE
DE MINISTROS.
TITULO IV.- CLAUSULAS
TRANSITORIAS
Art. 8° — Dase por
finalizada la Intervención de la ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS Y TECNOLOGIA MEDICA que se dispusiera por Decreto Nº 847/00
modificada por sus similares Nros. 197/02, 253/08 y 425/10, por encontrarse
regularizada la situación que promoviera dichos actos.
Art. 9° — Desígnase como
Administrador Nacional de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS
Y TECNOLOGIA MEDICA —ANMAT—, al doctor D. Carlos Alberto CHIALE (D.N.I. Nº
12.091.111), hasta tanto se sustancie el proceso de selección previsto en el
artículo 2° del presente.
Art. 10. — Desígnase como
Subadministrador Nacional de la ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS .Y TECNOLOGIA MEDICA —ANMAT—, al doctor D. Otto Alberto ORSINGHER
(L.E. Nº 7.436.762), hasta tanto se sustancie el proceso de selección previsto
en el artículo 2° del presente.
Art. 11. — La SECRETARIA
DE GABINETE Y COORDINACION ADMINISTRATIVA de la JEFATURA DE GABINETE DE
MINISTROS y el MINISTERIO DE SALUD, en un plazo de NOVENTA (90) días aprobarán
conjuntamente el Régimen para la Selección de las autoridades de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
Art. 12. — Hasta tanto se
concluya con la reestructuración de las áreas afectadas por la presente medida,
mantendrán su vigencia las aperturas estructurales existentes con nivel
inferior a las aprobadas por el presente Decreto, las que transitoriamente
mantendrán las responsabilidades primarias y dotaciones vigentes a la fecha,
con sus respectivos niveles, grados de revista y funciones ejecutivas y
directivas, compensaciones y suplementos que les correspondiere, previstos en
la normativa escalafonaria.
TITULO V.- DEL
PRESUPUESTO
Art. 13. — El gasto que
demande el cumplimiento de la presente medida será atendido con los créditos
asignados a la Entidad 904 - ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS
Y TECNOLOGIA MEDICA.
Art. 14. — Comuníquese,
publíquese, dése a la DIRECCION NACIONAL DEL REGISTRO OFICIAL y archívese. —
FERNANDEZ DE KIRCHNER. — Juan M. Abal Medina. — Juan L. Manzur.
ANEXO I
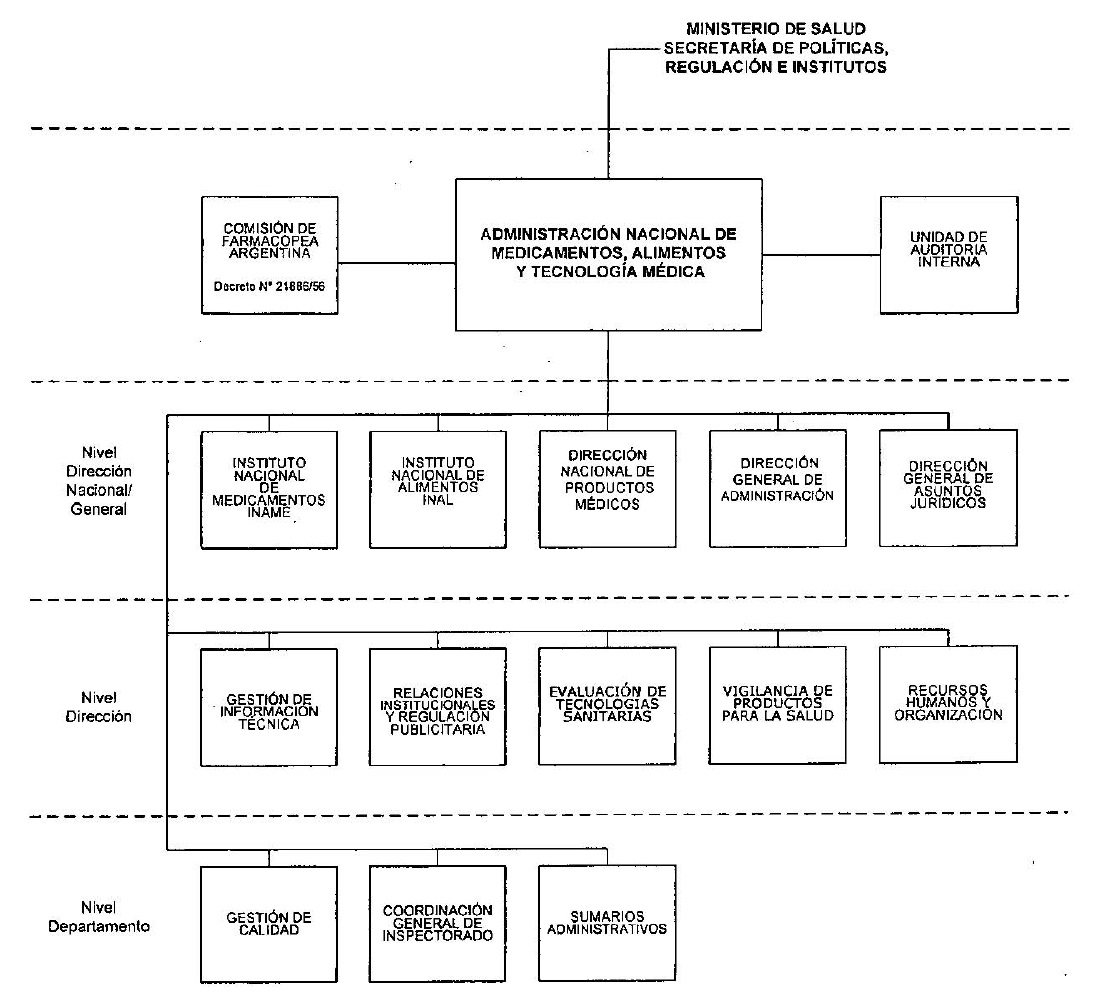
ANEXO II
MINISTERIO DE SALUD
SECRETARIA DE POLITICAS,
REGULACION E INSTITUTOS
ADMINISTRACION NACIONAL
DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
UNIDAD DE AUDITORIA
INTERNA
RESPONSABILIDAD PRIMARIA:
Realizar exámenes
integrales de las actividades, procesos y resultados de la ADMINISTRACION
NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA de manera de asegurar
niveles continuos de eficacia, eficiencia y economía en la gestión.
ACCIONES:
1.- Elaborar el ciclo de
auditoría y los planes anuales de auditoría que lo conforman.
2.- Evaluar el
cumplimiento de las políticas, planes y procedimientos determinados por la
autoridad superior.
3.- Tomar conocimiento en
forma integral de los actos administrativos, evaluando aquellos de
significativa trascendencia económica.
4.- Verificar el
cumplimiento de los niveles presupuestarios de la normativa legal vigente.
5.- Constatar la
confiabilidad de los antecedentes utilizados en la elaboración de los informes
de Auditoría.
6.- Comunicar a la
autoridad superior y a la SINDICATURA GENERAL DE LA NACION los resultados de
los informes practicados y de las sugerencias o recomendaciones que se
efectúen.
7.- Efectuar el
seguimiento de las recomendaciones u observaciones realizadas.
8.- Informar a la
SINDICATURA GENERAL DE LA NACION sobre temas que sean requeridos en lo atinente
al desarrollo de actividades de la Unidad de Auditoría Interna.
9.- Evaluar los cambios
que se produzcan en el esquema presupuestario del Organismo y su incidencia en
la formulación de planes.
10.- Apreciar el
comportamiento técnico-profesional en el desarrollo de las acciones de la
Unidad, evaluando los rendimientos individuales y los resultados por programas.
INSTITUTO NACIONAL DE
MEDICAMENTOS
RESPONSABILIDAD PRIMARIA:
Definir y planificar las
acciones dirigidas a la prevención, resguardo y atención de la salud de la
población que se desarrollen a través del control, la fiscalización y la
vigilancia de la calidad de medicamentos, ingredientes farmacéuticos activos,
productos biológicos y materiales de partida, mediante la evaluación clínica,
terapéutica y de calidad farmacéutica de los medicamentos, los estudios
farmacotécnicos, biológicos, farmacológicos y toxicológicos, como así también
de las actividades, procesos y tecnologías que se realicen en función de la
elaboración, fraccionamiento, importación y/o exportación, depósito y comercialización
de dichos productos.
ACCIONES:
1.- Controlar y
fiscalizar la sanidad y calidad de los productos químicos, drogas, formas
farmacéuticas y medicamentos.
2.- Ejercer la vigilancia
sobre la eficacia y la detección de los efectos adversos que resulten del
consumo y utilización de los productos de su incumbencia, como también la
referida a la presencia en los mismos de todo tipo de sustancias o residuos,
orgánicos e inorgánicos, que puedan afectar la salud de la población.
3.- Realizar el control
por medio de inspecciones de las actividades, procesos y tecnologías que se
realicen en función de la producción, elaboración, fraccionamiento,
importación, exportación y depósito de los productos químicos, drogas,
medicamentos y productos biológicos.
4.- Supervisar la
inscripción, la autorización y la certificación en cumplimiento de las
disposiciones pertinentes para los productos, sustancias, tecnologías y
procesos referidos a los productos de su incumbencia.
5.- Fiscalizar el
cumplimiento de las normas de calidad establecidas para los productos,
sustancias, tecnologías y procesos referidos a los productos de su incumbencia.
6.- Intervenir en las
acciones conducentes para otorgar la habilitación y/o autorización de
funcionamiento de establecimientos y plantas dedicadas a la producción,
elaboración, fraccionamiento, importación y/o exportación y depósito de los
medicamentos, ingredientes farmacéuticos activos, sustancias y laboratorios de
control relacionados; así como también en las modificaciones o cambios de rubro
de las licencias ya otorgadas.
7.- Supervisar la
autorización de ensayos clínicos y de bioequivalencia.
8.- Proponer ante la
detección de cualquier factor de riesgo relacionado con la calidad y sanidad de
los productos, sustancias, tecnologías y procesos referidos a los productos de
su incumbencia, las medidas más oportunas y adecuadas para proteger la salud de
la población, conforme a la normativa vigente.
9.- Elaborar y proponer
proyectos de normas técnicas y complementarias, modificatorias y/o aclaratorias
a la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA,
las que podrán aplicarse en función de la adecuación, sanidad y calidad
relativas a la producción, elaboración, fraccionamiento, importación y/o
exportación y depósito de los productos, sustancias y procesos referidos a los
productos de su incumbencia.
10.- Elaborar y elevar el
programa anual y plurianual de actividades y trabajo a los efectos de ser
considerado en la elaboración del presupuesto y el cálculo de recursos para su
funcionamiento.
11.- Proponer los
aranceles y tasas retributivas correspondientes a los trámites y registros que
se efectúen como también por los servicios que se presten.
12.- Realizar controles,
verificaciones e inspecciones, en función de las competencias atribuidas al
organismo, recabando, cuando ello sea necesario el auxilio de la fuerza
pública, así como la cooperación de otros organismos públicos.
13.- Proponer la
destrucción de los bienes que fuesen decomisados por infracciones a la
normativa de rigor o por carecer de condiciones de aptitud para ser consumidos
por la población o bien, en el caso de que fueran de origen importado, ordenar
su reexportación a cargo del importador.
14.- Proponer modalidades
de interacción y cooperación científica y académica con los diferentes sectores
públicos y privados, en coordinación con la Dirección de Relaciones
Institucionales y Regulación Publicitaria.
15.- Contribuir a la
evaluación y control de la pertinencia y legitimidad de los productos o insumos
que se importan o exportan con fines de investigación clínica.
INSTITUTO NACIONAL DE
ALIMENTOS
RESPONSABILIDAD PRIMARIA:
Velar por la protección
de la salud de la población, por los riesgos asociados a los alimentos;
contribuir a la prevención de las enfermedades transmitidas por los alimentos y
las enfermedades no transmisibles relacionadas con los alimentos; contribuir al
desarrollo productivo manteniendo la confianza de la población en el sector
alimentario y coordinar las actividades del sistema federal de control con los
organismos sanitarios de orden nacional, jurisdiccional, y por su intermedio, con
los de orden municipal.
ACCIONES:
1.- Promover la salud de
la población, asegurando la inocuidad y calidad de los productos alimenticios,
insumos y los materiales en contacto directo con los alimentos.
2.- Organizar y dirigir
las actividades de evaluación, gestión y comunicación de riesgos en el ámbito
de su competencia.
3.- Promover el abordaje
multidisciplinario e integrado de las actividades de vigilancia de los
alimentos y de las enfermedades relacionadas con los mismos.
4.- Fiscalizar y
controlar las actividades y autorizar e inscribir los productos comprendidos en
la Ley Nº 18.284 y la que se le asigne como parte de sus competencias.
5.- Otorgar y cancelar
las autorizaciones de importación y exportación en el ámbito de su competencia.
6.- Planificar, organizar
y coordinar las actividades de vigilancia y control del comercio internacional
de los productos de su competencia.
7.- Planificar, organizar
y coordinar las actividades de vigilancia, de la evaluación de riesgos y de la
exposición a substancias presentes o en contacto con productos de su
competencia en función de la protección de la salud.
8.- Proponer el
establecimiento de un sistema de monitoreo, control y auditoría sanitaria preventivos
basado en el análisis de riesgos.
9.- Planificar, organizar
y coordinar en el ámbito nacional las acciones frente a incidentes asociados a
los productos de su competencia.
10.- Organizar y
coordinar actividades de información, sensibilización y educación con la
finalidad de promover conductas alimentarias seguras y saludables en
coordinación con la Dirección de Relaciones Institucionales y Regulación
Publicitaria de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA.
11.- Diseñar estrategias
que contribuyan con la evaluación de las tendencias de consumo de alimentos de
la población y su relación con las condiciones de salud.
12.- Organizar y
coordinar el diseño de estrategias desde la perspectiva de los procesos tecnológicos
y normativos que contribuyan a la mejora en la calidad nutricional de los
alimentos.
13.- Promover y dirigir
la evaluación científica de los productos, ingredientes alimentarios o parte de
ellos y las declaraciones de propiedades en materia de alimentos que confieran
beneficios para la salud.
14.- Promover el
relevamiento y estudio de la relación entre las nuevas tecnologías y la salud
en el área de su competencia.
15.- Promover la
actualización normativa sobre una base científico-técnica y en las
recomendaciones regionales e internacionales en la materia.
16.- Asesorar en materia
normativa a los integrantes del sistema federal de control en el ámbito de su
competencia.
17.- Integrar los grupos
técnicos nacionales, regionales e internacionales en temas de su incumbencia.
18.- Promover y
normalizar sistemas de información sanitaria que permitan una gestión eficaz y
preventiva del sistema federal de control y una rápida toma de decisión en
resguardo de la salud.
19.- Liderar y articular
con las Autoridades Sanitarias Jurisdiccionales las acciones y tareas
contenidas en el Programa Federal de Control de Alimentos, su evaluación y
revisión permanente.
20.- Asistir en la
cooperación a los organismos sanitarios de orden nacional, provincial y
municipal.
21.- Promover el
fortalecimiento de la vinculación técnica permanente con las entidades
científicas, académicas, profesionales, empresariales, de los trabajadores y
los organismos no gubernamentales en la temática en coordinación con la
Dirección de Relaciones Institucionales y Regulación Publicitaria, de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
22.- Promover y coordinar
la conformación de redes de trabajo, intercambio y formación entre los
diferentes actores públicos y privados en el ámbito de competencia del
Instituto Nacional de Alimentos.
23.- Promover el
intercambio y la cooperación con organismos nacionales, regionales e internacionales
en temas de su incumbencia.
24.- Proponer los
aranceles y tasas retributivas correspondientes a los trámites y registros que
se efectúen como también por los servicios que se presten.
DIRECCION NACIONAL DE
PRODUCTOS MEDICOS
RESPONSABILIDAD PRIMARIA:
Controlar, fiscalizar,
evaluar y vigilar la calidad de los productos (equipamientos, aparatos,
materiales y sistemas de uso o aplicación médica, odontológica o laboratorial)
destinados a la prevención, diagnóstico, tratamiento, rehabilitación o anticoncepción
que no utilicen medios farmacológicos, inmunológicos o metabólicos para
realizar su función principal en seres humanos, pudiendo ser auxiliados en su
función por tales medios, como así también las actividades, procesos y
tecnologías que se realicen en función de la fabricación, fraccionamiento,
importación, distribución y/o exportación y depósito de dichos productos con el
fin de asegurar productos médicos de evaluada calidad, seguridad y eficacia
para la población.
ACCIONES:
1.- Dirigir la
fiscalización de los establecimientos dedicados a la fabricación,
fraccionamiento, importación, distribución y/o exportación y depósito de
productos médicos.
2.- Certificar e
inscribir los productos médicos en cumplimiento de las disposiciones
pertinentes.
3.- Aplicar las medidas
de seguridad más oportunas y adecuadas para proteger la salud de la población y
las sanciones que sean de su competencia.
4.- Elaborar, proponer,
divulgar y actualizar las normas científicas y técnicas que sean aplicables en
función de la adecuación, sanidad y calidad relativas a la producción,
elaboración, fraccionamiento, importación y/o exportación, comercialización y
depósito de los productos médicos.
5.- Evaluar y controlar
la continuidad de la habilitación y/o autorización, de las personas físicas o
jurídicas que intervengan en las acciones de producción, elaboración,
fraccionamiento, importación y/o exportación, depósito y comercialización de
los productos médicos.
6.- Proponer los
aranceles y tasas retributivas correspondientes a los trámites e inscripciones
que se efectúen como también para los servicios que se presten.
7.- Disponer la
realización de controles, verificaciones e inspecciones que se consideren
adecuados, recabando cuando ello sea necesario, el auxilio de la fuerza pública
y/o la cooperación de todo otro organismo público.
8.- Fortalecer la
comunicación con las autoridades sanitarias jurisdiccionales a los fines de
optimizar la estructura de intercambio de información y experiencia.
9.- Promover el
intercambio y la cooperación con organismos nacionales, regionales e
internacionales en temas de su incumbencia.
10.- Contribuir al
fortalecimiento del intercambio científico con entidades académicas, de
investigación, de desarrollo científico y tecnológico de su ámbito de
competencia, en coordinación con la Dirección de Relaciones Institucionales y
Regulación Publicitaria de la ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS Y TECNOLOGIA MEDICA.
DIRECCION GENERAL DE
ADMINISTRACION
RESPONSABILIDAD PRIMARIA:
Entender en la dirección
de la gestión económica, financiera, contable, administrativa, patrimonial y de
servicios de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA
MEDICA y en la coordinación de las tecnologías informáticas.
ACCIONES:
1.- Asistir en el diseño
de la política presupuestaria del Organismo y en la evaluación de su
cumplimiento.
2.- Coordinar la
formulación del anteproyecto de presupuesto.
3.- Efectuar las
registraciones dispuestas por la Ley de Administración Financiera y de los
Sistemas de Control del Sector Público Nacional Nº 24.156.
4.- Administrar los
ingresos y egresos de fondos de origen presupuestario.
5.- Supervisar el
movimiento, custodia y manejo de fondos de la entidad.
6.- Compatibilizar,
evaluar e implementar los distintos requerimientos de las dependencias del
organismo vinculados con la adquisición y contratación de bienes y servicios.
7.- Gestionar y
supervisar las contrataciones de refuncionalización y de mantenimiento de los
edificios del Organismo.
8.- Coordinar las
actividades de tecnología de la información del Organismo, incluyendo
infraestructura de equipamiento, software y de comunicaciones de datos y de
voz, los sistemas de información y las tecnologías asociadas.
9.- Definir y supervisar
las modalidades de percepción de recursos y pago a proveedores.
10.- Coordinar la gestión
del despacho y protocolización de los actos administrativos generados por la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
11.- Coordinar la
recepción y salida de la documentación administrativa, efectuando su
seguimiento y archivo.
12.- Coordinar y
supervisar el cumplimiento del control y asignación de los bienes patrimoniales
del Organismo, su actualización y aplicación de las normativas que
correspondan.
13.- Actuar como
autoridad de registro en los términos de la Ley Nº 25.506 y su Decreto
reglamentario Nº 2.628/02.
DIRECCION GENERAL DE
ASUNTOS JURIDICOS
RESPONSABILIDAD PRIMARIA:
Entender en los asuntos
relativos a la legislación general e instrumentación normativa en la que tiene
competencia el Organismo, como así también, en el perfeccionamiento de las
disposiciones legales y reglamentarias, en el control de legitimidad y
legalidad de los actos y procedimientos administrativos. Representar y asesorar
jurídicamente a la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA.
ACCIONES:
1.- Ejercer el control de
la legalidad y legitimidad de los actos administrativos.
2.- Asesorar en forma
permanente en los aspectos legales a las distintas áreas de la ADMINISTRACION
NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
3.- Entender en la
evaluación de los aspectos legales de los estudios y ensayos en farmacología clínica,
productos médicos y todo otro producto vinculado a la salud humana de
competencia de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA.
4.- Entender en la
producción de normas jurídicas necesarias para el mejor desarrollo de las
actividades de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA.
5.- Asistir a la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA en el
análisis y evaluación de los aspectos técnicos, legales en materia de
relaciones laborales en general, procesos licitatorios y demás trámites
vinculados a la Ley de Administración Financiera y de los Sistemas de Control
del Sector Público Nacional Nº 24.156.
6.- Representar a la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, en los
juicios en los que sea parte como actor o demandado por intermedio de los
apoderados que designe al efecto con relación a los derechos y obligaciones de
que pueda ser titular, pudiendo transigir, comprometer en árbitros, prorrogar
jurisdicciones, desistir de apelaciones y renunciar a prescripciones
adquiridas, contestar los oficios judiciales y remitirlos a los que deben
intervenir en su diligenciamiento y realizar todos aquellos actos necesarios
tendientes a iniciar, proseguir y concluir juicios.
7.- Instruir los sumarios
sanitarios originados por contravenciones a la legislación respecto de la cual
la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA es
organismo de aplicación.
DIRECCION DE GESTION DE
INFORMACION TECNICA
RESPONSABILIDAD PRIMARIA:
Coordinar la gestión y la
administración de la información generada como consecuencia de las acciones de
registro, regulación y control referidas a los alimentos, medicamentos,
productos médicos, cosméticos y domisanitarios, plantas elaboradoras,
importadores-exportadores, distribuidores y otros establecimientos de
incumbencia de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA, y prestar servicios de consulta de información de acceso
público.
ACCIONES:
1.- Consolidar y
gestionar la información técnica sobre medicamentos, alimentos, productos
médicos, cosméticos, domisanitarios y establecimientos.
2.- Generar información
validada para las distintas áreas de la ADMINISTRACION NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, entes y organismos oficiales,
sobre los productos y establecimientos obrantes en sus Registros.
3.- Supervisar y
coordinar los análisis prospectivos de la información generada que contribuyan
con la planificación estratégica de la ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS Y TECNOLOGIA MEDICA.
4.- Relevar y organizar
los datos considerados prioritarios para el diseño y la implementación de las
iniciativas que mejoren el cumplimiento de las funciones sanitarias.
5.- Promover la gestión
de la información a nivel federal de los aspectos legales y de procedimiento en
las materias de competencia de la ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS Y TECNOLOGIA MEDICA.
6.- Desarrollar productos
de información sistematizada referentes a las competencias de la ADMINISTRACION
NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, útiles para los
procesos de toma de decisiones en salud.
7.- Promover el resguardo
y el mantenimiento actualizado de los legajos correspondientes a productos y
establecimientos autorizados en el ámbito de la competencia de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
8.- Incorporar las
tecnologías de información y comunicación para dar respuesta a las necesidades
internas de información en salud, según estándares adecuados de accesibilidad.
DIRECCION DE RELACIONES
INSTITUCIONALES Y REGULACION PUBLICITARIA
RESPONSABILIDAD PRIMARIA:
Diseñar, proponer y
ejecutar la estrategia institucional en términos de comunicación y difusión;
promover y fortalecer el desarrollo de las relaciones institucionales con todos
los públicos estratégicos en temas vinculados al universo de competencia de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA; como
así también organizar las actividades del ceremonial y el protocolo y las de comunicación
interna.
Establecer e impulsar la
relación con las distintas instituciones científicas de la salud con el fin de
generar información estratégica de retroalimentación de los procesos decisorios
basados en paradigmas científicos.
Proponer y desarrollar el
plan estratégico de fortalecimiento de las capacidades de regulación,
fiscalización y vigilancia sanitaria a nivel nacional y provincial que
involucre los productos de competencia de la ADMINISTRACION NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
Velar por el cumplimiento
de la normativa en materia publicitaria a través del monitoreo y fiscalización
de toda comunicación publicitaria de los productos sujetos a vigilancia
sanitaria, como así también coordinar las relaciones de cooperación y
articulación internacional.
ACCIONES:
1.- Diseñar, proponer e
implementar la estrategia comunicacional de la Organización dirigida a los
públicos externos y al público interno.
2.- Establecer las vías
de comunicación adecuadas en términos de favorecer la comunicación y la
difusión de la producción científica e institucional.
3.- Promover la cultura,
la identidad, la imagen, la misión, la visión y los valores de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA, en la
mente de sus públicos externos e internos, a fin que la Institución permita ser
identificada y posicionada favorablemente.
4.- Organizar y dirigir
la relación con los medios masivos de comunicación con el fin de sensibilizar,
informar y educar acerca de temas de competencia de la Administración.
5.- Analizar los
resultados de las acciones de comunicación en función de los objetivos
establecidos por la autoridad pertinente.
6.- Establecer vínculos
con organizaciones intermedias, públicas o privadas, de reconocido prestigio y
representativas de la comunidad, a fin de conocer sus necesidades y
expectativas.
7.- Diseñar y promover
acuerdos con entidades de distintos niveles y ámbitos, que propendan a la
optimización de las acciones para el mejor cumplimiento de los objetivos de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
8.- Desarrollar y
promover las acciones y programas atinentes a la fiscalización y control de la
publicidad de productos para la salud.
9.- Promover programas de
divulgación de las acciones de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS
Y TECNOLOGIA MEDICA, dirigidos a la población en general y a sectores
especiales que se definan como de interés particular.
10.- Definir pautas
generales y contenidos para la difusión de temas de salud vinculados con
productos de incumbencia de la Administración.
11.- Difundir la
información pertinente referida a temas de diversa índole de incumbencia de la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA a través
de los medios de comunicación disponibles para tal fin.
12.- Administrar la
publicación de la información relacionada con alertas, retiro de productos y
sanciones originadas en las áreas competentes de la ADMINISTRACION NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
13.- Organizar y dirigir
la diagramación y contenidos acorde a la estrategia de la comunicación, externa
e interna, definida para ser efectuada mediante los medios informáticos y
otros, como así también gestionar, editar y publicar las publicaciones
científicas de la Institución.
14.- Organizar los actos
oficiales que se dispongan, como así también asistir transversalmente a toda la
institución gestionando y ejecutando actividades de ceremonial y protocolo.
15.- Conducir la labor y
establecer la estrategia de gestión de comunicación del área que brinda
respuesta al público —ANMAT Responde—.
16.- Impulsar planes de
acción en el escenario de las relaciones exteriores y liderar los desafíos que
presentan los procesos de integración, de cooperación y de representación
internacionales.
17.- Gestionar y promover
la participación de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA en los foros internacionales y en la celebración de convenios
bilaterales y multilaterales que pueden brindar nuevas capacidades para la Institución,
permitiendo analizar, adoptar y evaluar medidas aplicadas, en el ámbito
internacional, ante problemáticas similares.
18.- Establecer un fluido
intercambio con entidades extranjeras y organismos multilaterales vinculados
con el área de competencia de esta Administración, como así también elaborar
los actos administrativos relacionados con los viajes oficiales.
19.- Diseñar e
implementar las herramientas que efectivicen la relación del Organismo con
distintas instituciones del ámbito de la salud y con la ciudadanía para obtener
información integradora y multisectorial que permita realizar diagnósticos
sobre productos y procesos que son competencia de la ADMINISTRACION NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
20.- Recibir, producir,
sistematizar, interpretar .y comunicar información confiable y oportuna
obtenida a partir de fuentes primarias y secundarias para orientar acciones y
fortalecer la toma de decisiones.
21.- Asistir
operativamente las decisiones del ADMINISTRADOR NACIONAL en lo inherente a la
implementación del PLAN ANMAT FEDERAL, vinculado al fortalecimiento de las
capacidades de regulación, fiscalización y vigilancia a nivel nacional y
provincial articulando las acciones de trabajo con las áreas involucradas.
22.- Coordinar y promover
las acciones necesarias para fortalecer el PLAN ANMAT FEDERAL, manteniendo
estrechas relaciones con las áreas técnicas de los Ministerios de Salud
provinciales.
DIRECCION DE EVALUACION
DE TECNOLOGIAS SANITARIAS
RESPONSABILIDAD PRIMARIA:
Asistir a la
ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA en la
evaluación de la efectividad de las tecnologías sanitarias relacionadas con
medicamentos, dispositivos, procedimientos y modos de intervención utilizados
con el fin de prevenir, diagnosticar, tratar o rehabilitar a los individuos que
presenten o puedan presentar condiciones que afecten su estado de salud, en los
aspectos relacionados a procesos y productos innovadores y que resulten de
interés para la salud pública, como herramienta clave para orientar la toma de
decisiones de manera racional, basada en métodos científicos.
ACCIONES:
1.- Contribuir a
fortalecer las decisiones de la ANMAT mediante la elaboración de evaluaciones
sistemáticas de efectividad y toxicidad acordes al método científico, de la
evidencia científica relacionada a los temas de su competencia.
2.- Generar informes de
evaluación y/o recomendaciones de uso de las tecnologías, recolectando las
evidencias científicas publicadas y disponibles para la determinación de
oportunidad y/o conveniencia de su uso.
3.- Administrar la
información relativa a la evaluación de Tecnologías Sanitarias a través de
herramientas ágiles y confiables de recolección, almacenamiento y divulgación
de datos a fin de priorizar investigaciones aplicadas y desarrollos
estadísticos.
4.- Contribuir al
mejoramiento permanente de la capacidad fiscalizadora de la ANMAT y de los
organismos públicos jurisdiccionales que realizan tareas de fiscalización en
sus ámbitos de injerencia.
5.- Contribuir a la
evaluación y control de la pertinencia y legitimidad de los productos o insumos
que se importan o exportan, para la asistencia de la salud de personas
particulares.
6.- Representar a la
ANMAT y participar de las actividades de la Unidad Coordinadora de Evaluación y
Ejecución de Tecnologías en Salud (UCEETS) creada por Resolución MS Nº 458/09,
y colaborar con la revisión y evaluación de informes producidos por otras entidades
que integran la UCEETS.
7.- Participar de las
actividades de la Red Argentina Pública de Evaluación de Tecnologías Sanitarias
(RedARETS).
8.- Establecer un fluido
intercambio de información con entidades similares, nacionales o extranjeras, y
organismos multilaterales vinculados con el área, priorizando a los que
faciliten el desarrollo científico.
DIRECCION DE VIGILANCIA
DE PRODUCTOS PARA LA SALUD
RESPONSABILIDAD PRIMARIA:
Asistir en la
fiscalización y vigilancia del mercado de medicamentos, productos médicos, y
otros productos que así lo requieran. Intervenir en el control, la
fiscalización y la vigilancia de la calidad de otros productos vinculados a la
salud humana como productos de higiene personal, cosméticos y perfumes,
productos de higiene oral de uso odontológico, productos de uso doméstico o
domisanitarios y otros productos de competencia de la ADMINISTRACION NACIONAL
DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
ACCIONES:
1.- Monitorear y
fiscalizar, de manera permanente, la cadena de distribución de medicamentos y
productos médicos, de oficio y a partir de reportes, con el fin de
contrarrestar el comercio, distribución y entrega de medicamentos y productos
médicos ilegítimos.
2.- Desarrollar y
promover las acciones tendientes a controlar y fiscalizar la sanidad y calidad
de los productos vinculados a la salud humana como productos de higiene
personal, cosméticos y perfumes, productos de higiene oral de uso odontológico,
productos de uso doméstico o domisanitarios y otros productos que así lo
requieran.
3.- Entender en la
evaluación de los trámites de solicitudes de inscripción, en el registro,
modificación y reinscripción de los productos de incumbencia de la Dirección.
4.- Intervenir en la
verificación de la legitimidad de los productos para la salud existentes en el
mercado ante los respectivos titulares de registro, elaboradores o importadores
de los mismos.
5.- Verificar el
cumplimiento del Sistema Nacional de Trazabilidad de Medicamentos aprobada por
Resolución MS Nº 435/11 y complementada por Disposición ANMAT Nº 3683/11.
6.- Evaluar, en
coordinación con las áreas pertinentes de la Administración, la factibilidad y
procedencia de medidas preventivas, a los efectos de prevenir cualquier
situación de riesgo sanitario que pudiera suscitarse.
7.- Intervenir en las
actividades de vigilancia realizando la recopilación, el análisis y el registro
de situaciones de riesgo sanitario que aparezcan durante la etapa de
comercialización de los medicamentos, productos médicos y otros productos que
así lo requieran.
8.- Ejercer la vigilancia
sobre la eficacia, seguridad y la detección de los efectos adversos que
resulten del consumo y utilización de los productos de higiene personal,
cosméticos y perfumes, productos de higiene oral de uso odontológico, productos
de uso doméstico o domisanitarios y otros productos que así lo requieran, como
también la referida a la presencia en los mismos de todo tipo de sustancias o
residuos, orgánicos e inorgánicos, que puedan afectar la salud de la población.
9.- Realizar el control
por medio de inspecciones de las actividades, procesos y tecnologías que se
realicen en función de la producción, elaboración, fraccionamiento,
importación, exportación, depósito y comercialización de los productos de
higiene personal, cosméticos y perfumes, productos de higiene oral de uso
odontológico, productos de uso doméstico o domisanitarios y otros productos que
así lo requieran.
10.- Supervisar la
inscripción, autorización y la certificación en cumplimiento de las disposiciones
pertinentes para los productos, sustancias, tecnologías y procesos referidos a
los productos de higiene personal, cosméticos y perfumes, productos de higiene
oral de uso odontológico, productos de uso doméstico o domisanitarios y otros
productos que así lo requieran.
11.- Fiscalizar el
cumplimiento de las normas de calidad establecidas para los productos y
procesos referidos a los productos de higiene personal, cosméticos y perfumes,
productos de higiene oral de uso odontológico, productos de uso doméstico o
domisanitarios y otros productos que así lo requieran.
12.- Intervenir en las
acciones conducentes para otorgar la habilitación y/o autorización de
funcionamiento de establecimientos y plantas dedicadas a la producción,
elaboración, fraccionamiento, importación y/o exportación y depósito de los
productos de su incumbencia; así como también en las modificaciones o cambios
de rubro de las licencias ya otorgadas.
13.- Intervenir en las
acciones conducentes para otorgar la habilitación y/o autorización de
funcionamiento de droguerías y distribuidoras-operadores logísticos de
medicamentos y distribuidoras de productos médicos que actúen a nivel
interjurisdiccional y en las modificaciones posteriores a las habilitaciones
otorgadas, velando por el cumplimiento de las Buenas Prácticas de
Almacenamiento, Distribución y Transporte que resulten aplicables de
conformidad con la normativa vigente.
14.- Intervenir
activamente en la gestión de resolución de denuncias y/o reportes con relación
a su ámbito de competencia y disponer la realización de inspecciones a los
efectos de su verificación y seguimiento.
15.- Coordinar acciones
con otras dependencias de la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS
Y TECNOLOGIA MEDICA para el desarrollo e implementación de programas de
fiscalización y vigilancia de productos y establecimientos de competencias
compartidas.
16.- Proponer ante la
detección de cualquier factor de riesgo relacionado con la calidad y sanidad de
los productos de su incumbencia, las medidas más oportunas y adecuadas para
proteger la salud de la población, conforme a la normativa vigente.
17.- Atender en la
gestión efectiva de la comunicación de los resultados obtenidos en los
diferentes procedimientos de inspección y verificación.
18.- Informar, a las
áreas pertinentes, toda situación detectada en el área de su competencia que
pudiera configurar la comisión de un delito penal.
19.- Asistir en la
armonización de los Proyectos, Programas y Planes de normas vinculadas al
combate de la falsificación de medicamentos y productos médicos y otras áreas
de incumbencia de la Dirección, emanadas del Administrador Nacional u otra
autoridad pública competente.
20.- Elaborar y proponer
proyectos de normas técnicas y complementarias, modificatorias y/o aclaratorias
a la Administración Nacional, las que podrán aplicarse en función de la
adecuación, sanidad y calidad relativas a la producción, elaboración,
fraccionamiento, importación y/o exportación, depósito y comercialización de
los productos de su incumbencia.
21.- Coordinar la
interacción institucional con autoridades judiciales, aduaneras, autoridades
sanitarias jurisdiccionales, asociaciones profesionales, fuerzas policiales,
Ministerio Público, autoridades sanitarias extranjeras y toda otra autoridad
pública o asociación que así lo requiera en los temas relacionados con su
incumbencia.
22.- Confeccionar y
radicar, ante la detección de situaciones que pudieran configurar la comisión
de un delito penal, las correspondientes denuncias criminales por ante la
Comisión de Fiscales creada por la Resolución PGN Nº 54/97, ratificada por su
similar Nº 154/08, o cualquier otra autoridad que pudiere corresponder según el
caso de que se trate.
23.- Dar cumplimiento a
los compromisos asumidos en el marco del Convenio de Cooperación
Interinstitucional suscripto entre la ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS Y TECNOLOGIA MEDICA y la PROCURACION GENERAL DE LA NACION con fecha
18 de diciembre de 2008, protocolizado por Resolución PGN Nº 173/2008.
24.- Colaborar e impulsar
con las autoridades sanitarias, judiciales y fuerzas de seguridad que
correspondan, aquellas acciones que ameriten investigaciones complejas, tanto a
nivel nacional como provincial en los temas relacionados con su incumbencia.
25.- Participar
activamente en foros y grupos de trabajo que traten temáticas de competencia de
la Dirección, tanto a nivel nacional como internacional.
26.- Proponer los
aranceles y tasas retributivas correspondientes a los trámites y registros que
se efectúen como también por los servicios que se presten.
DIRECCION DE RECURSOS
HUMANOS Y ORGANIZACION
RESPONSABILIDAD PRIMARIA:
Administrar las políticas
y la aplicación de las normas que regulan al personal, su carrera
administrativa, su capacitación y desarrollo, las relaciones laborales y el
servicio de medicina del trabajo y de higiene y seguridad en el trabajo,
procurando mejorar los niveles de productividad y satisfacción laboral y la calidad
en las prestaciones de los servicios a cargo de la ADMINISTRACION NACIONAL.
Efectuar la planificación y diseño organizacional de la ADMINISTRACION NACIONAL
DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
ACCIONES:
1.- Administrar y
actualizar los sistemas de información relacionados con la aplicación de las
herramientas del sistema de planeamiento organizacional y de administración de
recursos humanos.
2.- Dirigir las acciones
de análisis, planeamiento y diseño organizacional. Elaborar y proponer las
modificaciones de las estructuras organizativas que correspondan en
consecuencia.
3.- Aplicar los controles
que permitan la correcta liquidación de haberes del personal.
4.- Ejercer la
coordinación técnica jurisdiccional y la actualización del sistema de
relevamiento y evaluación de los puestos de trabajo, como así también de los
procesos, flujos y procedimientos de trabajo, proponiendo las modificaciones y
simplificaciones pertinentes.
5.- Coordinar y asistir
técnicamente en el proceso de búsqueda, selección e integración del personal.
6.- Coordinar y asistir
técnicamente en el proceso de evaluación de desempeño del personal asistiendo a
las autoridades intervinientes y a los Comités de Evaluación en el cumplimiento
de sus responsabilidades y en la administración de los resultados del proceso.
7.- Planificar y
coordinar la capacitación del personal.
8.- Diseñar, proponer y
generar convenios con instituciones públicas y privadas.
9.- Monitorear el estado
de avance del personal en el régimen de carrera y proponer las políticas y
medidas pertinentes.
10.- Asegurar la adecuada
aplicación de la legislación en materia de recursos humanos, de la higiene y
seguridad laboral, y de la organización de las estructuras y procedimientos de
trabajo.
11.- Asistir técnicamente
a la Delegación Jurisdiccional de la Comisión Permanente de Interpretación de
la Carrera Profesional Sanitaria y de la Comisión Permanente de Interpretación
y Carrera.
12.- Coordinar y
supervisar el registro y actualización de la documentación de las personas que
integran la organización, asegurando un sistema de información permanente.
13.- Mantener relaciones
con los representantes gremiales, administrando los acuerdos resultantes de
convenios y negociaciones colectivas.
14.- Coordinar la
prestación del servicio médico de la Jurisdicción.
DEPARTAMENTO DE GESTION
DE CALIDAD
RESPONSABILIDAD PRIMARIA:
Intervenir en el diseño
del sistema de gestión de calidad institucional y coordinar la implementación y
monitoreo del mismo en vistas a mejorar el desempeño de la Administración.
ACCIONES:
1.- Intervenir en la
definición, diseño e implementación del sistema de gestión de calidad del
organismo.
2.- Analizar y monitorear
la implementación de la política de gestión de calidad en los procesos técnicos
y administrativos del organismo.
3.- Proponer la adopción
de instrumentos que incentiven la mejora de la calidad en la gestión de la
organización.
4.- Coordinar la
elaboración, actualización y resguardo de la documentación vinculada a la
gestión de la calidad.
5.- Coordinar la
certificación y/o acreditación nacional o internacional de los procesos
administrativos o técnicos que sean considerados necesarios para la
implementación de la política de calidad.
6.- Coordinar y
monitorear la implementación del sistema de gestión electrónica de trámites del
organismo.
7.- Intervenir en el
diseño y actualización del programa de despapelización del organismo.
8.- Proponer normativas
vinculadas al sistema de gestión electrónica de trámites del organismo.
COORDINACION GENERAL DE
INSPECTORADO
RESPONSABILIDAD PRIMARIA:
Coordinar las acciones de
las áreas de inspección de las Direcciones Nacionales de la ADMINISTRACION
NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA de acuerdo con los
lineamientos definidos por el titular, a fin de fortalecer las funciones de
fiscalización sanitaria desde una perspectiva integral y homogénea.
ACCIONES:
1.- Implementar un
sistema de calidad para todas las áreas de inspección como parte del Sistema de
Aseguramiento de Calidad de la ADMINISTRACION NACIONAL DE MEDICAMENTOS,
ALIMENTOS Y TECNOLOGIA MEDICA.
2.- Implementar y
coordinar la participación de las áreas de inspección en los programas de
acreditación de sistemas de calidad.
3.- Detectar problemas de
gestión y desvíos en la implementación de las políticas definidas por el
titular del organismo para las áreas de inspección, proponiendo las acciones
correctivas necesarias.
4.- Coordinar el análisis
funcional de los procesos orientados a la mejora continua del Sistema de
Calidad de las áreas de inspección.
5.- Articular la
adecuación de las estrategias a implementar por las áreas de inspección con los
objetivos institucionales.
6.- Promover la
generación y sistematización de información resultante de las inspecciones.
7.- Consolidar la
información técnica generada por las áreas de inspección en colaboración con la
Dirección de Gestión de Información Técnica.
8.- Desarrollar y
mantener actualizada una base de datos con la información resultante de las
inspecciones realizadas.
9.- Participar en
actividades de capacitación en procedimientos y técnicas de inspección, en
colaboración con la Dirección de Recursos Humanos y Organización.
10.- Promover y articular
el intercambio de información entre las áreas de inspección.
11.- Favorecer la
comunicación interna y externa de las actividades de las áreas de inspección,
en colaboración con la Dirección de Relaciones Institucionales y Regulación
Publicitaria.
12.- Colaborar con el
Departamento de Gestión de Calidad de la ADMINISTRACION NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA en la implementación de sistemas de
gestión de calidad.
DEPARTAMENTO DE SUMARIOS
ADMINISTRATIVOS
RESPONSABILIDAD PRIMARIA:
Realizar todas las
actividades vinculadas con la información y con la substanciación de los
sumarios administrativos disciplinarios que corresponda promover en órbita de
la ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA.
ACCIONES:
1.- Entender en la
investigación, instrucción, tramitación y resolución de los sumarios que se
originen en el Organismo.
2.- Formular las
denuncias ante los órganos competentes administrativos y judiciales que le
fueren requeridas por las autoridades respectivas, cuando fuere menester.
3.- Efectuar informes de
los recursos administrativos en materia disciplinaria que tramiten en la
Jurisdicción.
4.- Recopilar los
informes y la documentación necesaria para determinar la existencia de
perjuicio fiscal y la responsabilidad patrimonial emergente de los hechos
objeto de los sumarios de la Jurisdicción, proponiendo a los organismos
competentes el ejercicio de las acciones de recupero.
5.- Observar y supervisar
el cumplimiento de las diligencias dispuestas por el reglamento de
investigaciones y de toda otra que resulte necesaria a sus efectos.
6.- Llevar un registro
unificado del estado de trámite de la totalidad de los sumarios administrativos
del Organismo.