Disposición 1918-2013
Establécense los criterios para la selección de una especialidad medicinal como
producto de referencia para los estudios de Bioequivalencia y Equivalencia
In-Vitro.
Bs.
As., 11/4/2013
VISTO la Ley Nº 16.463, sus Decretos Reglamentarios Nros. 9763/64, 150/92 (T.O.
1993), las Disposiciones (ANMAT) Nros. 6677/10, 3185/99, sus complementarias y
modificatorias, 5040/06 (modificada por la Disposición ANMAT Nº 1746/07),
556/09 y 758/09 y el Expediente Nº 1-47-162-11-4 del registro de esta
Administración Nacional de Medicamentos, Alimentos y Tecnología Médica y;
CONSIDERANDO:
Que el artículo 1° de la Ley 16.463 establece que “quedan sometidos a la
presente ley y a los reglamentos que en su consecuencia se dicten, la
importación, exportación, producción, elaboración, fraccionamiento,
comercialización o depósito en jurisdicción nacional o con destino al comercio
interprovincial de las drogas, productos químicos, reactivas, formas
farmacéuticas, medicamentos, elementos de diagnóstico, y todo otro producto de
uso y aplicación en medicina humana y las personas de existencia visible o
ideal que intervengan en dichas actividades”.
Que el artículo 2° de la citada ley establece que las actividades mencionadas
sólo podrán realizarse previa autorización y bajo el contralor de la autoridad
sanitaria, en establecimientos por ella habilitados y bajo la dirección técnica
del profesional universitario correspondiente, todo ello en las condiciones y
dentro de las normas que establezca la reglamentación, atendiendo a las
características particulares de cada actividad y a razonables garantías
técnicas en salvaguarda de la salud pública y de la economía del consumidor.
Que asimismo el artículo 3° del mencionado cuerpo legal prescribe que los
productos comprendidos en la citada ley deberán reunir las condiciones
establecidas en la Farmacopea Argentina, y en caso de no figurar en ella, las
que surgen de los patrones internacionales y de los textos de reconocido valor científico,
debiendo a la vez ser inscriptos por ante esta Administración Nacional de
conformidad a lo establecido en el Decreto Nº 150/92 (T.O. 1993).
Que el artículo 1° del Decreto Nº 9763/64, reglamentario de la Ley 16.463,
establece que el ejercicio del poder de policía sanitaria referido a las
actividades indicadas en el artículo 1° de la mentada ley, y a las personas de
existencia visible o ideal que intervengan en las mismas, se hará efectivo por
el Ministerio de Asistencia Social y Salud Pública de la Nación (hoy Ministerio
de Salud), en las jurisdicciones que allí se indican.
Que por su parte el Decreto Nº 1490/92, crea esta Administración Nacional de
Medicamentos, Alimentos y Tecnología Médica (ANMAT), como organismo
descentralizado de la Administración Pública Nacional, con un régimen de
autarquía financiera y económica, con jurisdicción en todo el territorio
nacional, asumiendo dichas funciones.
Que en virtud del artículo 3°, inciso a) del mencionado decreto, esta
Administración Nacional tiene competencia, entre otras materias, en todo lo
referente al control y fiscalización sobre la sanidad y la calidad de las
drogas, productos químicos, reactivos, formas farmacéuticas, medicamentos,
elementos de diagnóstico, materiales y tecnologías biomédicas y todo otro
producto de uso y aplicación en medicina humana.
Que esta Administración Nacional es la autoridad reguladora de medicamentos, y
está facultada para otorgar su registro sanitario, de acuerdo a los requisitos
y procedimientos establecidos en cada caso.
Que el Decreto Nº 150/92 (T.O. 1993), reglamentario de la Ley de Medicamentos
Nº 16.463, estableció una serie de definiciones, normas y procedimientos, que
constituyen la base sobre la cual se sustenta todo lo relacionado con el
registro, elaboración, fraccionamiento, expendio, comercialización, exportación
e importación de medicamentos y especialidades medicinales.
Que de conformidad a las prescripciones de dicho decreto se entiende por
medicamento a “toda preparación o producto farmacéutico empleado para la
prevención, diagnóstico y/o tratamiento de una enfermedad o estado patológico,
o para modificar sistemas fisiológicos en beneficio de la persona a quien se le
administra” (art. 1° inciso a).
Que por su parte el inciso b) del citado artículo define principio activo o
droga farmacéutica como “toda sustancia o mezcla de sustancias relacionadas, de
origen natural o sintético que poseyendo un efecto farmacológico específico, se
emplea en medicina humana”.
Que asimismo el inciso c) define nombre genérico como “denominación de un
principio activo o droga farmacéutica, o cuando corresponda, de una asociación
o combinación de principios activos a dosis fijas, adoptada por la autoridad
sanitaria nacional, o, en su defecto, la denominación común internacional de un
principio activo recomendada por la Organización Mundial de la Salud”.
Que finalmente el inciso d) define especialidad medicinal como “todo
medicamento designado por su nombre convencional, sea o no una marca de fábrica
o comercial, o por el nombre genérico que corresponda a su composición y
contenido, preparado y envasado uniformemente para su distribución y expendio,
de composición cuantitativa definida, declarada y verificable, de forma
farmacéutica estable y acción terapéutica comprobable”.
Que la aplicación de las normativas aludidas, y las mencionadas en el Visto de
la presente disposición, tienen como finalidad última la protección de la salud
de la población, mediante la adopción de un modelo fiscalizador de gestión, que
sin perjuicio de la lectura objetiva de información calificada, destine los
mayores esfuerzos a garantizar la eficacia, seguridad y calidad de los
productos que aquélla consume.
Que mediante procesos de investigación y desarrollo se obtienen productos que
se denominan originales o innovadores, incluyendo entre sus etapas la síntesis
química, investigaciones preclínica, galénica y clínica, siendo esta última la
que permite inferir su farmacocinética, biodisponibilidad, farmacodinámica,
seguridad y eficacia terapéutica.
Que existen medicamentos que poseen los mismos ingredientes farmacéuticos
activos (IFAs) que el medicamento innovador, pudiendo diferir en la composición
de sus excipientes, y que cumplen con las Buenas Prácticas de Manufactura,
almacenamiento y distribución, definiéndose a éstos como productos multifuente
(OMS, Informe Técnico Nº 937, Anexo 7, del año 2006).
Que el fundamento científico de los estudios de bioequivalencia o de
equivalencia in Vitro es la comparabilidad de sus biodisponiblidades o de sus
perfiles de disolución, respectivamente, entre el producto multifuente y el
producto de referencia.
Que por Disposición (ANMAT) Nº 3185/99, en su ANEXO I, punto II,
“Definiciones”, se define al producto de referencia como aquel producto para el
cual la eficacia y seguridad han sido establecidas.
Que por Disposiciones (ANMAT) Nros. 3185/99, 5040/06, y su modificatoria
1746/07 y 758/09 se han establecido los requerimientos técnicos y metodológicos
para la realización de estudios de Bioequivalencia in-vivo y/o Equivalencia in
Vitro entre una formulación multifuente y otra que esta ANMAT fija como de
referencia.
Que a los fines de asegurar la continuidad de la calidad y del comportamiento
de los productos designados por este organismo de control, como referencia para
estudios de bioequivalencia, resulta necesario documentar sus características.
Que a fojas 1/3 obra el informe técnico de la Comisión Asesora “Ad Honorem” en
temas de Bioequivalencia y Biodisponibilidad, creada por Disposición ANMAT Nº
4351/10.
Que la aludida Comisión Asesora, el Instituto Nacional de Medicamentos y la
Dirección de Asuntos Jurídicos, han tomado la intervención de su competencia.
Que se actúa en virtud de las facultades conferidas por los Decretos Nros.
1490/92 y 425/10.
Por ello;
EL INTERVENTOR DE LA ADMINISTRACION NACIONAL DE MEDICAMENTOS, ALIMENTOS Y
TECNOLOGIA MEDICA
DISPONE:
Artículo 1° — Establécense los criterios para la selección de una
especialidad medicinal como producto de referencia para los estudios de
Bioequivalencia y Equivalencia In-Vitro que figuran en el Anexo I de la
presente disposición, que forma parte integrante de la misma.
Art. 2° — Establécese que para la designación de una especialidad
medicinal como producto de referencia para los estudios de Bioequivalencia y
Equivalencia In-Vitro, ya sea solicitada por su titular o cuando así lo estime
necesario esta Administración Nacional, deberá presentarse la documentación que
obra en el Anexo II de la presente disposición, que forma parte integrante de
la misma.
Art. 3° — Una vez aprobada la documentación mencionada en el artículo
inmediato precedente, esta ANMAT designará el Producto de Referencia para
estudios de Bioequivalencia y Equivalencia In-Vitro, que deban cumplimentar
todas las formas farmacéuticas y las concentraciones de todos los productos
similares / multifuentes comercializados a la fecha, incluyendo los
establecidos en la Disp. ANMAT Nº 4788/12.
Art. 4° — Déjanse sin efecto los criterios de selección del producto de
referencia establecidos en la Disposición (ANMAT) Nº 758/09, Anexo I, Punto IV.
Art. 5° — Apruébase el formulario índice para la presentación de la
documentación necesaria para que una especialidad medicinal sea designada como
producto de referencia (según lo establecido en el Anexo II), que obra en el
Anexo III de la presente disposición y que forma parte integrante de la misma.
Art. 6° — Apruébase el formulario de caracterización del producto, que
figura como Anexo IV de la presente disposición y que forma parte integrante de
la misma.
Art. 7° — La presente Disposición entrará en vigencia a partir del
primer día hábil siguiente al de su publicación en el Boletín Oficial.
Art. 8° — Regístrese. Dése a la Dirección Nacional del Registro Oficial
para su publicación. Notifíquese a las Cámaras de Especialidades Medicinales
(CILFA, CAEME, COOPERALA, CAPGEN, CAPEMVeL, SAFYBI), Confederación Médica de la
República Argentina (COMRA) y la Confederación Farmacéutica Argentina (COFA).
Cumplido archívese PERMANENTE. — Carlos Chiale.
ANEXO I
CRITERIOS DE SELECCION PARA LA DESIGNACION DE UNA ESPECIALIDAD
MEDICINAL COMO PRODUCTO DE REFERENCIA PARA ESTUDIOS DE BIOEQUIVALENCIA Y
EQUIVALENCIA IN-VITRO
Esta ANMAT seleccionará, según los criterios del presente ANEXO, para cada
ingrediente farmacéutico activo, forma farmacéutica y concentración, al
candidato a Producto de Referencia y notificará al laboratorio titular del
Registro, el cual deberá presentar la documentación del Anexo II cuya
aceptación determinará su designación como Producto de Referencia para estudios
de Bioequivalencia y Equivalencia In-Vitro.
Se exceptúan de este procedimiento los productos comparadores del Item 2 del
presente Anexo para los cuales esta ANMAT implementará las acciones necesarias
para facilitar la disponibilidad del producto de Referencia.
Los criterios para la selección del Producto de Referencia son:
1° Producto Innovador consumido y comercializado en el país; o
2° Producto no consumido ni comercializado en el país, que:
2.1. Se encuentra incluido como producto comparador para estudios de
bioequivalencia en el Informe Técnico de la OMS, Nº 902, del año 2002 y
posteriores; o
2.2. Producto Innovador consumido y proveniente de un país ICH (International
Conference on Harmonisation) o país asociado; o
3° Producto designado por esta ANMAT de acuerdo a su perfil de seguridad,
eficacia y/o estudio/s de su comportamiento farmacocinético y toda otra
Información que esta autoridad sanitaria estime correspondiente, ejemplo:
antecedentes de farrnacovigilancla registrados a lo largo de su
comercialización.
A continuación se presenta el algoritmo decisorio para establecer el producto
de referencia.
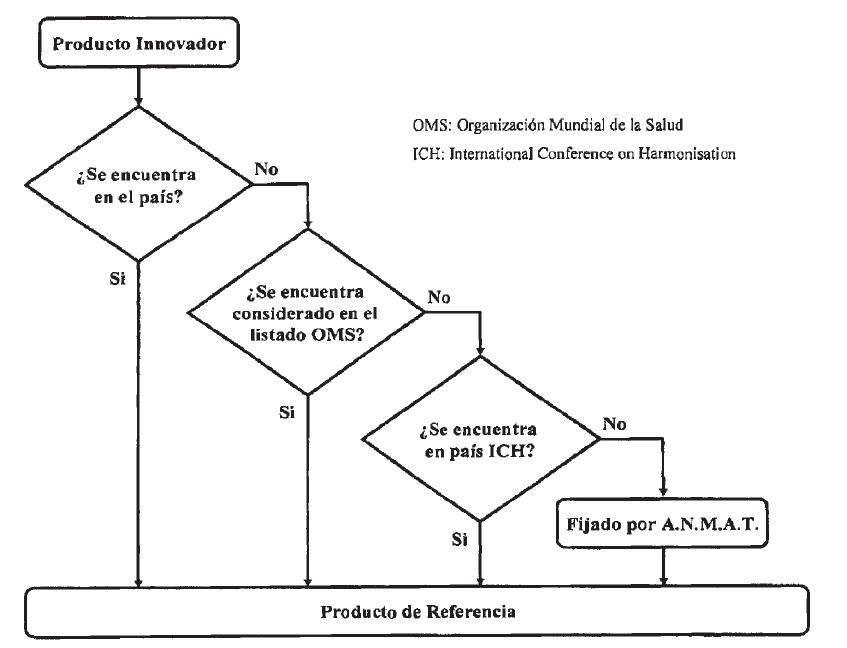
Arbol
(algoritmo) de decisión para la designación de una especialidad medicinal como
producto de referencia para estudios de bioequivalencia y/o equivalencia
in-vitro.
ANEXO II
DOCUMENTACION QUE DEBE PRESENTAR EL LABORATORIO TITULAR DE UNA
ESPECIALIDAD MEDICINAL PARA COMPLETAR EL FORMULARIO INDICE (ANEXO III) PARA SU
EVALUACION COMO PRODUCTO DE REFERENCIA
1. Denominación Común Argentina (DCA) o de corresponder Denominación Común
Internacional (DCI) del ingrediente farmacéutico activo: incluir dicha
denominación y la del principal metabolito activo cuando corresponda.
2. Certificado: copia del certificado de inscripción en el REM, incluidos
cambios posteriores al registro.
3. Origen de la elaboración de cada etapa desde el IFA hasta el producto
terminado: estableciendo claramente el país, empresa productora y dirección de
la misma.
4. Evidencia de consumo en Argentina.
5. Formas farmacéuticas y concentraciones aprobadas.
6. Caracterización de fórmula: conforme al formulario que figura en el Anexo IV
del presente.
7. Registro maestro de elaboración.
8. Características físicas del ingrediente farmacéutico activo:
8.1. forma cristalina.
8.2. solubilidad.
8.3. tamaño de partícula.
9. Trazabilidad en las condiciones de elaboración del producto actualmente
comercializado, respecto al biolote.
10. Metodología del Test de disolución: coincidente con la aprobada y
presentación de los resultados.
11. Perfiles de disolución de dos o más lotes, en tres medios: según lo
establecido en la Disposición (ANMAT) Nº 758/09 con cálculo del factor de
similaridad interlote.
12. Resultados del/los estudio/s de Biodisponibilidad/Bioequivalencia:
correspondiente a la formulación seleccionada para consumir en Argentina,
especificando el lote, con respecto al producto innovador que haya demostrado
seguridad y eficacia inicialmente con el fin de demostrar que el producto a ser
designado de referencia en el país está correlacionado de manera confiable con
los datos clínicos originales, incluyendo:
12.1. presentación de los resultados según Disposición (ANMAT) Nº 5040/06 y su
modificatoria 1746/09, ítem 4.9, Anexo I y Anexo IV.
12.2. cuando corresponda:
12.2.1. estudios realizados en ayunas y/o con alimentos.
12.2.2. principal metabolito activo.
12.2.3. estudios puente entre fase II - III y la formulación comercializada.
12.2.4. estudios para cada forma farmacéutica y concentración que lo requiera.
13. Productos asociados (o combinados). Incluir el perfil farmacocinético de
los fármacos:
13.1. En forma individual.
13.2. De la asociación.
14. Declaración de aceptación de que no será confidencial la información
suministrada en el ítem 6.
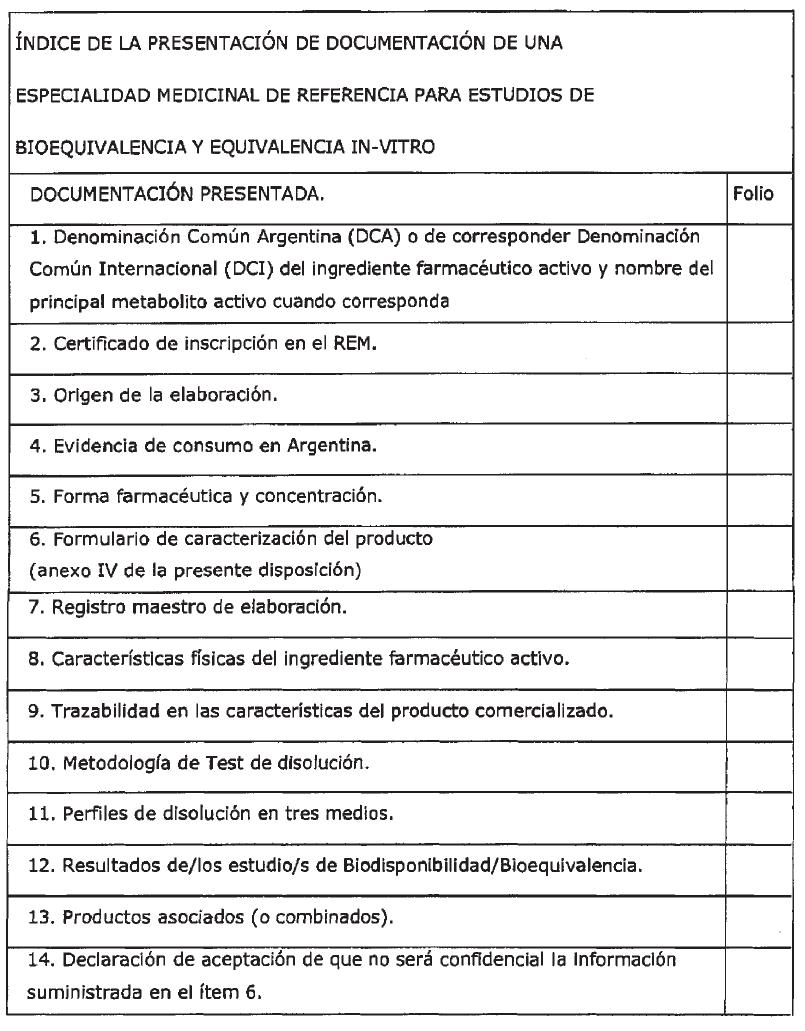
ANEXO III
FORMULARIO INDICE DE LA PRESENTACION DE DOCUMENTACION POR EL
LABORATORIO TITULAR DE UNA ESPECIALIDAD MEDICINAL PARA SU EVALUACION /
DESIGNACION COMO PRODUCTO DE REFERENCIA PARA ESTUDIOS DE BIOEQUIVALENCIA Y/O
EQUIVALENCIA IN-VITRO
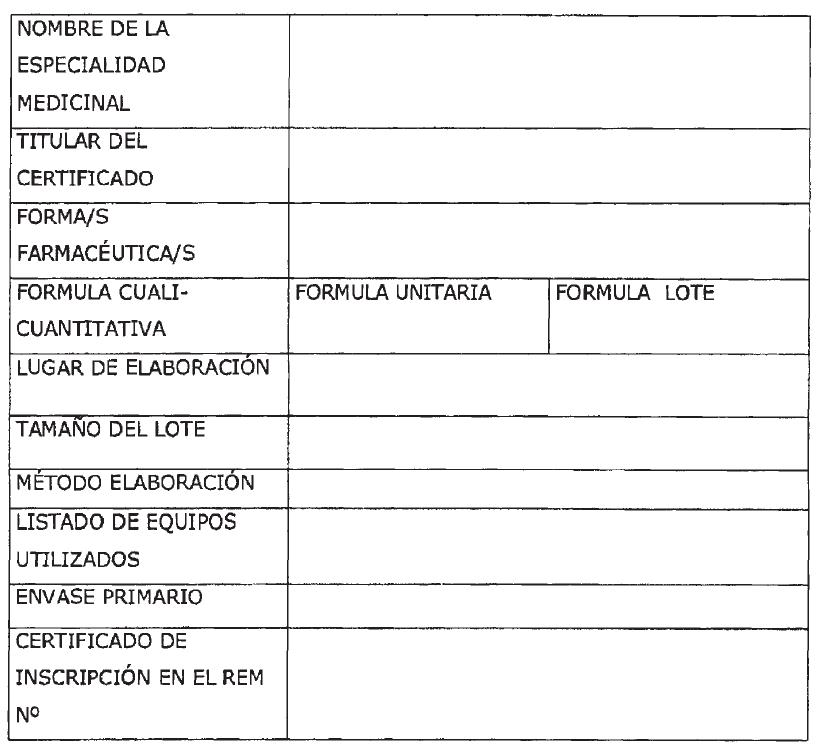
ANEXO IV
FORMULARIO DE
CARACTERIZACION DEL PRODUCTO