Resolución 598-2012-SENASA
Elaboración, importación, exportación,
tenencia, distribución y expendio de las vacunas virales no vesiculares para
bovinos
Bs.
As., 4/12/2012
VISTO el Expediente Nº S01:0080568/2011 del Registro del MINISTERIO DE
AGRICULTURA, GANADERIA Y PESCA, y
CONSIDERANDO:
Que es imperiosa la necesidad de establecer reglamentación que permita la
regulación de la elaboración, importación, exportación, tenencia, distribución
y expendio de las vacunas virales inactivadas no vesiculares para bovinos de
uso veterinario.
Que la vacunación es un instrumento básico en la prevención de las enfermedades
virales de los bovinos.
Que la administración de vacunas puras, seguras y eficaces es imprescindible
para el mantenimiento de la salud animal y el funcionamiento satisfactorio de
los programas de producción bovina.
Que se debe actualizar la legislación, atendiendo los avances científicos y
técnicos acumulados.
Que se debe dar a los productores pecuarios seguridad en cuanto a los productos
biológicos a aplicar.
Que a fojas 319 y 312, respectivamente, la Dirección de Aprobación de Productos
Alimenticios y Farmacológicos y la Dirección de Laboratorios informan que están
en condiciones de cumplimentar las distintas etapas de control que se
establecen.
Que a fojas 11/12 la Dirección de Laboratorio Animal de la Dirección General de Laboratorios y Control Técnica expone que se han tenido en cuenta las
sugerencias del Consejo Asesor de Virología del SERVICIO NACIONAL DE SANIDAD Y
CALIDAD AGROALIMENTARIA y de las empresas involucradas en la elaboración y
comercialización de vacunas.
Que a fojas 11/12 la Dirección de Laboratorio Animal de la Dirección General de Laboratorios y Control Técnica expone que para introducir las
modificaciones normativas que se pretenden se han tenido en cuenta las
recomendaciones efectuadas por la ORGANIZACION MUNDIAL DE SANIDAD ANIMAL (Oficina internacional de epizootias; OIE) en el Manual de las Pruebas de Diagnóstico y de las Vacunas para los Animales Terrestres
(Capítulo 1.1.7).
Que el SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA realizó un
proceso de consulta pública.
Que la Dirección de Asuntos Jurídicos del SERVICIO NACIONAL DE SANIDAD Y
CALIDAD AGROALIMENTARIA, ha emitido el correspondiente dictamen jurídico.
Que el suscripto es competente para dictar la presente resolución en función de
la Ley Nº 13.636, el Decreto Reglamentario Nº 583 del 31 de enero de 1967,
modificado por el Decreto Nº 3.899 del 2 de junio de 1972 y sus modificatorias;
y de lo normado por los incisos f) y l) del Artículo 8° del Decreto Nº 1.585
del 19 de diciembre de 1996, sustituido por su similar Nº 825 del 10 de junio
de 2010.
Por ello,
EL PRESIDENTE DEL SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA
RESUELVE:
ARTICULO 1° — Objeto. La elaboración, importación, exportación, tenencia,
distribución y expendio de las vacunas virales no vesiculares para bovinos será
autorizada por el SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA
(SENASA), a través de la Dirección Nacional de Agroquímicos, Productos
Veterinarios y Alimentos (DNAPV y A) y de la Dirección General de Laboratorios y Control Técnico (DGL y CT), de conformidad con la Ley Nº 13.636, el Decreto Reglamentario Nº 583 del 31 de enero de 1967, modificado por el
Decreto Nº 3.899 del 2 de junio de 1972 y sus modificatorias; y de lo normado
por los incisos f) y l) del Artículo 8° del Decreto Nº 1.585 del 19 de
diciembre de 1996, sustituido por su similar Nº 825 del 10 de junio de 2010 y
con lo dispuesto en la presente resolución.
ARTICULO 2° — Antígenos virales. Se incluyen como vacunas virales no
vesiculares para bovinos aquellos inmunógenos que contengan algunos de los
siguientes antígenos virales:
Inciso a) Agente causal de la Rinotraqueitis Infecciosa Bovina (IBR) Herpes virus bovino tipo I (BoHV-1).
Inciso b) La variante neurológica Herpes virus bovino tipo V (BoHV-5).
Inciso c) Virus de la Diarrea Viral Bovina (VDVB).
Inciso d) Rotavirus bovino (RVB).
Inciso e) Virus Parainfluenza Bovina tipo 3 (PI3).
Inciso f) Virus respiratorio sincicial bovino (VRSB).
Inciso g) Coronavirus bovino (CoVB).
ARTICULO 3° — Categorización. A los efectos de la fabricación, importación,
tenencia, distribución y expendio de vacunas, de acuerdo a lo establecido en la Ley Nº 13.636, el Decreto Reglamentario Nº 583 del 31 de enero de 1967, modificado por el
Decreto Nº 3.899 del 2 de junio de 1972 y sus modificatorias; y en la Resolución Nº 345 del 6 de abril de 1994 del ex-SERVICIO NACIONAL DE SANIDAD ANIMAL, las
personas físicas o jurídicas serán categorizadas, según corresponda, de la
siguiente manera:
Inciso a) Firmas productoras de vacunas con establecimiento en el país o en el
exterior, con registro, elaboración de antígenos y formulación propios.
Inciso b) Firmas productoras de vacunas que formulen con antígenos elaborados
por terceros y con registro propio.
Inciso c) Firmas que no poseen establecimientos de elaboración y que acrediten
fehacientemente, además del derecho de comercialización, que el producto se
elabora en establecimientos habilitados, estando todo el proceso bajo la
responsabilidad directa del titular del registro.
Inciso d) Firmas que detenten extensiones de certificados de productos
elaborados por firmas incluidas en el inciso “a” del presente artículo.
ARTICULO 4° — Auditorías e Inspecciones. En todas las categorías citadas en el
Artículo 3° de la presente resolución, la totalidad de las auditorías e
inspecciones que se establecen en esta norma, serán realizadas en las
instalaciones del laboratorio elaborador.
ARTICULO 5° — Exigencias. Las firmas incluidas en las categorías establecidas
en los incisos a, b, c y d del Artículo 3° de la presente resolución, están
sujetas a las exigencias que se reglamentan en el presente artículo:
Inciso a) A la habilitación del establecimiento elaborador y depósitos.
Inciso b) A auditorías e inspecciones del proceso de producción.
Inciso c) A las pruebas de registro o autorización del producto.
Inciso d) Al control de series, previa a la venta y uso de las vacunas.
Inciso e) Al pago de aranceles por las vacunas presentadas a registro, control
de series y auditorías.
ARTICULO 6° — Responsabilidad. Los titulares o responsables jurídicos de los
establecimientos de las categorías citadas por el Artículo 3° de la presente
resolución, serán responsables de la inocuidad, pureza, calidad y legitimidad
de los productos elaborados, fraccionados, depositados y distribuidos.
ARTICULO 7° — Producción. En todos los casos la producción se realizará en
establecimientos autorizados y habilitados por el SERVICIO NACIONAL DE SANIDAD
Y CALIDAD AGROALIMENTARIA.
ARTICULO 8° — DE LA HABILITACION Y REGISTRO DE LOS LABORATORIOS. Inscripción y
Habilitación. La inscripción y habilitación de los laboratorios que elaboran
antígenos y vacunas destinados a prevenir las enfermedades virales no
vesiculares de los bovinos, debe ser gestionada ante el SENASA llenando con
carácter de Declaración Jurada, una solicitud, que además de adecuarse a los
alcances de las Resoluciones Nros. 345 del 6 de abril de 1994 y 765 del 3 de
diciembre de 1996, ambas del ex-SERVICIO NACIONAL DE SANIDAD ANIMAL hace
constar lo siguiente:
Inciso a) Nombre de la firma comercial.
Inciso b) Nombre del Director y/o Responsable Técnico con Título de Profesional
de las Ciencias Veterinarias.
Inciso c) Organigrama donde consten como mínimo los profesionales responsables
de Producción, Control de Producción, Aseguramiento de Calidad.
Inciso d) Ubicación del laboratorio, domicilio y teléfono.
Inciso e) Habilitación municipal.
Inciso f) Planos de los locales y memoria descriptiva de las instalaciones y
equipos destinados a la producción, cuarentena, control de calidad, bioterio,
envase, conservación, depósito y expendio de conformidad al tipo de producto
elaborado.
Inciso g) Capacidad de elaboración y depósito mensual y anual de los productos
terminados.
Inciso h) Si posee campo experimental, deberá presentar ubicación y planos de
las instalaciones, detallando pruebas y actividades que se desarrollarán en el
mismo.
ARTICULO 9° — DE LA HABILITACION Y REGISTRO DE LOS LABORATORIOS. Revocación o
suspensión de la habilitación. La habilitación de los laboratorios, así como
las autorizaciones de elaboración, importación, y venta de vacunas que se
otorguen al amparo de la presente resolución, pueden ser revocadas o
suspendidas, sin derecho a indemnización alguna, si se demuestra con hechos
fundados y protocolizados el incumplimiento a las disposiciones contenidas en
la presente norma.
ARTICULO 10. — INSPECCION Y RETIRO DE MUESTRAS. Los depósitos para vacunas
terminadas deberán cumplir con los siguientes requisitos:
Inciso a) Las cámaras frías utilizadas para conservar vacunas, productos
biológicos y fármaco-veterinarios que requieran cadena de frío, debidamente
segregados, deben ser independientes de las utilizadas para depositar otro tipo
de productos.
Inciso b) Se prohíbe el uso compartido de las cámaras frías utilizadas para
conservar vacunas y fármaco-veterinarios, ambos en su producto final envasado,
con vacunas y fármacos de uso humano, productos alimenticios, materias primas y
productos semielaborados.
Inciso c) Debe contar con la habilitación municipal correspondiente.
Inciso d) El predio donde se encuentre el depósito, debe contar con medidas de
seguridad y con registros de ingreso y egreso de vehículos y de personas.
Inciso e) Los inspectores del SENASA tendrán acceso a las instalaciones del
predio donde se encuentre el depósito sin restricciones de ningún tipo.
Inciso f) Es obligatoria la designación de un Responsable Técnico, el cual debe
ser profesional de las Ciencias Veterinarias, quien será responsable de las
vacunas depositadas.
Inciso g) Las cámaras frías deberán mantener una temperatura entre DOS GRADOS
CENTIGRADOS (2°C) y OCHO GRADOS CENTIGRADOS (8°C), con registro continuo de la misma. Deben estar conectadas a un grupo electrógeno para
emergencias con tablero de transferencia automática.
Inciso h) Los frascos de vacunas deben estar etiquetados e inequívocamente
identificados.
Inciso i) Las vacunas que requieren otra temperatura de conservación, cumplirán
con las indicaciones de conservación del fabricante.
Inciso j) Las vacunas deben estar depositadas en contenedores o canastos que
permitan conseguir una temperatura uniforme sobre todos los frascos de vacunas.
Inciso k) En los canastos con las vacunas de uso local deberá constar:
I- Nombre del producto.
II- Número de serie.
III- Fecha de vencimiento.
IV- Numeración del estampillado oficial.
V- Los canastos deberán estar ordenados de forma correlativa a fin de permitir
a los inspectores del SENASA contar los frascos que componen cada serie y
seleccionar los frascos sorteados.
Inciso l) El predio donde se encuentre el depósito, debe contar con áreas
segregadas para vacunas en control oficial y vacunas aprobadas. De ambas áreas
debe llevarse un registro donde conste nombre del producto, número de
certificado, serie, numeración de las estampillas y fecha de vencimiento.
Inciso m) El predio donde se encuentre el depósito debe contar con un espacio
independiente, cerrado con llave y con restricciones de acceso donde se
depositarán las contramuestras oficiales.
Inciso n) El predio donde se encuentre el depósito, debe contar con una oficina
para los inspectores del SENASA con los elementos necesarios para controlar la
documentación, preparar los paquetes con las muestras y completar las actas
correspondientes.
Inciso o) La presentación para los retiros de series deberá hacerse de acuerdo
a las fechas estipuladas en el calendario anual de Control de Vacunas Virales
No Vesiculares.
Inciso p) Una vez presentada la Solicitud de Retiro de Muestras en la
Coordinación de Biológicos de la Dirección del Laboratorio Animal por parte del
laboratorio elaborador, se inicia el control de la serie de vacunas de acuerdo
al Manual de Procedimientos de la Dirección General de Laboratorios y Control Técnico (DGLyCT).
Inciso q) En la cámara refrigerada del laboratorio elaborador se realiza el
conteo total de dosis presentadas.
Inciso r) En el laboratorio elaborador, sobre las dosis presentadas, se realiza
un sorteo al azar basándose en la numeración de las estampillas de los frascos.
Inciso s) Se toma como retiro para la Coordinación de Virología, Departamento
de Control de Vacunas, un mínimo de CUATROCIENTAS (400) dosis de vacuna oleosa
u acuosa, para cada uno de los TRES (3) paquetes que serán armados [haciendo un
total de UN MIL DOSCIENTAS (1200) dosis como mínimo].
Inciso t) Una vez separados los frascos estampillados de acuerdo al sorteo, se
procede a distribuirlos en TRES (3) paquetes que luego se firman, quedando UN
(1) paquete como contramuestra en el laboratorio elaborador (Paquete Nº 3).
Inciso u) Se completa el Acta de Retiro de Muestras con la cantidad de dosis,
el número de estampillas de los frascos seleccionados por sorteo, firmando los
responsables por el laboratorio productor y por el SENASA.
Inciso v) Si hubiera devolución de estampillas se adjunta al trámite el
detalle.
Inciso w) Las actas se realizan por duplicado quedando una copia en el
laboratorio elaborador.
Inciso x) Las muestras deben trasladarse refrigeradas entre los CUATRO GRADOS
CENTIGRADOS (4°C) y los OCHO GRADOS CENTIGRADOS (8°C).
Inciso y) Las muestras (Paquetes Nros. 1 y 2) y el trámite interno con su
respectiva Acta de Retiro, deberán ingresar en la DGLyCT, la que otorgará un
número de trámite interno y será su personal el responsable de abrir el Paquete
Nº 1, verificar la temperatura y distribuir la muestra a las Coordinaciones de
Bacteriología y de Virología. El restante del Paquete Nº 1 (abierto) y el
Paquete Nº 2 (cerrado) firmados serán entregados a la Coordinación de Virología
a fin de ser conservados entre los CUATRO GRADOS CENTIGRADOS (4°C) y los OCHO GRADOS CENTIGRADOS (8°C).
Inciso z) El Paquete Nº 1 se utilizará para todas las pruebas. El Paquete Nº 2
se mantiene cerrado como contramuestra hasta su vencimiento.
ARTICULO 11. — Habilitación. Registro del Laboratorio. Efectuadas las
inspecciones y verificado el cumplimiento de los requisitos establecidos, el
SENASA concede la habilitación, expidiendo oportunamente el Certificado de
habilitación respectivo y procediendo a registrar al laboratorio en el Registro
Nacional correspondiente, previo informe favorable de la Dirección Nacional de Agroquímicos, Productos Veterinarios y Alimentos (DNAPVyA) y de la Dirección General de Laboratorios y Control Técnico (DGLyCT).
ARTICULO 12. — NORMAS GENERALES. Solicitud de Registro de Productos Biológicos.
Las Firmas debidamente inscriptas según lo establecido en los artículos
precedentes, deben presentar para la aprobación de sus vacunas, una Solicitud
de Registro de Productos Biológicos, que debe adecuarse a la normativa vigente
para el registro y aprobación de productos destinados al diagnóstico,
prevención o tratamiento de las enfermedades de los animales. Asimismo, deberán
responder a los informes técnicos emitidos por la DGLyCT.
ARTICULO 13. — Controles de la DGLyCT. La DGLyCT tiene acceso a todas las etapas del proceso de elaboración de las vacunas y tiene la potestad de efectuar
auditorías o inspecciones periódicas con el fin de controlar la producción, el
buen estado de los locales, instalaciones y equipos de los laboratorios elaboradores.
ARTICULO 14. — Retiro de Muestras. Se autoriza al personal de la DGLyCT, para
retirar muestras de los distintos componentes que integran las vacunas en las
etapas de elaboración, a fin de someterlos a los controles correspondientes y
al retiro de muestras del producto semielaborado y terminado.
ARTICULO 15. — Estampilla Oficial. No puede presentarse a control ni expenderse
en el mercado local ningún envase de vacuna sin su correspondiente estampilla
oficial numerada correlativamente. La estampilla debe certificar la serie que
corresponda, así como su fecha de vencimiento y la cantidad de dosis que
contiene.
ARTICULO 16. — Exigencias. Control Oficial. Las vacunas destinadas a prevenir
las enfermedades virales no vesiculares de los bovinos ya sean monovalentes o
polivalentes, virales exclusivamente, o combinadas con antígenos bacterianos,
deben cumplir las exigencias para el registro que se encuentran incluidas en
esta reglamentación, las series sucesivas al registro serán muestreadas y se
aprobarán con el análisis por parte de la DGLyCT de inocuidad, esterilidad,
físico-químico y potencia. El control oficial se realizará luego de recibidos
los controles internos con resultado satisfactorio.
ARTICULO 17. — DE LOS PRODUCTOS A IMPORTAR. Autorización. Sólo se autoriza la
importación de antígenos o vacunas en cuyo proceso de producción se utilicen
materias primas de origen animal, que resulten autorizadas por la Resolución Nº 117 del 22 de enero de 2002 del SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA,
la que establece la evaluación de la situación de riesgo de Encefalopatía
Espongiforme Bovina (EEB) para cada país exportador, y su modificatoria
Resolución SENASA Nº 1052 del 30 de diciembre de 2002.
ARTICULO 18. — Materias Primas. Las materias primas importadas para ser
utilizadas en vacunas producidas localmente, deben estar autorizadas por la citada Resolución Nº 117/02, la que establece la evaluación de la situación de riesgo de
Encefalopatía Espongiforme Bovina (EEB) para cada país exportador, y su
modificatoria Nº 1052/02.
ARTICULO 19. — Exigencias y condiciones. Las firmas interesadas en la
importación de vacunas o antígenos deben cumplimentar la totalidad de las
exigencias y condiciones que se establecen en la presente resolución. Asimismo,
deben poseer en el país instalaciones habilitadas para la formulación,
conservación, depósito y expendio, según el caso, de estos productos, acorde a
lo establecido en la presente reglamentación.
ARTICULO 20. — Aprobación del Registro de Firmas para Importar. La aprobación
pertinente se debe gestionar ante el SENASA. La misma se va a conceder, si
correspondiere, previa inspección y habilitación del establecimiento elaborador
y depósitos por la DGLyCT.
ARTICULO 21. — Previo al Registro de la Firma. Previo al inicio de los trámites de registro, los interesados deben presentar lo
siguiente:
I- La habilitación del laboratorio por parte del Ente Sanitario Oficial del
país de origen para la elaboración de vacunas.
II- El registro del producto en su país de origen.
III- Acreditación en Buenas Prácticas de Manufactura.
ARTICULO 22. — Auditorías y Controles. Las vacunas o antígenos importados serán
sometidos a la totalidad de las auditorías y controles establecidos en la
presente reglamentación, al igual que los aplicados a las vacunas elaboradas en
el país.
ARTICULO 23. — DE LA ADMISION Y REGISTRO DE LAS VACUNAS. Control de
autorización o registro. Todas las vacunas cuyos certificados de uso y
comercialización se soliciten, serán sometidas por la DGLyCT a los controles
que determina esta reglamentación bajo la denominación de “Control de
autorización o registro”.
ARTICULO 24. — Registro de Laboratorios. Las firmas deben registrar sus
laboratorios habilitados en el Registro Nacional respectivo, que a tal efecto
lleva la Dirección Nacional de Agroquímicos, Productos Veterinarios y Alimentos
(DNAPVyA) de este Servicio Nacional.
ARTICULO 25. — Solicitud de Inscripción de Vacunas. Se debe gestionar ante el
Registro Nacional enunciado en el Artículo 24 de la presente resolución, la
solicitud de inscripción de las vacunas que deseen elaborar, adecuando el
contenido de cada una de las presentaciones a lo establecido en la normativa
vigente.
ARTICULO 26. — Exclusividad. Se aceptarán únicamente vacunas virales no vesiculares
para bovinos inactivadas.
ARTICULO 27. — Presentación de antecedentes de la Prueba del Producto. Previo a
la presentación de la primera serie de registro a control, las firmas deben
presentar los antecedentes del producto probado en la especie de destino o en
especies de laboratorio con concordancia aceptada que demuestre lo siguiente:
Inciso a) La potencia del producto.
Inciso b) La eficacia del producto.
Inciso c) La duración de inmunidad del producto.
Inciso d) La estabilidad del producto.
Estos deberán ir acompañados de:
Inciso e) Sus resultados de inocuidad o control de inactivación.
Inciso f) Sus resultados de seguridad.
Inciso g) Sus resultados de esterilidad.
Inciso h) Antecedentes del desarrollo.
Inciso i) Antecedentes científicos.
Inciso j) Antecedentes bibliográficos.
ARTICULO 28. — Presentación de rótulos y folletos. Previo a la presentación de
la primera serie de registro a control, las firmas deben acompañar los
proyectos de rótulos y folletos a utilizar de acuerdo a las Resoluciones Nros.
345 del 6 de abril de 1994 y 765 del 3 de diciembre de 1996, ambas del
ex-SERVICIO NACIONAL DE SANIDAD ANIMAL, y 897 del 23 de diciembre de 2002 del
SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA.
ARTICULO 29. — Pruebas de Registro de Vacunas. Se consideran pruebas de
registro de vacunas aquellas a las que se somete a dichos inmunógenos con el
fin que las personas físicas o jurídicas recurrentes puedan obtener el
Certificado de Uso y Comercialización pertinente.
ARTICULO 30. — Aceptación de la serie de registro. A los fines de aceptación de
la serie de registro, así como las series posteriores, los laboratorios
habilitados deben presentar lo detallado a continuación:
Inciso a) Documentación. Los registros de los procesos de elaboración y de los
controles internos presentados por el laboratorio elaborador deben ser
rubricados por el Responsable de Producción y de Aseguramiento de Calidad.
Los mismos tienen carácter de Declaración Jurada y deben seguir normas de
aseguramiento de la calidad y buenas prácticas de manufactura de conformidad a
lo establecido en la Resolución SENASA Nº 482 del 24 de mayo 2002.
La documentación necesaria se completa con:
I- El sistema de protocolización adoptado para registrar los procesos de
producción y los controles internos que permitan una eficaz auditoría.
II- Diagrama de flujo de producción y los Procedimientos Operativos Estándares
(POE) que describan el protocolo para la producción y el control de cada
producto.
III- Información relativa a la constitución, proceso de elaboración y control,
debiendo consignar como mínimo lo siguiente: número del protocolo, tipo de la
vacuna, número de la serie, cantidad de dosis, fechas de elaboración,
protocolos de producción y protocolos de control.
IV- Registros que permitan la trazabilidad de todos los procesos de producción
y control, así como del origen de las materias primas. Los registros deberán
guardarse al menos durante UN (1) año después de cumplida la fecha de
vencimiento de la vacuna.
Inciso b) Semilla Maestra. Cada semilla o inóculo maestro de cada antígeno
viral que sirva de fuente de siembra para la inoculación de todos los cultivos
de trabajo y de producción, debe tener documentado su origen y debe estar
analizado de manera que se garanticen su identidad, pureza y que esté libre de
agentes adventicios: bacterias, hongos, micoplasmas y virus.
Inciso c) Banco de Células Maestro. Se establece un banco de células maestro
para cada tipo de célula que se emplee. Asimismo se debe:
I- Documentar su identidad y origen.
II- Especificar en los POE la cantidad de pasajes admitidos en la producción y
control.
III- Caracterizarse para garantizar su identidad y su estabilidad genética.
IV- Analizarse su pureza para garantizar que esté libre de bacterias, hongos,
micoplasmas y virus.
Inciso d) Inactivantes. Se recomienda el empleo de inactivantes químicos de
primer orden. En caso de utilizarse el formol, se deben presentar controles de
formol residual.
Inciso e) Otros componentes. El uso de antibióticos y conservantes debe
declararse y registrarse, indicando si deberán aplicarse restricciones al uso
de los alimentos derivados de los animales vacunados.
Inciso f) Controles internos. Clasificación. Los controles internos deben
incluir como mínimo y según el caso en que corresponda, los siguientes que a
continuación se detallan:
I- Los controles de identidad.
II- Los controles de esterilidad.
III- Los controles de inocuidad o seguridad.
IV- Los controles de inactivación.
V- Los controles de pureza.
VI Los controles físico-químicos.
VII- Los controles de potencia o eficacia.
Los procedimientos operativos para estos controles deberán estar de acuerdo con
las normativas internacionales (9 CFR o Farmacopea Europea o Manual de OIE) o
nacionales aceptados por la DGLyCT.
Inciso g) La primera serie de registro a control deberá estar producida en las
mismas condiciones que las series posteriores según las buenas prácticas de
manufactura. La primera serie de registro a control, deberá contener un mínimo
número de dosis que representen la producción del laboratorio para esa vacuna.
ARTICULO 31. — Controles Internos. La totalidad de los controles internos de la
serie de registro, deberán estar finalizados al momento del retiro de las
muestras del producto final debidamente envasado, rotulado y estampillado según
se establece en la presente resolución. En el rótulo deberá constar el número
de expediente y la leyenda PRIMERA SERIE A CONTROL. Los controles internos
podrán ser realizados por el elaborador o por un tercero habilitado por SENASA
para tal fin.
ARTICULO 32. — Retiro de muestras. Una vez presentados los controles internos
con resultados satisfactorios y la Solicitud de Retiro de Muestras, la DGLyCT
tomará muestras del producto final, envasado, rotulado y estampillado. La
DGLyCT podrá retirar muestras de la fase acuosa viral, previo a su inactivación
o fase acuosa viral inactivada. En caso de tratarse de vacunas polivalentes se
pueden solicitar muestras de cada uno de los antígenos virales utilizados para
la formulación del producto previo a la inactivación y/o inactivados.
ARTICULO 33. — Tratamiento de Muestras. Las muestras serán empaquetadas,
cerradas y firmadas por el inspector del SENASA y el representante del
laboratorio elaborador conforme los requisitos estipulados en el Artículo 10 de
la presente resolución, para la inspección, retiro y codificación de muestras.
ARTICULO 34. — CONTROLES OFICIALES. Procedimientos. La DGLyCT realizará en la
Serie de Registro los controles de esterilidad, de inocuidad, físicos-químicos
y de potencia en cobayos con procedimientos de acuerdo al tipo de producto.
ARTICULO 35. — Control de Esterilidad. A continuación se detallan las
instrucciones y los lineamientos que se deben utilizar para llevar adelante un
correcto Control de Esterilidad.
Inciso a) Para cultivo de Anaerobios facultativos y Aerobios. Se sembrará UN
MILILITRO (1 ml) de vacuna en medio Tioglicolato fluido USP con el agregado de
Tween 80 al UNO POR CIENTO (1%) en tubos con DIEZ MILILITROS (10 ml) de medio.
Inciso b) Para hongos saprofitos y patógenos. Se sembrará CERO COMA CINCO
MILILITROS (0,5 ml) de vacuna en Agar glucosa CUATRO POR CIENTO (4%) según
Sabouraud en tubos con CINCO MILILITROS (5 ml) de medio.
Inciso c) Para determinación de contenido microbiano. Se sembrará CERO COMA
CINCO MILILITROS (0,5 ml) de vacuna en Agar caso - Peptona de Caseína - Peptona
de harina de soja USP en tubos con CINCO MILILITROS (5 ml) de medio.
Inciso d) Se siembran DOS (2) juegos de tubos con los TRES (3) medios de
cultivo y se incuban a VEINTICINCO GRADOS CENTIGRADOS (25°C) y a TREINTA Y CINCO GRADOS CENTIGRADOS (35°C) durante CATORCE (14) días.
Inciso e) Interpretación de los resultados. La muestra debe ser estéril para
pasar a las siguientes etapas de control. Se considera el control aprobado
cuando no se observa desarrollo bacteriano o fúngico en los cultivos
efectuados.
ARTICULO 36. — Control de Inactivación. A continuación se detallan las
instrucciones y los lineamientos que se deben utilizar para llevar adelante un
correcto Control de Inocuidad o Inactivación.
Inciso a) Las pruebas oficiales de inactivación viral evaluada por su inocuidad
sobre cultivos celulares, se realizan exclusivamente sobre muestras de
antígenos o vacunas que tengan controles de inactivación viral previos con
resultados satisfactorios realizados por el elaborador.
Inciso b) Cada elaborador debe presentar el método de elusión de antígeno o
ruptura de emulsión para su producto.
Inciso c) Se controlan vacunas terminadas, fase acuosa inactivadas y lotes de
antígenos inactivados sin adyuvantes.
Inciso d) Para verificar la correcta inactivación de las cepas virales
contenidas en la formulación de las vacunas, se utilizan células sensibles a
estos virus.
Inciso e) Células utilizadas. Las células utilizadas crecidas en monocapa
durante VEINTICUATRO y CUARENTA Y OCHO HORAS (24 y 48 hs), en frascos de
células de VEINTICINCO CON SETENTA Y CINCO CENTIMETROS CUADRADOS (25,75 cm2) o
CIENTO SETENTA Y CINCO CENTIMETROS CUADRADOS (175 cm2), son las siguientes o
cualquier otra que en un futuro demuestre ser sensible a estos virus:
I- MDBK (Madin Darby Bovine Kidney): para los virus DVB, IBR, BRSV, PI3 y
Coronavirus.
II- MA (Monkey, African green, kidney, embriónica): para Rotavirus.
III- HRT-18 (Human rectal tumor): para Coronavirus.
Inciso f) Preparación de la muestra.
I- El control de inactivación se puede realizar con muestra de fase acuosa,
muestra de lotes de antígenos virales inactivados y/o muestra de vacuna
terminada.
II- Las muestras de fase acuosa inactivada y de lotes de antígenos virales
inactivados utilizados para la formulación de la vacuna se inoculan en forma
directa.
III- En el caso de vacuna terminada, de acuerdo a su formulación oleosa u
acuosa, debe procederse según la metodología adecuada para la obtención del
antígeno viral (fase acuosa recuperada).
IV- Los laboratorios deberán proveer el método de ruptura de emulsión o elusión
de antígeno adecuado para cada vacuna presentada a control. Una vez realizado
el procedimiento adecuado, la fase acuosa recuperada se inocula directamente.
Inciso g) Inoculación de células.
I- Se inocula UN MILIMETRO (1 ml) de muestra en frascos de células de
VEINTICINCO CENTIMETROS CUADRADOS (25 cm2), SETENTA Y CINCO CENTIMETROS
CUADRADOS (75 cm2) o CIENTO SETENTA Y CINCO CENTIMETROS CUADRADOS (175 cm2). En
todos los casos, dejar adsorber UNA HORA (1 h) a TREINTA Y SIETE GRADOS
CENTIGRADOS (37°C) antes de colocar el medio de mantenimiento DIEZ, TREINTA Y
SETENTA Y CINCO MILILITROS (10, 30 y 75 ml), respectivamente. Dejar en
incubación a TREINTA Y SIETE GRADOS CENTIGRADOS (37°C) durante VEINTICUATRO HORAS (24 hs).
II- Observar si presenta efecto citopático. Si no presenta, congelar,
descongelar y efectuar un segundo pasaje con: UN MILILITRO (1 ml) del primer
pasaje de frasco de VEINTICINCO CENTIMETROS CUADRADOS (25 cm2) a otro frasco de
células de VEINTICINCO CENTIMETROS CUADRADOS (25 cm2); DIEZ MILILITROS (10 ml)
del primer pasaje de frasco de SETENTA Y CINCO (75) o CIENTO SETENTA Y CINCO
(175) a otro de SETENTA Y CINCO (75) o CIENTO SETENTA Y CINCO CENTIMETROS
CUADRADOS (175 cm2). Dejar adsorber UNA HORA (1 h) a TREINTA Y SIETE GRADOS
CENTIGRADOS (37°C) antes de colocar el medio de mantenimiento. Dejar en
incubación a TREINTA Y SIETE GRADOS CENTIGRADOS (37°C) durante CUARENTA Y OCHO HORAS (48 hs).
III- Observar si se presenta efecto citopático, si no presenta efecto el
resultado es NEGATIVO.
Inciso h) Interpretación de los resultados. La vacuna se considerará inocua
cuando no existan signos de replicación viral.
ARTICULO 37. — Control físico-químico para vacunas oleosas. A continuación se
detallan las instrucciones y los lineamientos que se deben utilizar para llevar
adelante un correcto control físico-químico para vacunas oleosas.
Inciso a) Control de tipo de emulsión.
I- Prueba de la Gota: Con una pipeta de UN MILILITRO (1 ml) se deposita una
gota de la vacuna en un envase con agua destilada.
II- Emulsión simple “agua en aceite”: La gota deberá permanecer compacta o
formará una película siempre en la superficie.
III- Emulsión doble “agua en aceite en agua”: La gota deberá diluirse
parcialmente, otorgando al agua una apariencia lechosa.
Inciso b) Control de estabilidad de la emulsión simple.
I- Por centrifugación de CUARENTA MILILITROS (40 ml) de vacuna durante UNA HORA
(1 h), a TRES MIL GRAMOS (3000 gr), separándose la fase aceitosa no emulsionada
en la parte superior, y la emulsión sin romper en la parte inferior. Se
permitirá una pequeña separación de líquido oleoso en la superficie siendo todo
el resto una emulsión uniforme.
II- Control de estabilidad de emulsión simple y doble a diferente temperatura.
Manteniendo la vacuna a diferentes temperaturas: Temperatura ambiente y a
TREINTA Y SIETE GRADOS CENTIGRADOS (37°C) durante TREINTA (30) días.
III- Sólo se permite una separación inferior de fase acuosa de hasta un CINCO
POR CIENTO (5%) del volumen total.
IV- También pueden llegar a formarse DOS (2) capas de emulsión blancas con un
borde más blancuzco en la superficie.
V- No se aceptarán vacunas con ruptura que formen una capa clara de agua en el
fondo del frasco.
Inciso c) Control de Conductividad:
I- Se medirá con celda de conductividad del tipo de inmersión cuya constante
sea no menos de SETENTA Y CINCO CENTESIMOS (0,75 cm-1).
II- La medición se realizará a VEINTE GRADOS CENTIGRADOS MAS MENOS DOS GRADOS
CENTIGRADOS (20°C ± 2°C).
III- La exactitud del equipo para realizar la determinación debe ser no menor
al UNO POR CIENTO (1%).
IV- Interpretación de resultados. Emulsión simple “agua en aceite”: deberá ser
menor a DIEZ MICROSIEMENS POR CENTIMETRO (10 uS/cm). Emulsión doble “agua en
aceite en agua”: deberá ser mayor a UN MICROSIMEN POR CENTIMETRO (1 mS/cm).
Inciso d) Control de viscosidad.
I- Se realizará utilizando un viscosímetro de Brookfield con rotor, y expresada
en centipoise. Se utilizará el rotor Nº 2, y la determinación se efectuará a
una velocidad de TREINTA REVOLUCIONES POR MINUTO (30 rpm).
II- Se aceptarán como valores mínimos y máximos QUINCE (15) y QUINIENTOS (500)
centipoise respectivamente, medidos a temperatura ambiente.
ARTICULO 38. — CONTROL DE POTENCIA EN COBAYOS. Los controles de potencia se
realizan en cobayos.
Inciso a) Este ensayo de prueba de vacunas virales en cobayos se basa en la
inmunización de cobayos con DOS (2) dosis de vacuna, por vía intramuscular o
subcutánea, de un volumen correspondiente a UNO SOBRE CINCO (1/5) de la dosis
bovina y un intervalo de VEINTIUN (21) días. Los animales se mantienen bajo
estudio durante un mínimo de TREINTA (30) días y se toman muestras de suero. En
caso de requerirse muestreos adicionales, éstos se especificarán en el
formulario de ensayo correspondiente.
Inciso b) A los TREINTA (30) días de iniciado el control se sangran los
animales vacunados, realizándoles el Control Indirecto de acuerdo a la valencia
viral a analizar por ELISA (BoHV-1, RVB y CoVB), Seroneutralización (BoHV-1,
VDVB) o inhibición de la hemoaglutinación (PI3) (ver Anexos I al IV).
Inciso c) La prueba de potencia en cobayos se considera válida cuando los
sueros de CERO (0) días posvacunación (DPV) y/o los sueros de los testigos
utilizados en la prueba resultan negativos para la prueba indirecta.
ARTICULO 39. — Vacunas en prueba. Codificación. Las vacunas en prueba perderán
su identidad mediante una codificación en la cual se utilizan frascos metálicos
numerados, donde se introduce el frasco original de vacuna y se precinta la tapa. Al momento de la codificación se confeccionan las siguientes planillas:
Inciso a) Planilla 1. En la cual consta el nombre del laboratorio elaborador,
nombre del producto, número de serie y número de estampilla del frasco a
utilizar. Es firmada por los representantes de cada laboratorio que posee
muestras a control de potencia y del SENASA presentes en la codificación de la
prueba y permanece en un sobre cerrado, sellado y firmado, hasta su
finalización.
Inciso b) Planilla 2. En la que figura la fecha de vacunación, el número de
frasco con su número de precinto.
ARTICULO 40. — Controles de Potencia. Técnicas. Los controles de potencia se
realizarán en cobayos conforme los requisitos estipulados en los Artículos 38
al 52 de la presente resolución. Para la Herpes-virus bovino 1 agente
etiológico de la Rinotraqueitis Infecciosa Bovina, para Rotavirus Bovino (RVB) agente causal de diarrea neonatal, para parainfluenza bovina tipo 3 agente
asociado a enfermedad respiratoria, y para el virus de diarrea viral bovina
responsable de enfermedad generalizada que lleva el mismo nombre, se
especifican a continuación las técnicas que se llevan a cabo para cada una de
ellas en particular:
Inciso a) Para Rinotraqueitis Infecciosa Bovina (IBR) los sueros serán
analizados por las técnicas de seroneutralización y/o ELISA, conforme el
procedimiento y las instrucciones tipificadas en el Anexo I de la presente
resolución.
Inciso b) Para RVB por la técnica de ELISA se lleva a cabo conforme el
procedimiento y las instrucciones tipificadas en el Anexo II de la presente
resolución.
Inciso c) Para PI3 por la técnica de inhibición de la Hemoaglutinación se lleva
a cabo conforme el procedimiento y las instrucciones tipificadas en el Anexo
III de la presente resolución.
Inciso d) Para VDVB por seroneutralización se lleva a cabo conforme el
procedimiento y las instrucciones tipificadas en el Anexo IV de la presente
resolución.
ARTICULO 41. — Vacunas para prevenir la Rinotraqueitis Infecciosa Bovina. En las vacunas para prevenir la Rinotraqueitis Infecciosa Bovina se considerarán aprobadas las que obtengan un título
de anticuerpos seroneutralizantes promedio en los cobayos vacunados, igual o
mayor a 1.31 o un título de ELISA igual o mayor a 1.93.
ARTICULO 42. — Vacunas para prevenir la diarrea neonatal por Rotavirus Bovino.
En las vacunas destinadas a prevenir la diarrea neonatal por Rotavirus
Bovino se considerarán aprobadas las que obtengan un título de anticuerpos
promedio determinado por ELISA en los cobayos inmunizados igual o mayor a 1.96.
ARTICULO 43. — Recontrol. Las vacunas que no aprueben el control de potencia
podrán ser presentadas a recontrol por única vez a solicitud del laboratorio
elaborador. Los resultados del nuevo control definen si la serie de vacuna es
aprobada o rechazada.
ARTICULO 44. — Controles Positivos. Los controles positivos serán incluidos en
cada prueba de potencia. En todas las pruebas serán incluidas vacunas de
referencia, según corresponda de Herpesvirus Bovino tipo 1 (BoHV-1) y Rotavirus
Bovino, oleosa o acuosa como control.
ARTICULO 45. — Controles Negativos. Los controles negativos serán incluidos en
cada prueba de potencia. Todas las pruebas incluirán un grupo de TRES (3) a
CINCO (5) cobayos testigos no vacunados que serán muestreados y sus sueros
analizados paralelamente a los grupos de vacuna en control y las vacunas de
referencia.
ARTICULO 46. — Nuevas Técnicas. Una vez validados los métodos de control
adecuados para establecer la potencia en los virus restantes contenidos en las
vacunas virales no vesiculares, se podrán agregar las nuevas técnicas.
ARTICULO 47. — Condiciones de los cobayos. Por cada serie en control se
vacunarán como mínimo SEIS (6) cobayos que reúnan las siguientes condiciones:
Inciso a) Edad: Mayor a TREINTA (30) días
Inciso b) Sexo: macho o hembra
Inciso c) Peso: CUATROCIENTOS GRAMOS (400 gr) ± CINCUENTA GRAMOS (50 gr).
ARTICULO 48. — Materiales a utilizar. Para efectuar el control de potencia en
cobayos es indispensable contar con los materiales que a continuación se
detallan:
Inciso a) Cajón con tapa o recipiente plástico con tapa que contendrá los
elementos.
Inciso b) Cinta adhesiva, de papel o celofán para rotular.
Inciso c) Fibra indeleble o lápiz negro de grafito (en este caso se escribirá
sobre la cinta de papel).
Inciso d) Algodón.
Inciso e) Guantes descartables.
Inciso f) Cofia y barbijo.
Inciso g) Servilletas de papel.
Inciso h) Jeringas descartables de 1,5 y 10 ml para la inoculación.
Inciso i) Jeringas descartables de 5, 10 y 20 ml para toma de muestra de
sangre.
Inciso j) Agujas descartables, cono rosa (40x12) y cono verde (21x8).
Inciso k) Recipiente con bolsa para descarte de materiales sucios.
Inciso l) Bolsas de autoclave, pequeñas y grandes.
Inciso m) Descarte de cortopunzantes.
Inciso n) Tubos de hemólisis largos para recolección de sangre.
Inciso o) Tijera.
Inciso p) Precintos.
Inciso q) Acido pícrico para marcar los animales.
Inciso r) Etanol SETENTA POR CIENTO (70%) y Cloroxilenol DOS COMA CINCO POR
CIENTO (2,5%)
Inciso s) Vacunas en control.
Inciso t) Vacuna de referencia para los antígenos vírales correspondientes.
ARTICULO 49. — PROCEDIMIENTO DE INOCULACION DE VACUNAS. Cuarentena de animales.
Los animales tendrán un plazo de adaptación después del ingreso a la sala de
inoculación en el bioterio de SIETE (7) días como mínimo.
ARTICULO 50. — Procedimiento. Se procede de la siguiente manera:
Inciso a) Se le da inicio a la experiencia sólo si se cuenta con animales
sanos. En caso de utilizar hembras, éstas no deberán estar preñadas, ni tener
crías al pie.
Inciso b) Antes de comenzar la inoculación se deben rotular las jaulas para
identificar los lotes asignados a las diferentes vacunas.
Inciso c) Retirar los animales de la jaula. La sujeción del animal dentro de la jaula será en forma cautelosa, silenciosa y firme para evitar el distrés.
Los animales se colocarán luego en un contenedor.
Inciso d) La sala deberá tener una temperatura confortable, bien iluminada y
contar con una mesada de trabajo y una pileta.
Inciso e) La mesada debe ser desinfectada.
Inciso f) Un operario debe tomar el cobayo con ambas manos y colocarlo boca
abajo, en posición horizontal, paralelo y apoyado sobre la mesa.
Inciso g) El segundo operario procederá a la inoculación subcutánea sobre la
parrilla costal, tomará la jeringa con la dosis medida de inóculo y con el
bisel de la aguja “hacia arriba”.
Inciso h) En el caso de aplicarla vía intramuscular el lugar de aplicación es
la cara interna del muslo.
Inciso i) Antes de descargar el contenido de la jeringa, se debe retraer el
émbolo para verificar que la inoculación no se realice en ninguna vía
sanguínea. Una vez realizado esto, se descargará el contenido de la jeringa.
Inciso j) Una vez finalizado el procedimiento, colocar cada animal en el
contenedor. Una vez finalizada la inoculación de todo el grupo, devolver los
animales a su jaula.
Inciso k) Se considera conforme un procedimiento de inmunización de cobayos
cuando el animal no sufre alteraciones fisiológicas durante la inoculación, y
no presenta reacciones adversas graves (shock anafiláctico, abscesos,
infecciones y necrosis en el punto de inoculación).
ARTICULO 51. — Extracción de sangre para obtención de muestras de suero. El
procedimiento es el siguiente:
Inciso a) La vía recomendada para el sangrado de cobayos es la punción
cardíaca, aunque son una alternativa, la vena yugular y la vena de la oreja.
Inciso b) Una vez terminado el procedimiento, el operario que sangró debe
retirar la aguja de la jeringa, y colocar la sangre en un tubo haciéndola
deslizar por la pared de éste para evitar la hemólisis.
Inciso e) Los tubos de sangre se llevan al laboratorio, se colocan a
temperatura ambiente durante UNA hora (1 h) para permitir el exudado del suero
o durante UNA HORA (1 h) a TREINTA Y SIETE GRADOS CENTIGRADOS (37°C) y luego se colocan a CUARENTA Y OCHO GRADOS CENTIGRADOS (48°C) durante UNA HORA (1 h). Los tubos se centrifugan a MIL QUINIENTOS REVOLUCIONES POR MINUTO (1500 rpm) durante
DIEZ MINUTOS (10 m) y el suero se trasvasa a tubos plásticos de UNO PUNTO CINCO
MILILITROS (1.5 ml). Si la muestra se ve turbia se vuelve a centrifugar en
microcentrífuga a CATORCE MIL REVOLUCIONES POR MINUTO (14.000 rpm) DIEZ MINUTOS
(10 m) y se trasvasa el sobrenadante a un nuevo tubo limpio.
Inciso f) Una vez obtenido el suero, rotular cada muestra y almacenarlas en
tubos de UNO PUNTO CINCO MILILITROS (1.5 ml) plásticos tipo eppendorf.
Inciso g) Todos los sueros de las sangrías serán fraccionados en CUATRO (4)
alícuotas y serán envueltas, selladas y firmadas. Una de ellas es utilizada por
la DGLyCT para su procesamiento, DOS (2) permanecerán en dependencias de la
DGLyCT como contramuestras. Una cuarta muestra permanecerá sellada en la DGLyCT
y será entregada a los representantes del laboratorio una vez concluidos la
totalidad de los controles, si son solicitados.
Inciso h) En los casos en que se produjeran problemas técnicos en la
realización de los controles que impidieran arribar a conclusiones precisas, la
DGLyCT decidirá al respecto.
ARTICULO 52. — DECODIFICACION. Finalización de los controles. Una vez
finalizados la totalidad de los controles se procederá a la apertura de los
sobres firmados y recipientes oportunamente precintados a los efectos de
identificar las marcas y series de las vacunas en control y confeccionar un
acta.
ARTICULO 53. — Rechazo y decomisación. Las series de vacunas que no aprobaran
los controles de esterilidad, inocuidad o inactivación y/o fisico-químicos,
citados en los Artículos 35, 36 y 37 de la presente resolución no podrán
continuar con las siguientes etapas de control y serán rechazadas y
decomisadas.
ARTICULO 54. — Aprobación de controles oficiales. Información. Obtenidos los
resultados aprobados de esterilidad, inocuidad o inactivación, físico-químicos
y potencia en cobayos, se informa a la DGLyCT.
ARTICULO 55. — Facultad de la DGLyCT. Queda facultada la DGLyCT para realizar
cualquier otro control adicional que considere necesario a fin de asegurar la
correcta elaboración según lo declarado en el expediente de registro,
conservación de las vacunas, así como el correcto desempeño del producto una
vez aplicado.
ARTICULO 56. — Prueba de estabilidad inmunogénica. La DGLyCT podrá optar por su
realización, previa comunicación al laboratorio productor. Se procederá de
acuerdo al método establecido para el control de potencia de series y podrá ser
realizada hasta la fecha de vencimiento de la vacuna.
ARTICULO 57 — Otorgamiento del Certificado de Uso y Comercialización.
Finalizada la totalidad de los controles de autorización con resultados
satisfactorios, la DGLyCT elevará los mismos a la Dirección Nacional de Agroquímicos, Productos Veterinarios y Alimentos (DNAPVyA) y se
otorgará el Certificado de Uso y Comercialización.
ARTICULO 58. — Series aprobadas. Comercialización. Las series de registro
aprobadas podrán ser comercializadas una vez obtenido el certificado
correspondiente, cuyo número deberá ser impreso en cada uno de los envases.
ARTICULO 59. — Plazo de decomisación. Las series rechazadas o retiradas de
control serán decomisadas en un plazo máximo de SESENTA (60) días, no
admitiéndose cambios de destino.
ARTICULO 60. — Cuarentena. Las series presentadas quedarán en cuarentena hasta
la finalización de los controles oficiales y no podrán ser modificadas o
alteradas.
ARTICULO 61. — Controles posteriores a la obtención del Certificado. Una vez
obtenido el Certificado de Uso y Comercialización, todas las series elaboradas
con posterioridad deben ser sometidas a los controles de serie según lo
descripto en la presente reglamentación.
ARTICULO 62. — SOBRE EL CONTROL DE SERIES. Obtención del Certificado. Las
personas físicas o jurídicas deben obtener el Certificado de Uso, previo a la
presentación a control de cada una de las series posteriores.
ARTICULO 63. — Solicitud de Retiro de Muestras. Las series de vacuna
presentadas a control, iniciarán su trámite con la presentación de la Solicitud
de Retiro de Muestras en la DGLyCT, ésta deberá estar acompañada con los
resultados de los controles de producción y de los controles de producto
terminado firmados por los responsables técnicos respectivos.
ARTICULO 64. — Toma de Muestras. Las muestras serán tomadas por personal del
DGLyCT según el procedimiento determinado en el Artículo 10 de la presente
resolución.
ARTICULO 65. — Fórmula cuali-cuantitativa y el Proceso de Producción. La
fórmula cuali-cuantitativa y el proceso de producción de las series deberá ser
igual a la serie de registro aprobada y presentada en el expediente
correspondiente.
ARTICULO 66. — Controles Oficiales. Las series son controladas por la DGLyCT en
esterilidad, inocuidad o inactivación, físico-químico y potencia en cobayos
conforme los requisitos estipulados en los Artículos 34 al 61 de la presente
resolución para los Controles Oficiales.
ARTICULO 67. — Imposibilidad de realizar controles. En caso que la DGLyCT no
pueda realizar alguno de los controles mencionados anteriormente, esa serie de
vacuna puede ser liberada con los controles internos aprobados del elaborador
con resultado satisfactorio.
ARTICULO 68. — Series no aprobadas. Las series no aprobadas en el control de
potencia pueden ser presentadas a un nuevo control oficial por única vez a
solicitud del laboratorio elaborador. Los resultados del nuevo control definen
si la serie de vacuna es aprobada o rechazada.
ARTICULO 69. — Certificado de Uso y Comercialización. Finalizados la totalidad
de los controles, con resultados satisfactorios, la DGLyCT otorgará el
correspondiente Certificado de Uso y Comercialización de la serie en control.
ARTICULO 70. — DISPOSICIONES GENERALES. Control de autorización y de serie. Los
controles de autorización y los de series deben ser analizados por personal del
servicio oficial en las dependencias de la DGLyCT o en aquellas que el SENASA
determine.
ARTICULO 71. — Interdicción en el depósito. Las series de vacunas presentadas a
control de autorización o de serie quedan interdictas en el depósito
establecido y autorizado por la DGLyCT, desde la extracción de la muestra hasta
que la DGLyCT lo determine. A solicitud del elaborador, la DGLyCT puede
autorizar el traslado de las series en control.
ARTICULO 72. — Garantía de la inviolabilidad del producto. Las firmas
elaboradoras deben asegurar bajo Declaración Jurada y con utilización de
precintos o cerramientos que garanticen la inviolabilidad del producto, la
permanencia de la totalidad de las dosis presentadas a control en las cámaras
autorizadas durante todo el proceso.
ARTICULO 73. — Temperatura de Conservación. La temperatura de conservación de
la vacuna debe estar comprendida entre DOS GRADOS CENTIGRADOS (2°C) y OCHO GRADOS CENTIGRADOS (8°C) o según lo indicado por el elaborador. Las cámaras frías deben
contar con registro de temperatura.
ARTICULO 74. — Período de Validez. El período de validez de las vacunas virales
no vesiculares es de UN (1) año a partir de su formulación cuando no se
presenten pruebas de estabilidad.
ARTICULO 75. — Solicitud de Períodos de Validez Mayor. Para obtener períodos de
validez mayores a los detallados en el artículo anterior, se deben presentar
pruebas de estabilidad que acrediten un plazo mayor de validez del producto. No
se aceptan solicitudes de extensión de vencimiento de series en particular. La
prueba de estabilidad se realizará en la DGLyCT y deberá cumplir con los
requisitos de aprobación de Potencia en Cobayos, descriptos en los Artículos 38
al 46 de la presente resolución, al tiempo solicitado por el laboratorio
elaborador.
ARTICULO 76. — Medidas de transporte. El laboratorio elaborador debe arbitrar
las medidas necesarias para que los productos sean remitidos y conservados
hasta que lleguen a poder del destinatario, en las condiciones especificadas en
la solicitud de inscripción.
ARTICULO 77. — Cantidad mínima de dosis. Se aceptan únicamente series con una
cantidad mínima de CINCUENTA MIL (50.000) dosis.
ARTICULO 78. — Se aprueba el procedimiento y las instrucciones tipificadas para
llevar a cabo las técnicas de Seroneutralización o ELISA, para la Rinotraqueitis Infecciosa Bovina (IBR) que, como Anexo I, forma parte integrante de la
presente resolución.
ARTICULO 79. — Se aprueba el procedimiento y las instrucciones tipificadas para
llevar a cabo las técnicas de ELISA, para RVB que, como Anexo II, forma parte
integrante de la presente resolución.
ARTICULO 80. — Se aprueba el procedimiento y las instrucciones tipificadas para
llevar a cabo las técnicas de inhibición de la Hemoaglutinación para PI3 que,
como Anexo III, forma parte integrante de la presente resolución.
ARTICULO 81. — Se aprueba el procedimiento y las instrucciones tipificadas para
llevar a cabo las técnicas de Seroneutralización, para VDVB que, como Anexo IV,
forma parte integrante de la presente resolución.
ARTICULO 82. — Infracciones. Los infractores a la presente resolución son
pasibles de las sanciones que pudieran corresponder de conformidad con lo
establecido por el Capítulo VI del Decreto Nº 1.585 del 19 de diciembre de
1996, sin perjuicio de las medidas preventivas inmediatas que pudieran
adoptarse.
ARTICULO 83. — Carácter de las Pruebas Oficiales de Control. Declárense
públicas las pruebas oficiales de control de vacunas en todas sus etapas.
ARTICULO 84. — Plazos de Actualización. Los laboratorios que poseen vacunas con
registro y número de certificado vigente a la fecha de emisión de la presente
resolución deben actualizar el expediente del producto de acuerdo con las
exigencias de la presente resolución en un plazo máximo de TRES (3) años.
ARTICULO 85. — Organo Rector. La Dirección General de Laboratorios y Control Técnico (DGLyCT) del SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA es el
órgano rector para la interpretación y decisión en aquellas cuestiones no
contempladas en la presente norma.
ARTICULO 86. — Vigencia. La presente resolución entra en vigencia a partir de
su publicación en el Boletín Oficial.
ARTICULO 87. — De Forma. Comuníquese, publíquese, dése a la Dirección Nacional del Registro Oficial y archívese. — Méd. Vet. MARCELO S. MIGUEZ, Presidente,
Servicio Nacional de Sanidad y Calidad Agroalimentaria.
ANEXO I
A- ELISA para BoHV
Este ensayo es un ELISA directo para la detección de anticuerpos anti-BoHV-1.
Kit del INSTITUTO NACIONAL DE TECNOLOGIA AGROPECUARIA (INTA).
Se sensibilizan placas con virus BoHV-1 (obtenido a partir de células MDBK
infectadas) (pocillo positivo) o células MDBK control negativo de infección
(pocillo negativo), especialmente preparado para tal fin. La concentración
óptima de virus y mock para sensibilizar las placas se determina por titulación
cruzada para cada lote producido y es constante para toda la placa. Los sueros se ensayan en ambos posillos (+ y -) en diluciones seriadas base 4
comenzando desde una dilución mínima de 1/40 en SEIS (6) diluciones para
evaluar la respuesta a la vacunación de cobayos (Parreño, Romera y col, 2010).
El ensayo se revela utilizando como anticuerpo detector un Ac anti IgG (H+L) de
cobayo marcado con peroxidasa. Como sistema sustrato cromógeno se utiliza
H202/ABTS.
MATERIALES
• Placas para ELISA Immulon 1 B (Dynatech Lab, USA, cat. # 014-01-3455).
• Tips amarillos (hasta 200 µl).
• Tips azules (hasta 1000 µl).
• Tips blancos Multistep Multicanal (1000 µl).
• Cubetas descartables o reciclables autoclavables.
• Descarte.
• Bolsas de autoclave verdes.
• Papel absorbente.
• Guantes descartables.
EQUIPOS
• Micropipeta hasta 200 µl (tolerancia máxima admitida: 5 µl).
• Micropipeta hasta 20 µl (tolerancia máxima admitida: 0.2 µl).
• Micropipeta hasta 1000 µl (tolerancia máxima admitida: 10 µl).
• Micropipeta multicanal OCHO (8) o DOCE (12) canales, hasta 300 µl. Sin
restricciones respecto a la tolerancia.
• Estufa de 37°C con atmósfera controlada a CERO COMO CINCO POR CIENTO (0,5%)
de CO2. Se admite para esta técnica una variabilidad en el rango de:
1. Temperatura de la estufa: 0.5°C.
2. Porcentaje de CO2: 0.1%.
• En ausencia de estufa con CO2, se pueden realizar las incubaciones
en una estufa de 37°C dentro de una cámara húmeda.
• Lector de ELISA con filtro para lectura a 405 nm (rango: 400-410 nm).
• Heladera 4-8°C.
REACTIVOS
• Buffer Coating (carbonato/bicarbonato) pH 9,6. (Tolerancia en pH: 0.03)
Na2CO3
0,159 grs.
NaHCO3
0,293 grs.
Agua destilada c.s.p.
100 ml
Ajustar pH con NaOH/HCl 1 N
Almacenar a 4°C (1-8°C).
• Buffer Acido cítrico pH 5.0 (Tolerancia en pH: 0.03)
Acido Cítrico Monohidrato
0,960 grs.
NaOH 1 N aproximadamente 10 ml para llevar a pH
5,0
Ajustar a pH: 5,0 ± 0.5 con Na(OH) o HCI1N.
Agua destilada c.s.p. 100 ml
Medir pH luego de agregarle el agua destilada. Ajustar nuevamente en caso de
ser necesario.
Almacenar a 4°C (1-8°C).
• ABTS Solución Madre
ABTS
0,22 grs.
Buffer Acido Cítrico 10 ml.
Fraccionar en alícuotas de 1 ml en tubos plásticos tipo “eppendorf” de 1.5 ml.
Almacenar a: -20 ± 5°C.
• Solución de uso ABTS
(Preparar en el momento de uso sólo la cantidad necesaria y descartar el
remanente).
Solución madre ABTS 300
µL
Buffer Acido cítrico
10 ml
Agua oxigenada (H2O2) 10
µL
Se puede reemplazar por soluciones de ABTS comerciales listas para usar
• SDS (dodecil/laurel sulfato de sodio) al CINCO POR CIENTO (5%) en agua.
• Agua Oxigenada de 30 volúmenes.
• Buffer de Lavado (PBS 1X Tween 0,05%)
PBS
1000 ml
Tween20
500 µL
• Buffer de bloqueo y diluyente. PBS/Tween 20 0.05%/OVA 1% PH 7.4
Tween20
500 ul.
PBS 1X
1000 ml.
Ovoalbúmina 10 grs.
ANTIGENO
Antígeno viral positivo: Preparado a partir de cultivos de MDBK
infectados con cepas de BHV-1 de referencia.
Antígeno control, negativo o mock: Preparado a partir de cultivos de
MDBK mock infectados.
CONJUGADO
Conjugado Anti IgG de Cobayo marcado con peroxidasa.
Affinity purified goat anti- Guinea Pig Ig G (H+L) peroxidase labeled, KPL,
cat. # 14-17-06.
Peroxidase- conjugated affiniPure Goat anti-guinea pig IgG (H+L), Jackson, cat.
# 106-035-003
Conjugados de otras marcas o conjugados producidos internamente previamente
verificados/validados en INTA como óptimos para ser utilizados en el ensayo de
ELISA.
CONTROLES
Se utiliza un Control Positivo (suero de cobayo inmunizado con vacuna de
referencia, de título conocido), un Control Negativo, (suero negativo para
cualquier concentración de siembra) y Blanco de Reactivos (PBS). Para cada uno
de los controles se utilizan CUATRO (4) pocillos (DOS (2) capturas positivas y
sus DOS (2) capturas negativas correspondientes).
Se recomienda además, incluir en cada ensayo una muestra positiva de título
conocido y otra muestra negativa (sueros estándares internos). Estas muestras
se siembran aleatoriamente en distintos lugares en al menos dos de las placas
del ensayo y se corren en todos los ensayos.
Control positivo cobayo: Pool de sueros de CINCO (5) cobayos vacunados
con DOS (2) dosis de 0.600 ml de vacuna conteniendo 107 DICT50/ml
de HoVB-1 en adyuvante oleoso o acuoso según corresponda (Vacuna de Referencia
INTA-SENASA).
Se considerarán conformes aquellos ensayos donde el control positivo se
encuentre dentro del valor promedio ± 1 desvío Standard (SD).
_____________________________________________________________________________________________________________________
valor promedio ± 1 SD = 0.520 ≤ 0.740 ≤ 0.960
_____________________________________________________________________________________________________________________
Dicho suero, analizado por seroneutralización debe arrojar un título de
anticuerpos neutralizantes contra BoHV-1 entre DOS PUNTO CUATRO (2.4) y TRES
PUNTO CERO (3.0).
Control negativo cobayo: Suero de cobayo cuya absorbancia corregida en
la dilución de uso resulte menor al cut off de la técnica CUARENTA POR CIENTO (40%) de la absorbancia corregida del control positivo.
STD +: Suero positivo de cobayo de título conocido
STD
Preparación: Estos controles y estándares se seleccionan a partir de
sueros de cobayos vacunados con vacunas de concentración de Ag conocida y
asignada como vacuna de referencia.
PROCEDIMIENTO DEL ELISA
Sensibilización de la placa.
Realizar la dilución de trabajo del Antígeno Positivo (Producción de virus
BoHV-1) en Buffer Coating pH 9,6.
Diluir el Ag Negativo (MDBK Mock) en la misma dilución que el Ag + en Buffer
Coating pH 9,6.
Colocar 50 µl de Captura Positiva en las filas B-D-F-H.
Colocar 50 µl de Captura Negativa en las filas A-C-E-G.
_____________________________________________________________________________________________________________________
Se necesitan 3 ml de Ag+ y Ag- por placa de NOVENTA Y SEIS (96) pocillos
_____________________________________________________________________________________________________________________
• Incubar la placa tapada ON (17 horas ±2 hs), entre 4° C y 8° C.
• Descartar el contenido de la placa.
• Lavar la placa TRES (3) veces con PBS/Tween20 0,05%.
• Secar golpeando la placa contra un papel absorbente.
1. Bloqueo
Sobre la placa sensibilizada con Virus y Mock, lavada y secada según el punto
3.1, se deben colocar 100 µL/pocillo de Buffer de bloqueo (PBS/Tween20
0.05%, Ova 1%, pH 7.4).
• Incubar la placa 1 hora ± 15 minutos, a 37°C en 5% CO2.
• Descartar el contenido de la placa.
• Secar golpeando la placa contra un papel absorbente.
2. Muestras
Descongelar las muestras a ensayar, así como también controles y estándares
positivos y negativos.
En un ensayo estándar entran SIETE (7) muestras por placa, con SEIS (6)
diluciones para cada una, aunque según las necesidades especiales se pueden
diseñar las placas con más muestras, y menos diluciones por muestra.
Las diluciones de las muestras se realizan en placas sustitutas (placas limpias
de NOVENTA Y SEIS (96) pocillos aptas para cultivos celulares).
Los pocillos donde se sembrarán los controles (Positivo, Negativo y PBS), no
deben ser completados con PBS en la placa sustituta, sino que se cargarán
directamente sobre la placa original (ver diseño de placa).
Para el sembrado de muestras y diluciones correspondientes se procederá sobre
la placa sustituta.
Se colocarán 195 µL, de buffer diluyente en las columnas 1 (A-B-C-D-E-F-G-H) y
7 (A-B-C-D-E-F-G-H).
Se colocarán 150 µl de buffer diluyente en el resto de las columnas 2-3-4-5-6
(A-B-C-D-E-F-G-H) y 8-9-10-11-12 (C-D-E-F-G-H).
En los pocillos 1H y 1G se colocarán 5 µl respectivamente de la muestra “1”.
En los pocillos 1F y 1E se colocarán 5 µl respectivamente de la muestra “2”. Así sucesivamente con el resto de las muestras (ver ilustración de diseño de placa).

Diseño de placa:
• Diluciones de muestras:
Con una pipeta multicanal de 50 µl se homogenizarán las muestras de la primer
columna de pocillos (195 µl PBS+ 5 µl muestra) y se traspasarán 50µl a la
segunda columna, donde se homogenizará tomando 50 µl para traspasarlos a la siguiente. Así sucesivamente hasta la columna SEIS (6) inclusive. El mismo procedimiento se
seguirá desde la columna UNA (1) a SEIS (6) y con nuevos tips de SIETE (7) a la
DOCE (12) inclusive.
De esta manera quedarán las muestras diluidas, desde una dilución inicial de
1/40 y luego diluciones en base 4 (Rango de diluciones analizadas expresadas en
logaritmos: 1.6-4.61).
Tomar 50 µL de las diluciones hechas en la placa sustituta, y traspasarlos a la
placa de reacción, utilizando el mismo set de tips comenzando de la dilución
más diluida a la más concentrada.
Sembrado de controles: Preparar la dilución correspondiente de los
controles y sembrar 50 µl de éstos en los pocillos correspondientes 7-8 y
9-10, A-B de la placa de reacción según se indica en la figura.
• Luego de sembradas todas las muestras en la placa:
• Incubar la placa 1 hora ± 15 minutos, a 37°C en 5% CO2.
• Descartar el contenido de la placa.
• Lavar la placa 4 veces con PBS/Tween 0.05%.
• Secar golpeando la placa contra un papel absorbente.
3. Conjugado.
Realizar la dilución de conjugado en PBS Tween OVA, según su título específico
para este ensayo. Agregar la dilución de uso (según su titulación en este
ELISA) de conjugado Anti IgG de Cobayo marcado con Peroxidasa.
- Colocar 50 µl en todos los pocillos.
• Incubar la placa UNA (1) hora a 37°C en 5% CO2.
• Descartar el contenido de la placa.
• Lavar la placa CINCO (5) veces con PBS/Tween 0.05%.
• Secar golpeando la placa contra un papel absorbente.
4. Revelado
Preparar: Solución de uso ABTS
Sol. Madre 300 µl
Buffer ácido cítrico 10 ml
Agua oxigenada 10 µL
_____________________________________________________________________________________________________________________
Se necesitan 5 ml de solución de Revelado por placa de NOVENTA Y SEIS (96)
pocillos
_____________________________________________________________________________________________________________________
- Colocar 50 µl, en cada pocillo
- Dejar reaccionar 10 minutos o hasta que los controles entren en el rango
esperado de lectura.
Los SD+ deben llegar a su título correspondiente.
- Cortar la reacción con 50 µl de SDS al 5%
5. Lectura y cálculos
LECTURA
• Leer las placas a 405 nm o 410 nm en un Lector de ELISA.
CALCULOS
Calcular la Densidad óptica (DO) corregida de cada muestra (DO cap positiva -
DO de cap negativa).
Calcular el promedio de las réplicas del control positivo.
Calcular el CUARENTA POR CIENTO (40%) del promedio del control positivo.
Calcular el promedio de las réplicas del control negativo.
Calcular el SD del control negativo.
Calcular el PP% de cada muestra en cada dilución
PP=DOcorr. muestra/DOcorr. C+ * 100
6. Aceptación del ensayo (CONFORMIDAD)
Los criterios que a continuación se describen se aplicarán individualmente a
cada placa.
Los resultados pueden interpretarse e informarse siempre que se haya dado
conformidad al ensayo.
El ensayo se considera conforme cuando: el valor de la DOc del control positivo
se encuentra dentro del rango establecido (0.520 a 0.960), el control negativo y el blanco de reactivos presentan porcentaje de positividad
menores al punto de corte de la técnica CUARENTA POR CIENTO (40%), el título del suero standard positivo da el valor esperado +/- una dilución base 4 (error del
método).
Para validar el ensayo los sueros de los cobayos inmunizados con la vacuna de
referencia deben dar un título promedio dentro del rango establecido como el
valor promedio obtenido (luego de realizar 5 pruebas) ± dos desvíos estándar.
7. Informe de resultados
Se informa el título de Ac anti-BoHV-1 detectado como el log en base 10 de la
inversa de la máxima dilución cuyo porcentaje de positividad es mayor o igual
al punto de corte del ensayo, establecido como mayor o igual al CUARENTA POR
CIENTO (40%) del control positivo (100%PP).
Las muestras negativas en la mínima dilución de suero ensayada (1/40) se
expresan con un título arbitrario de CERO PUNTO TRES (0.3) para los cálculos.
8. APROBACION DE LA PRUEBA DE POTENCIA EN COBAYO SEGUN ESTA TECNICA
Se evaluarán todos los sueros de los animales inmunizados con la vacuna en
control. Se seleccionarán CINCO (5) de los sueros con mayor título obtenido y
sobre ellos se realizará el promedio. Para la APROBACION de la vacuna sometida
a control, el promedio de los títulos deberá ser mayor o igual a 1.93 por la
técnica de ELISA para BoHV-1.
B- SERONEUTRALIZACION PARA BoHV-1
La prueba de seroneutralización para la detección de Ac contra BoHV-1 emplea el
método Suero variable-virus fijo: donde diluciones variables de sueros problema
(seriadas base 2 o base 4) se enfrentan a una cantidad establecida y fija de
virus (100 DICT50/ml). La mezcla suero-virus se coloca en un sistema
susceptible a la infección por BoHV-1, en este caso células de línea MDBK.
La inversa de la mayor dilución que protege a las células de la infección se
denomina título seroneutralizante del suero (expresión del título por punto
final).
El título neutralizante del suero también se puede establecer por el método de
Reed y Muench (virus fijo-suero variable).
MATERIALES
• Placas de Cultivo de NOVENTA Y SEIS (96) pocillos, estériles.
• Tips amarillos (hasta 200µl).
• Tips azules (hasta 1000 µ).
• Tubos plásticos cónicos de 1500 µl.
• Tubos cónicos de 50ml.
• Frascos de vidrio con tapa a rosca (GIBCO o similar).
• Pipetas de vidrio estériles de 5-10ml.
• Cubetas descartables.
• Descarte.
• Bolsas de autoclave verdes.
• Papel absorbente.
EQUIPOS
• Micropipeta monocanal, hasta 200 µl (tolerancia admitida 5).
• Micropipeta monocanal, hasta 20 µl (tolerancia admitida 5).
• Micropipeta monocanal, hasta 1000 µl (tolerancia admitida 10).
• Micropipeta multicanal 8 hasta 1000 µl. Sin restricciones respecto a la tolerancia.
• Micropipeta multicanal 12. Sin restricciones respecto a la tolerancia.
• Propipeta (pipetaid, Drummond Scietific Co. O equivalente).
• Incubadora de 37°C y 5% CO2.
• Cabina de seguridad biológica.
• Baño termostático (temperatura a 56 ± 3°C).
• Heladera 4-8°C.
• Microscopio óptico invertido.
REACTIVOS
• Suspensión de células MDBK: con una concentración de 250.000 cel./ml, (rango
200.000-280.000).
• MEM-E
• Suero Fetal Bovino (SFB): controlado (libre de micoplasmas y endotoxinas y
probado en cultivos celulares), fraccionado en alícuotas de 10 ± 2ml y 20 ± 2ml
y conservado a -20 ± 3°C.
• Antibiótico 100X
Penicilina sódica G
10,025 gr
Sulfato de Streptomicina
33,35 gr
Gentamicina SO4
25 gr
PBS(10X)
50 ml
Agua destilada c.s.p.
5 litros
Una vez disuelto se esteriliza por filtración (0.22 um) y se almacena a -20 ± 3°C.
La fracción en uso se conserva a 4-8°C.
Se adiciona 10 ml de ATB por cada litro de medio de trabajo.
• Virus de trabajo: BoHV-1 Cepa de referencia Los Angeles (LA) o cepa de virus
BoHV-1 autóctonos. Diluida de tal manera de contener 100DICT 50%.
CONTROLES
* Control positivo cobayo: Suero de cobayo vacunado con vacuna anti-BoHV-1.
* Control negativo cobayo: Pool de sueros normales de cobayo (sueros de cobayos
pre-inmunización).
* Estándar positivo: Suero de título conocido.
* Estándar negativo: Suero normal de cobayo.
Preparación: Estos controles se seleccionan a partir de sueros de cobayos
vacunados con vacunas de referencia para BoHV-1.
Se corren en un mínimo de CINCO (5) ensayos de SN y se seleccionan si su título
cumple con los requisitos antes mencionados. Diluir ½ en glicerol para evitar
su congelamiento, fraccionar en alícuotas de 100 µl y almacenar a -20°C.
PROCEDIMIENTO
1. Suspensión celular
Se necesitan 10ml de suspensión celular con 250.000 cel./ml por placa.
Una vez que se recibe la suspensión se realiza el recuento celular, si la
suspensión contiene menor cantidad de células, ésta se concentra por
centrifugación a 1000 rpm, 5 minutos y se elimina el sobrenadante excedente. Si
la suspensión contiene más células se diluye con medio de trabajo. Una vez
realizado el ajuste se repite el recuento, el rango admitido va desde
200.000-280.000 cel/ml. Una vez ajustada la suspensión se mantiene a
temperatura ambiente bajo agitación suave en agitador magnético.
Fórmula a utilizar para el ajuste:
vol final = conc inicial * vol inicial / 250.000 cel/ml
2. Inactivación de las muestras
Previo a su utilización en el ensayo de SN, las muestras de suero deben ser
inactivadas en baño a 56 ± 3°C, durante 30 ± 5 minutos. Este paso se realiza
fundamentalmente para inactivar el complemento de los sueros a analizar.
3. Preparación del medio de trabajo
El medio de dilución de las muestras y del virus, se prepara a partir del MEM-E
+ 1% de ATB + 2% de SFB.
4. Ensayo de SERONEUTRALIZACION SUERO VARIABLE-VIRUS FIJO
• Colocar 75 µl/pocillo de medio en todas las placas a utilizar.
• Diseño de la placa de los sueros problema: Agregar 25 µl de la muestra
problema, por cuadruplicado, (Fila A o Fila E pocillos 1-4; 5-8; 9-12,
respectivamente) (ver figura 1).
• Se comienza desde una dilución mínima de 1/4 que sumado al volumen de virus y
células queda en una dilución inicial de 1/8.
• Incluir en forma aleatoria entre las muestras a analizar estándares de título
conocido.
• Diseño de la placa control: Se colocan los sueros control positivo y negativo
del mismo modo que las muestras. Para realizar el control de células se colocan
150 µl de medio de trabajo por cuadruplicado en cuatro filas (16 pocillos
totales). Para el control de las 100 DICT de virus, se realizan 3 diluciones en
base 10 a partir de la dilución de trabajo. Se siembran 75 µl por cuadruplicado
de las 4 diluciones preparadas a las cuales se les agrega 75 µl de medio (ver
figura 2).
• Realizar diluciones en base 4, pasando 25 µl, descartando los últimos 25 µl
para todas las muestras y sueros controles.
• Se realiza un control de toxicidad de cada muestra colocando 75 µl de medio
en otra placa.
• Preparar la dilución de trabajo de virus (100 DICT) en el medio de trabajo.
Preparar el volumen necesario para todas las placas del ensayo considerando que
se necesitan 8 ml de virus por placa.
• Colocar 75 µl de la dilución de trabajo del virus en todas las placas,
excepto en la placa de controles de toxicidad, en el control de células y en el
control de 100 DICT.
• Incubar las placas (mezcla suero-virus) durante 1 hora a 37 ± 1°C en atmósfera de CO2 al 5 ± 1%.
• Agregar sobre la mezcla suero-virus 100 µl por pocillo, de la suspensión
celular conteniendo 250.000 cel./ml en todas las placas.
• Incubar las placas a 37 ± 1°C en atmósfera de CO2 al 5 ± 1%, durante 48-72
hs.
5. Lectura
• Al cabo de las 48-72 horas la lectura se realiza por inspección de las
monocapas al microscopio óptico.
• La lectura es por observación de efecto citopático. Se considera positivo
aquel pocillo que presente un foco de CPE característico de BoHV-1. En los
controles de toxicidad se debe observar la monocapa igual que los controles de
células, libre de efecto citopático viral y libre de efecto tóxico.
• Si un suero determinado presenta toxicidad en las diluciones analizadas, el
título de anticuerpos neutralizantes no podrá determinarse por esta
técnica.
6. Aceptación del ensayo (CONFORMIDAD) El ensayo se considera conforme cuando:
6.1. Las monocapas de los controles de células se encuentran en buen estado (MC
confluentes, células refringentes, sin alteraciones morfológicas, sin rastros
de contaminación y sin CPE de BoHV-1).
6.2. El título de la suspensión viral debe contener 100 DICT 50%, con un rango
admitido entre 50-200 DICT (ver tabla 1).
6.3. El control positivo debe dar el título esperado ± 1 pocillo. Ejemplo:
2.30< 2.4 < 2.50
6.4. El control negativo debe dar negativo. Se le coloca un valor arbitrario de
0.3 para los cálculos.
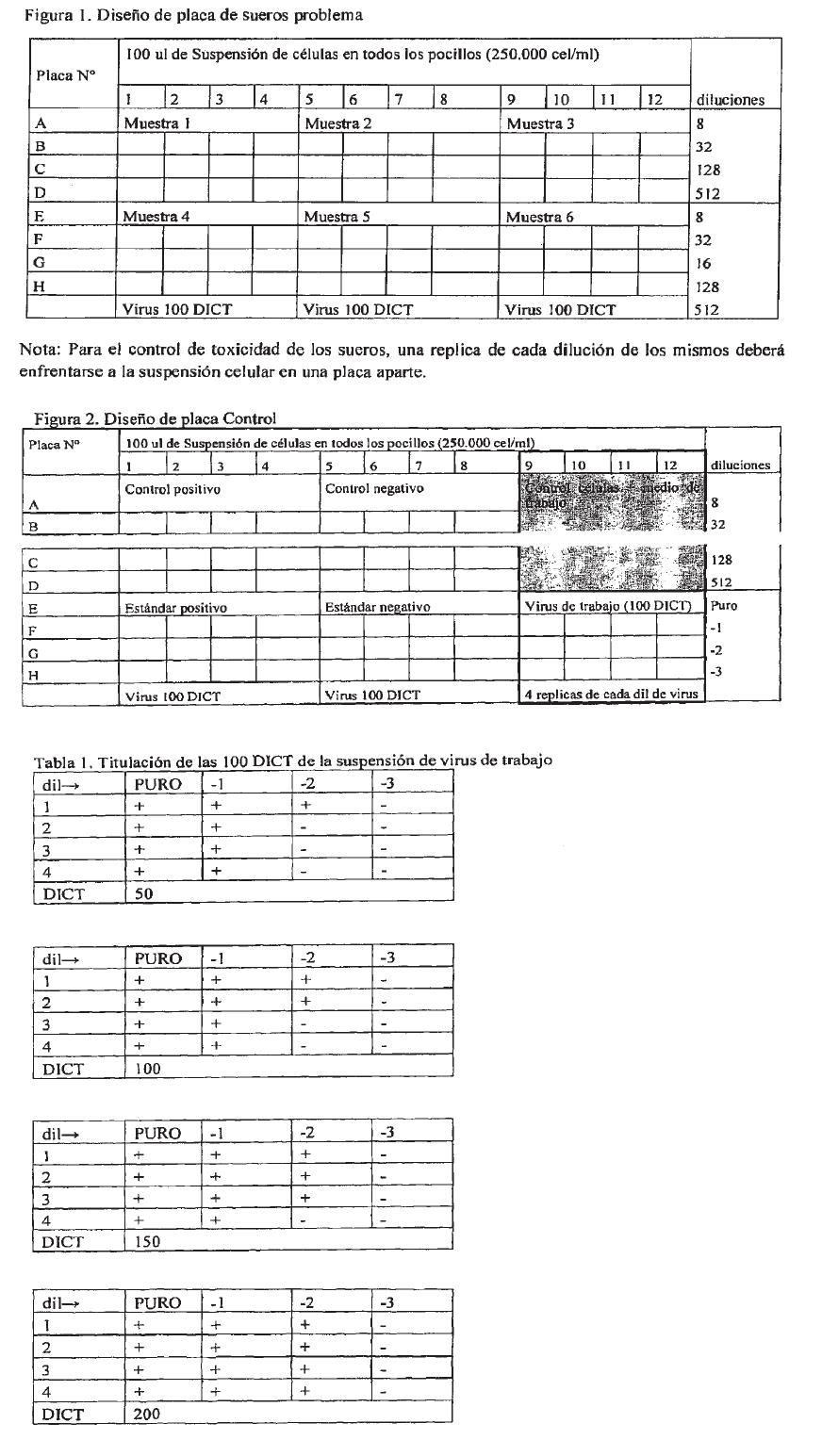
7. Interpretación
El título neutralizante del suero analizado se obtiene según la cantidad de
replicadas protegidas en las diluciones seriadas en base al método de
interpolación de Reed y Muench.
Tabla 2. Titulación de Ac en microplacas (log 10)
|
Pocillos Protegidos
|
1/8
|
1/32
|
1/128
|
1/512
|
1/2048
|
1/8192
|
1/32768
|
1/131072
|
|
1
|
0.70
|
1.30
|
1.90
|
2.50
|
3.10
|
3.70
|
4.30
|
4.90
|
|
2
|
0.90
|
1.50
|
2.10
|
2.70
|
3.30
|
3.90
|
4.50
|
5.10
|
|
3
|
1.10
|
1.70
|
2.30
|
2.90
|
3.90
|
4.10
|
4.70
|
5.30
|
|
4
|
1.20
|
1.80
|
2.40
|
3.00
|
4.10
|
4.20
|
4.80
|
5.40
|
Para validar el ensayo los sueros de los cobayos inmunizados con la vacuna de
referencia deben dar un título promedio dentro del rango establecido como el
valor promedio obtenido (luego de realizar 5 pruebas) ± dos desvíos estándar.
8. Informe de resultados
Se informa el título de Ac anti-BoHV-1 neutralizantes obtenido según el método
de Reed y Muench.
Las muestras negativas en la mínima dilución de suero ensayada (1/8) se
expresan con un título arbitrario de 0.3 para los cálculos.
9. APROBACION DE LA PRUEBA DE POTENCIA EN COBAYO PARA IBR SEGUN SN
Se evaluarán todos los sueros de los animales inmunizados con la vacuna
sometida a control. Se seleccionarán CINCO (5) de los sueros con mayor título
obtenido y sobre ellos se realizará el promedio. Para la APROBACION de la
vacuna sometida a control, el promedio de los títulos deberá ser mayor o igual
a 1.31 por la técnica de SN para BoHV-1.
ANEXO II
ELISA PARA RVB
Este ELISA utilizado consiste en un ensayo doble sándwich, desarrollado a
partir de la técnica descripta para bovinos (Fernández y col. 1996; 1998;
Parreño y col, 2004). La técnica fue adaptada para detectar Ac IgG en suero de
cobayos vacunados con vacunas utilizadas para la prevención de las diarreas
neonatales que contengan RV. Se utiliza para detectar anticuerpos IgG anti
rotavirus en suero de cobayos inmunizados con vacunas destinadas a prevenir las
diarreas neonatales del ternero.
Brevemente, se sensibilizan placas de ELISA de NOVENTA Y SEIS (96) pocillos con
un suero hiperinmune anti-RVB obtenido en terneros descalostrados desafiados e
hiperinmunizado con rotavirus bovino en buffer carbonato-bicarbonato pH: 9,6.
Las placas se incuban durante 18 horas a 48°C y luego se bloquean con leche descremada. Posteriormente se agrega sobrenadante clarificado de cultivos de MA-104
infectados con RVB cepa IND (P[5]G6) con título viral no menor a 10^7 UFF/ml
(pocillos positivos) o sobrenandante de células MA-104 sin infectar (pocillos
negativos). A continuación se colocan las muestras a analizar en diluciones seriadas
en base 4 a partir de una dilución de 1/16. Finalmente, se agregan un
anticuerpo comercial anti-IgG de cobayo, marcado con peroxidada. La reacción se
revela utilizando H2O2/0,05% ABTS como sistema sustrato/cromógeno y detenida
con el agregado de 50 de SDS al 10%. La lectura de las placas se realiza a 405
nm.
Los resultados pueden interpretarse e informarse siempre que se haya dado
conformidad al ensayo. Una muestra puede ser negativa, positiva o inespecífica.
Pero en general el ensayo se utiliza para obtener el título de Ac IgG anti-RV
el que se expresa como la inversa de la máxima dilución con lectura superior al
punto de corte o “cut off” del ensayo.
ALCANCE Y OBJETIVOS
Este ELISA se ha diseñado para detectar Ac IgG (H+L) en sueros de cobayos vacunados
con vacunas para la prevención de las diarreas neonatales, que contengan RV.
MATERIALES
• Placas para ELISA NUNC-inmuno plate-Maxisorp, cat.# 442404 o similar
• Tips amarillos (hasta 200 µl)
• Tips azules (hasta 1000 µl)
• Tips blancos Multistepper Multicanal (1000 µl).
• Cubetas descartables o reciclables autoclavables
• Cubeta descartable para ABTS (según lo indicado en el I 22-02-05 -
Clasificación y Disposición de Residuos Especiales)
• Tubos cónicos de 15 y 50 ml
• Descarte
• Bolsas de autoclave verdes
• Papel absorbente
• Guantes descartables
EQUIPOS
• Micropipeta hasta 200µl (tolerancia máxima admitida: 5µl)
• Micropipeta hasta 20µl (tolerancia máxima admitida: 0.2µl)
• Micropipeta hasta 1000µl (tolerancia máxima admitida: 10 µl)
• Micropipeta multicanal 8-12 hasta 300µl. Sin restricciones respecto a la tolerancia.
• Micropipeta multistepper multicanal 8 hasta 300 µl. Sin restricciones
respecto a la tolerancia.
• Estufa de 37°C con atmósfera controlada a 0,5% de CO2.
Se admite para esta técnica una variabilidad en el rango de:
3. temperatura de la estufa: 0.5° C.
4. Porcentaje de CO2: 0.1%.
• Lector de ELISA con filtro para lectura a 405 nm (rango: 400-410 nm)
• Microcentrífuga (hasta 14.000 rpm)
• Heladera 4-8°C
• Balanza digital hasta 200 g
REACTIVOS
• Buffer Coating (carbonato/bicarbonato) pH 9,6. (Tolerancia en pH: 0.03)
Na2CO3
0,159 grs.
NaHCO3
0,293 grs.
Agua destilada c.s.p. 100 ml
Ajustar pH con NaOH/HCl I N
Almacenar a 4°C (1-8°C)
• Buffer Acido cítrico pH 5.0 (Tolerancia en pH: 0.03)
Acido Cítrico Monohidrato 0,960 grs.
NaOH IN aprox.
10 ml para llevar a pH 5,0
Ajustar a pH: 5,0 ± 0.5 con Na(OH) o HCIIN.
Agua destilada c.s.p. 100 ml
Medir pH luego de agregarle el agua destilada. Ajustar nuevamente en caso de
ser necesario.
Almacenar a 4°C (1-8°C)
• ABTS Solución Madre
ABTS
0,22 grs.
Buffer Acido Cítrico 10 ml.
Fraccionar en alícuotas de 1 ml en tubos plásticos tipo “eppendorf” de 1.5 ml.
Almacenar a -20°C ± 5°C.
• Solución de uso ABTS
(Preparar en el momento de uso sólo la cantidad necesaria y descartar el
remanente).
Solución madre ABTS
300µl
Buffer Acido cítrico
10ml
Agua oxigenada H2O2
10µL
• SDS (dodecil/laurel sulfato de sodio) al 5% en agua.
• Agua Oxigenada de TREINTA (30) volúmenes.
• Buffer de Lavado (PBS 1X Tween 0,05%)
PBS
1000ml
Tween 20
500 µL
• Buffer de bloqueo
Leche descremada en polvo 10 grs.
PBS / Tween 20 c.s.p.
100ml
• Captura suero hiperinmune de ternero descalostrado desafiado e
hiperinmunizado con rotavirus (INTA).
ANTIGENOS
• Antígeno Positivo: suspensión de Rotavirus Bovino grupo A producido en
células MA104 (INTA).
• Antígeno negativo: Células MA-104 MOCK (NO INFECTADAS O CONTROL NEGATIVO DE
INFECCION)
CONJUGADO
• Ac conjugados con peroxidasa: Conjugado Anti IgG de Cobayo marcado con
peroxidasa. Affinity purified goat anti- Guinea Pig Ig G (H+L) peroxidase
labeled, KPL, cat # 14-17-06 o de otras marcas o productos internamente
verificados/validados en INTA como óptimos para utilizarse en esta técnica.
CONTROLES
• Controles positivos: muestra de suero de cobayo ya titulados en ensayos
previos y que presentan un título conocido probado al menos en CINCO (5)
ensayos. Estos sueros se obtiene a partir de animales vacunados con vacuna de
RVB de referencia.
• Controles negativos: suero normal de cobayo diluido 1 en 4.
Se corren los controles que correspondan en TODAS las placas de un ensayo,
según el tipo de muestras a ensayar.
Sueros Estándares positivos y negativos: sueros de título conocido que se
corren intercalados entre las muestras.
• PBS (Blanco de reactivos). Se corre en TODAS las placas de un ensayo.
PREPARACION DE MUESTRAS
Sueros:
No necesitan preparación previa, sólo que estén totalmente descongelados y
homogeneizados.
PROCEDIMIENTO DEL ELISA
1. Sensibilización de la placa
Preparar el volumen necesario de Captura positiva: según la cantidad de placas
a utilizar y el la dilución de trabajo del lote de suero en uso. Se necesitan
10ml de del dilución de trabajo de la captura positiva por placa de NOVENTA Y
SEIS (96) pocillos.
Colocar 100 µL/ pocillo, en todas las placas de reacción
Incubación: ON 18 ± 2 hs a 4-8°C
• Descartar el contenido de la placa.
• Lavar la placa 1 vez con PBS/Tween20 0.05%
• Secar golpeando la placa contra un papel absorbente.
2. Bloqueo
Leche Descremada 10% en PBS/ Tween 20 0.05%
Colocar 100 µL/pocillo
Incubación: 1 hs 37°C
_____________________________________________________________________________________________________________________
A partir de este paso, si no se cuenta con estufa con atmósfera de CO2
las incubaciones se pueden realizar a 37°C en una cámara húmeda (recipiente plástico con tapa donde se coloca una servilleta de papel humedecido con agua
destilada).
_____________________________________________________________________________________________________________________
• Descartar el contenido de la placa.
• Lavar la placa 2 veces con PBS/Tween 20 0.05%
• Secar golpeando la placa contra un papel absorbente.
3. Antígenos
• Realizar la dilución de trabajo del Antígeno Positivo (Lote de Rotavirus
bovino para ELISA) en PBS/Tween20 0.05%
• Diluir el Ag Negativo (MA-104 Mock) en la misma dilución que el Ag positivo,
en PBS/Tween20 0.05%.
_____________________________________________________________________________________________________________________
Se necesitan 5ml de Ag+ y 5 ml de Ag por placa de NOVENTA Y SEIS (96) pocillos
_____________________________________________________________________________________________________________________
• Colocar 100µl de Ag positivo en las columnas impares
• Colocar 100µl de Ag negativo en las columnas pares
• Incubación: 1 hs 37°C
• Descartar el contenido de la placa.
• Lavar la placa 4 veces con PBS/Tween20 0,05%.
• Secar golpeando la placa contra un papel absorbente
_____________________________________________________________________________________________________________________
NOTA: Si las placas no se usan en el momento, después de los lavados, se
almacenan a -20°C (± 2°C) hasta su momento de uso.
_____________________________________________________________________________________________________________________
4. Muestras
_____________________________________________________________________________________________________________________
NOTA: En cada placa del ensayo incluir: Blanco de reactivos: PBS/Tween20 0.05%,
4 diluciones de un control positivo y dos pocillos con la dilución 1/4 de un
control negativo. Incluir en el ensayo en forma aleatoria en alguna de las
placas estándares positivos de título conocido y estándares negativos.
_____________________________________________________________________________________________________________________

Realizar las diluciones en placas sustitutas (placas de NOVENTA Y SEIS (96)
pocillos de cultivo, limpias, no estériles)
• Cargar 150µl de PBS/Tween en todos los pocillos y cargar en la primera fila
el volumen de muestra o su dilución previa
Ejemplos: 50µl de muestra pura (dil inicial 1/4); o 50µL de una dilución previa
1/16 (dil inicial 1/64) 10µl de muestra pura (dil. inicial 1/16); o 10µL de una
dilución previa 1/16 (dil inicial 1/256)
• Traspasar 50µl de fila en fila (así se obtienen diluciones base 4)
• Una vez finalizadas las diluciones, traspasar 100µl/pocillo a la placa de
reacción, comenzando desde la dilución más diluida a la más concentrada.
• Descartar las placas sustitutas y colocar las placas de reacción en la estufa
• Incubar la placa de 1 h a 37°C, en 5% CO2.
• Descartar el contenido de la placa.
• Lavar la placa 4 veces con PBS/Tween 0.05%.
• Secar golpeando la placa contra un papel absorbente.
5. Conjugado
Realizar la dilución de trabajo del conjugado - anti-lgG (H+L) cobayo. Colocar
100µl del conjugado en todos los pocillos.
_____________________________________________________________________________________________________________________
Se necesitan 10ml de dilución de trabajo de conjugado por placa de NOVENTA Y
SEIS (96) pocillos
_____________________________________________________________________________________________________________________
• Incubar la placa una hora a 37°C, en 5% CO2.
• Descartar el contenido de la placa.
• Lavar la placa 4 veces con PBS/Tween 0.05%.
• Secar golpeando la placa contra un papel absorbente.
6. Revelado
Preparar: Solución de uso ABTS
Sol. Madre 300µl
Buffer ácido cítrico 10ml
Agua oxigenada 10µL.
_____________________________________________________________________________________________________________________
Se necesitan 10ml de Solución de Revelado por placa de NOVENTA Y SEIS (96)
pocillos
_____________________________________________________________________________________________________________________
Se puede reemplazar por reactivos comerciales listo para usar
• Colocar 100µL en cada pocillo
• Dejar reaccionar en oscuridad, revisar las placas cada 2-3 minutos, realizar
lecturas previas y cortar cuando el control positivo y los estándares positivos
hayan alcanzado el título esperado.
• Cortar la reacción con 50 µL de SDS al 5%
7. Lectura y cálculos
LECTURA
• Leer las placas a 405 nm en un Lector de ELISA.
CALCULOS
o Calcular la Densidad óptica (DO) corregida de cada muestra (DO cap positiva -
DO de cap negativa).
o Calcular el promedio y el desvío de la ODc los controles negativos
o Calcular el Cut off de la placa: promedio de los controles negativos + 2 STD,
en general este valor no debe superar un valor de 0.100. Se toma como positivas
a las muestras que cuya ODc superan un valor de corte del ensayo establecido en
una DOc = 0.100 ± 0.050.
8. Aceptación del ensayo (conformidad)
El ensayo se considera conforme cuando el título del control positivo, alcanza
su título esperado, el negativo se mantiene negativo DO y la DOc del blanco de
reactivo no supera el valor 0.100.
Una muestra se considera:
Positiva: Si su DOc es mayor al cut off de la placa.
Negativa: Si su DOc es menor al cut off de la placa.
Inespecífica: Si su DO en virus y mock es elevada. Es decir la muestra
presenta un color intenso en ambas capturas. En este caso se recomienda volver
a ensayar la muestra previa adsorción con suspensión de células MA-104. Si el
problema persiste el título de Ac no pude definirse por esta técnica.
9. Informe de resultados
El título de Ac de una muestra se establece como la inversa de la máxima
dilución cuya DOc sea mayor al cut off de la placa, (cut off=0.100).
Se informa el título de Ac anti-RVB detectado como el log en base 10 de la
inversa de la máxima dilución cuyo DOc resulte mayor al punto de corte del
ensayo (cut off=0.100)
Las muestras negativas en la mínima dilución de suero ensayada (1/16) se
expresan con un título arbitrario de 0.3 para los cálculos.
10. APROBACION DE LA PRUEBA DE POTENCIA EN COBAYO SEGUN ESTA TECNICA:
Se evaluarán todos los sueros de los animales inmunizados con la vacuna en
control. Se seleccionarán CINCO (5) de los sueros con mayor título obtenido y
sobre ellos se realizará el promedio. Para la APROBACION de la vacuna sometida
a control, el promedio de los títulos deberá ser mayor o igual a 1.96 por la
técnica de ELISA para RVB.
ANEXO III
IHA PARA PI3
Este ensayo determina la presencia de anticuerpos dirigidos contra las
hemoaglutininas virales, también llamados “inhibidores de la hemoaglutinación”
en sueros de animales vacunados. Antes del ensayo, los sueros sufren un
tratamiento con kaolín para adsorber inhibidores inespecíficos de la
hemoaglutinación que pudieran estar presentes, luego, diluciones seriadas de
los sueros se enfrentan a una concentración fija de virus, establecida en 8
UHA/25 ul. La reacción se revela agregando glóbulos rojos de cobayo. Cuando en
un suero existen anticuerpos específicos dirigidos a la HA viral, se formarán
complejos Ag-Ac que bloquearán la hemoaglutinación e inhibirán su capacidad de
aglutinar glóbulos rojos, es decir, se impide la unión del virus a los glóbulos
en suspensión y consecuentemente se observa la formación de un botón rojo
característico en el fondo del pocillo.
Los resultados pueden interpretarse e informarse siempre que se haya dado
conformidad al ensayo. Las muestras se ensayan diluciones seriadas base 2
comenzando a partir de 5 (ver Tabla I). Se tomará como punto final de la
actividad del suero (título de Ac IHA anti PI-3) a la inversa de la máxima
dilución en la que el fenómeno de hemoaglutinación ha sido inhibido. El
resultado final se expresa en Unidades Inhibidoras de la Hemoaglutinación
(UIHA). La recíproca de la dilución de punto final de la actividad del suero,
multiplicada por las unidades hemoaglutinantes del virus utilizado (8 UHA) nos
resultará en el número de unidades inhibidoras de la hemoaglutinación del suero
por unidad de volumen.
La presencia de reacciones IHA de diluciones inferiores a 1/10 (40-80 UIHA) se
consideran NEGATIVAS.
Valores superiores a 1/80 (640 UIHA o más) representan respuesta a la
vacunación.
Para cobayos vacunados (DOS (2) dosis con un intervalo de VEINTIUN (21) días):
se considera como respuesta óptima a la vacuna cuando se detecta seroconversión
(incremento de al menos de 1 logaritmo) entre el título de UIHA de la muestra
de suero pre-vacunación y la muestra correspondiente a los 30 dpv (NUEVE (9)
días post 2° dosis).
MATERIALES
• Placa de 96 wells fondo en U limpias no estériles.
• Cubetas descartables o autoclavables, limpias, no estériles.
• Tips amarillos (hasta 200 µl)
• Tips azules (hasta 1000 µl)
• Tubos plásticos de 1.8 ml tipo “eppendorf”
• Tubos cónicos de 15 ml
• Tubos cónicos de 50 ml
• Pipeta pasteur plástica
• Descarte
• Bolsas de autoclave verdes
• Papel absorbente
• Guantes de látex descartables
• Agujas 25/8
• Jeringa de 5 ml
• Algodón y alcohol
EQUIPOS
• Micropipeta hasta 200µl (tolerancia máxima admitida: 5ul)
• Micropipeta hasta 40µl (tolerancia máxima admitida: 0.4ul)
• Micropipeta hasta 1000 µl (tolerancia máxima admitida: 10ul)
• Micropipeta multicanal 8-12 hasta 5-50µl. Sin restricciones respecto a la tolerancia.
• Microcentrífuga (hasta 14.000 rpm)
• Centrífuga refrigerada (hasta 5.000 rpm)
REACTIVOS
• Virus de Trabajo:
Suspensión de PI-3, ajustado a la concentración de 8 UHA/25 ul o 16 UHA/50 ul
• Diluyente:
PBS 1 X, pH: 7.2-7.4
• Solución de Kaolín:
Kaolín
0,04g
PBS 1X
5ml
• Glóbulos rojos de cobayos (ver obtención en punto 4)
• Alsever 1X
• Sueros control: positivo y negativo
• Sueros Estándar: positivo y negativo
Preparación: Los sueros controles corresponden a pooles de sueros de cobayos
vacunados con vacunas de concentración de Ag conocida. Para confeccionar los
pooles se seleccionan sueros con títulos medios (320-640 UIHA) (control
positivo) y o sueros de animales negativos (control negativo).
Como estándares se utilizar sueros de cobayos de título conocido,
preferentemente altos (1260 UIHA) y negativos.
TRATAMIENTO PREVIO DE LAS MUESTRAS
• Inactivar los sueros durante 30 minutos a 56°C.
• Colocar 50ul de suero en un tubo de 1.8 ml, agregar 50ul de la solución de
Kaolín, homogenizar por vortex. Incubar durante 10 ± 2 minutos a temperatura
ambiente (24-27°C).
• Centrifugar durante 15 ± 2 minutos a 1500 rpm.
• Tomar 50ul del sobrenadante y transferir a otro tubo con 75ul de PBS 1X y
homogenizar con vortex.
(La dilución final del suero es de 1/2 * 2/5=1/5)
• Los sueros controles y estándares positivos y negativos deben tratarse de
igual manera que las muestras.
_____________________________________________________________________________________________________________________
En el caso que los sueros no sean utilizados en ese momento, pueden guardarse a
-20°C y analizarse dentro de la semana de tratados.
_____________________________________________________________________________________________________________________
PREPARACION DE LA DILUCION DE GLOBULOS ROJOS
• Preparar, en esterilidad, una jeringa con 1 ml de anticoagulante Citrato (o
Alsever 1X al medio del volumen que se necesita de glóbulos).
• Tomar muestra de sangre de un cobayo por punción cardíaca (4 ml + 1 ml
anticoagulante = 5ml totales).
• Una vez finalizada la extracción, sacar la aguja de la jeringa (descartar en
descarte de material corto-punzante). Este procedimiento se realiza para evitar
la hemólisis de los GR.
• Colocar la sangre en un tubo cónico de 15 ml, estéril. Centrifugar a 1500 ±
200 rpm, a 4-8°C durante 5 ± 1 min.
• Eliminar la fase líquida utilizando una pipeta pasteur plástica o pipeta
automática/tip de 1000ul.
• Lavado: Resuspender el paquete de glóbulos en PBS 1X y llevar a un volumen de
aprox. 15 ml. Centrifugar durante 10 minutos a 1800 ± 200 rpm a 4-8°C. Realizar 2 lavados. Descartar el sobrenadante.
_____________________________________________________________________________________________________________________
IMPORTANTE: En cada lavado el sobrenadante debe mantenerse límpido, la
presencia de un tinte rojizo es indicador de hemólisis y en ese caso los GR NO
son aptos para su utilización en el ensayo.
_____________________________________________________________________________________________________________________
La suspensión de GR debe preparase fresca en el momento de realización del
ensayo.
• Preparar la dilución de trabajo de glóbulos: Primero se realiza una dilución
¼ (1 ml de paquete de glóbulos más 3 ml de PBS 1X) y luego partiendo de esta
dilución se hace una dilución 1/40 (1 ml de la dil ¼ más 29 ml de PBS 1X). De
este modo se obtiene la dilución final de trabajo de 1/120 ó 0.8%.
• Una vez hecha la dilución de GR se procede a titular y a ajustar el Virus PI-3 a la dilución de trabajo mediante la técnica de hemoaglutinación.
TITULACION Y AJUSTE DE LA DILUCION DE TRABAJO DEL VIRUS PI-3
1. Descongelar el virus en uso, una placa fondo en U cargar 50ul de PBS 1X en 2
filas y cargar otra fila para el control de GR.
2. Agregar 50ul del virus de trabajo.
3. Realizar diluciones al medio, transfiriendo 50ul desde los pocillos 1 hasta
12.
4. Agregar 50ul de la dilución 1/120 glóbulos rojos en todos los pocillos.
5. Incubar a Temperatura ambiente (20-27°C) durante 1 hora.
6. Una vez que se visualiza la formación del botón de glóbulos en la hilera de
control de GR, se puede proceder a la lectura.
7. El virus debe tener un título de 16 UHA/50ul. Si el título obtenido es
menor, dicha suspensión NO ES APTA PARA EL ENSAYO. Si el título viral es mayor,
diluir con PBS 1X y volver a titular.
PROCEDIMIENTO DEL ENSAYO DE IHA
• Colocar 25ul de PBS 1X en toda la placa excepto en fila G.
• Agregar 25ul del suero tratado en los pocillos F, G y H.
(Se pueden analizar DOCE (12) muestras por placa de la fila UNO (1) a DOCE (12) con SIETE (7) diluciones por muestra, o se pueden usar la placa
apaisada, en cuyo caso se analizan OCHO (8) muestras de A a H con ONCE (11)
diluciones por muestra)
• Realizar diluciones seriadas base 2, pasando 25ul, desde la fila F hasta la fila A, descartando los últimos 25ul.
Los sueros estándares se colocan en forma aleatoria entre las muestras. Los
sueros controles positivos y negativos se colocan al final de todos los sueros
problemas ya tratados y del mismo modo que éstos. Se deja una columna libre
para realizar el control de glóbulos rojos y otra para realizar nuevamente la
titulación de virus.
• Agregar 25ul de virus en la dilución establecida de uso (16 UHA/25 ul) en
todas las filas, excepto en H que quedará como control de suero sin virus. Este
último control cumple la función de detectar la presencia de actividad
hemoaglutinante inespecífica en los sueros problema.
• Incubar las placas con la mezcla suero-virus durante una hora a temperatura
ambiente (24-27°C).
• Agregar 50ul de la suspensión de glóbulos rojos (81/120) en todas las placas.
• Incubar a temperatura ambiente hasta la formación del botón de glóbulos en la
columna de control de glóbulos.
LECTURA E INTERPRETACION
La lectura se realiza por visualización directa.
ACEPTACION DEL ENSAYO (CONFORMIDAD)
Para que un ensayo se considere conforme se deben cumplir los siguientes
requisitos:
o La suspensión de virus de trabajo debe dar un título de 16 UHA/50ul (8
UIHA/25ul)
o El botón de GR en los pocillos control debe ser sólido
o Los sueros controles y estándares positivos deben dar el título esperado (se
admite una variación de 1 dilución).
o Los sueros controles y estándares negativos deben ser negativos.
o Para determinar el título de una muestra, no debe observarse hemoaglutinación
en el pocillo control de suero sin virus.
INTERPRETACION
Se tomará como punto final de la actividad del suero (título de Ac IHA anti
PI-3) a la máxima dilución en la que el fenómeno de hemoaglutinación ha sido
inhibido. El resultado final se expresa en unidades inhibidoras de la
hemoaglutinación (UIHA). La recíproca de la dilución de punto final de la
actividad del suero, multiplicada por las unidades hemoaglutinantes del virus
utilizado (8 UHA/25ul) resultará en el número de unidades inhibidoras de la
hemoaglutinación del suero por unidad de volumen.
Para evaluación de la inmunogenicidad de vacunas en cobayos (dos dosis
de un volumen correspondiente a 1/5 de la dosis bovina, administrada con un
intervalo de VEINTIUN (21) días): Se considera como respuesta óptima a la
vacuna cuando se detecta seroconversión (incremento de al menos de UN (1)
logaritmo) entre el título de UIHA de la muestra de suero pre-vacunación (o
testigo) y la muestra correspondiente a los 30 dpv (NUEVE (9) días post segunda
dosis). El promedio del título de Ac IHA anti PI-3 en el sueros de los cobayos
(n=5) analizados deberá ser mayor o igual a 1.50 para considerar la vacuna como
APROBADA.
Tabla 1. Título de Ac IHA anti PI-3
|
POCILLO
|
Ultima Dilución que
presenta IHA
|
Título de la muestra
(UIHA/25 ul) = dil * 8
|
Título de la muestra
(log10)
|
|
H
|
1
|
10
|
1
|
|
G
|
5
|
40
|
1,60
|
|
F
|
10
|
80
|
1,90
|
|
E
|
20
|
160
|
2,20
|
|
D
|
40
|
320
|
2,50
|
|
C
|
80
|
640
|
2,80
|
|
B
|
160
|
1280
|
3,10
|
|
A
|
320
|
2560
|
3,40
|
ANEXO IV
SERONEUTRALIZACION PARA VDVB
La prueba de seroneutralización para la detección de Ac contra VDVB emplea el
método Suero variable-virus fijo: donde diluciones variables de sueros problema
(seriadas base 2 o base 4) se enfrentan a una cantidad establecida y fija de
virus (100 DICT50). La mezcla suero-virus se coloca en un sistema susceptible a
la infección por BDV, en este caso células de línea MDBK.
El título neutralizante del suero se establece por el método de Reed y Muench
(virus fijo - suero variable), siempre que se haya dado conformidad al ensayo.
MATERIALES
• Placas de Cultivo de NOVENTA Y SEIS (96) pocillos, estériles
• Tips amarillos (hasta 200µl)
• Tips azules (hasta 1000 µl)
• Tubos plásticos cónicos de 1500 µl
• Tubos cónicos de 50 ml
• Frascos de vidrio con tapa a rosca (GIBCO o similar)
• Pipetas de vidrio estériles de 5-10 ml
• Cubetas descartables
• Descarte
• Bolsas de autoclave verdes
• Papel absorbente.
EQUIPOS
• Micropipeta monocanal, hasta 200µl (tolerancia admitida 5)
• Micropipeta monocanal, hasta 20µl (tolerancia admitida 5)
• Micropipeta monocanal, hasta 1000 µl (tolerancia admitida 10)
• Micropipeta multicanal 8 hasta 1000 µl. Sin restricciones respecto a la
tolerancia
• Micropipeta multicanal 12. Sin restricciones respecto a la tolerancia
• Propipeta (Pipetaid, Drummond Scietific Co. O equivalente)
• Incubadora de 37°C y 5% CO2
• Cabina de seguridad biológica
• Baño termostático (temperatura a 56 ± 3°C)
• Heladera 4-8°C
• Microscopio óptico invertido
REACTIVOS
• Suspensión de células MDBK: con una concentración de 250.000 cel./ml, (rango
200.000-280.000).
• MEM-E
• Suero Fetal Bovino (SFB): controlado (libre de micoplasmas y endotoxinas y
probado en cultivos celulares), fraccionado en alícuotas de 10 ± 2 ml y 20 ± 2
ml y conservado a -20 ± 3°C. Su fraccionamiento debe registrarse con un Nº de
PR (lote interno).
• Antibiótico 100X
Penicilina sódica G
10,025gr
Sulfato de Streptomicina
33,35gr
Gentamicina SO4
25g
PBS (10X)
50ml
Agua destilada c.s.p.
5 litros
Una vez disuelto se esteriliza por filtración (0.22 um) y se almacena a -20° ± 3°C.
La fracción en uso se conserva a 4-8°C. Se adiciona 10 ml de ATB por cada litro
de medio de trabajo.
• Virus de trabajo: BDV citopático tipo 1 A - Cepa de Referencia Singer, NADL o cepas autóctonas antigénicamente similares.
CONTROLES
Control Positivo Cobayo: Suero de cobayo vacunado con vacuna conteniendo
VDVB de título 10^7 DICT50/dosis o mayor.
Control Negativo Cobayo: Pool de sueros normales de cobayo (sueros de cobayos
preinmunización).
Estándar Positivo: Suero de título conocido.
Estándar negativo: Suero normal de cobayo.
PROCEDIMIENTO
SUSPENSION CELULAR
Se necesitan 10 ml de suspensión celular con 250.000 cel./ml por placa.
Una vez que se recibe la suspensión se realiza el recuento celular, si la
suspensión contiene menor cantidad de células, ésta se concentra por
centrifugación a 1000 rpm, 5 minutos y se elimina el sobrenadante excedente. Si
la suspensión contiene más células se diluye con medio de trabajo. Una vez
realizado el ajuste se repite el recuento, el rango admitido va desde
200.000-280.000 cel/ml. Una vez ajustada la suspensión se mantiene a
temperatura ambiente bajo agitación suave en agitador magnético.
Fórmula a utilizar para el ajuste:
vol final = conc inicial * vol inicial /250.000 cel/ml
INACTIVACION DE LAS MUESTRAS
Las muestras de suero, deben ser inactivadas, previo a su siembra, en baño a 56
± 3°C, durante 30 ± 5 minutos.
PREPARACION DEL MEDIO DE TRABAJO
El medio de dilución de las muestras y del virus, se prepara a partir del MEM-E
+ 1% de ATB + 2% de SFB.
ENSAYO DE SERONEUTRALIZACION SUERO VARIABLE-VIRUS FIJO
• Colocar 75 µI/pocillo de medio en todas las placas a utilizar.
• Diseño de la placa de los sueros problema: Agregar 25µl de la muestra
problema, por cuadruplicado, (Fila A o Fila E pocillos 1-4; 5-8; 9-12,
respectivamente), ver Figura 1.
• Se comienza desde una dilución mínima de 1/4 que sumado al volumen de virus y
células queda en una dilución inicial de 1/8.
• Incluir en forma aleatoria entre las muestras a analizar estándares de título
conocido.
• Diseño de la placa control: Se colocan los sueros control positivo y negativo
del mismo modo que las muestras. Para realizar el control de células se colocan
150µl de medio de trabajo por cuadruplicado en cuatro filas (DIECISEIS (16)
pocillos totales). Para el control de las 100 DICT de virus, se realizan TRES
(3) diluciones en base 10 a partir de la dilución de trabajo. Se siembran 100µl
por cuadruplicado de las 4 diluciones preparadas (ver Figura 2).
• Realizar diluciones en base 4, pasando 25µl, descartando los últimos 25µl
para todas las muestras y sueros controles.
• Se realiza un control de toxicidad de cada muestra colocando 75µl de medio en
otra placa.
• Preparar la dilución de trabajo de virus (100 DICT) en el medio de trabajo.
Preparar el volumen necesario para todas las placas del ensayo considerando que
se necesitan 8 ml de virus por placa.
• Una vez preparada la dilución de trabajo del virus, se deben realizar tres
diluciones en base 10 (-1, -2 y -3) de la misma. Para ello colocar 900µl de medio en tres tubos de 1.8 ml (1-2-3). Agregar 100µl de la
suspensión de virus de trabajo en el tubo 1: (dil -1 ó 1/10), sin tocar el
medio con el tip, homogeneizar por vortex, cambiar el tip, tomar 100µl de esta
dilución y transferir al tubo 2, nuevamente sin que el tip toque el medio, (dil
-2) homogeneizar, descartar el tip y transferir 100µl al tubo 3 (dil -3).
• Colocar 75µl de la dilución de trabajo del virus en todas las placas, excepto
en la placa de controles de toxicidad, en el control de células y en el control
de 100 DICT.
• En la última placa colocar donde se colocaron los controles de suero positivo
y negativo, incluir la titulación del virus de trabajo para verificar que
contenga las 100 UFF. Para ello colocar 4 réplicas de 75µl de cada dilución
(tubos 1, 2 y 3), comenzando de la más diluida a la más concentrada -3, -2, -1,
puro (ver diseño de placa control).
• Incubar las placas (mezcla suero-virus) durante 1 hora a 37 ± 1°C en atmósfera de CO2 al 5 ± 1 %.
• Agregar sobre la mezcla suero-virus 100µl por pocillo, de la suspensión
celular conteniendo 250.000 cel./ml en todas las placas.
• Incubar las placas a 37 ± 1°C en atmósfera de CO2 al 5 ± 1 %, durante 48-72
hs.
LECTURA E INTERPRETACION
LECTURA
- Al cabo de las 48-72 hs. la lectura se realiza por inspección de las
monocapas al microscopio óptico.
- La lectura es por observación de efecto citopático. Se considera positivo
aquel pocillo que presente un foco de CPE característico de VDVB. En los
controles de toxicidad se debe observar la monocapa igual que los controles de
células.
ACEPTACION DEL ENSAYO (CONFORMIDAD)
El ensayo se considera conforme cuando:
1. Las monocapas de los controles de células se encuentran en buen estado (MC
confluentes, células refriengentes, sin alteraciones morfológicas, sin rastros
de contaminación y sin CPE de VDVB).
2. El título de la suspensión viral debe contener 100 DICT 50, con un rango
admitido entre 50-150 DICT, ver Tabla 1.
3. El control positivo debe dar el título esperado ± 1 pocillo. Ejemplo:
2.30< 2.4 <2.50
4. El control negativo debe dar negativo. Se le coloca un valor arbitrario de
0.6 para los cálculos.


INTERPRETACION
El título neutralizante del suero analizado se obtiene según la cantidad de
replicadas protegidas en las diluciones seriadas en base al método de
interpolación de Reed y Muench.
Tabla 2. Titulación de Ac en microplacas (log 10)
|
Pocillos Protegidos
|
1/8
|
1/32
|
1/128
|
1/512
|
1/2048
|
1/8192
|
1/32768
|
1/131072
|
|
1
|
0.70
|
1.30
|
1.90
|
2.50
|
3.10
|
3.70
|
4.30
|
4.90
|
|
2
|
0.90
|
1.50
|
2.10
|
2.70
|
3.30
|
3.90
|
4.50
|
5.10
|
|
3
|
1.10
|
1.70
|
2.30
|
2.90
|
3.90
|
4.10
|
4.70
|
5.30
|
|
4
|
1.20
|
1.80
|
2.40
|
3.00
|
4.10
|
4.20
|
4.80
|
5.40
|