Disposición 3185-1999-ANMAT
Apruébanse las recomendaciones técnicas
contenidas en el documento "Cronograma para exigencias de estudios de
equivalencia entre medicamentos de riesgo sanitario significativo".
Bs. As., 25/6/99
VISTO la Ley 24.766, el Decreto 150/92 modificado
por los Decretos 1890/92 y 177/93, la Resolución Conjunta
988/92 (M.E. y O. y S.P.) y 748/92 (M.S. y A.S.), y
el Expediente Nº 1-47-11003/98-8 del registro de esta
Administración Nacional y;
CONSIDERANDO:
Que las precitadas normas, y las disposiciones
complementarias dictadas en su consecuencia, constituyen el ordenamiento legal
aplicable a la aprobación, registro y autorización de venta de las
especialidades medicinales cuya elaboración, importación y comercialización en
el país se desarrolla al amparo de los preceptos generales establecidos por la
Ley 16.463.
Que quedó consolidado así un sistema
fiscalizador de la actividad con el objetivo primario de garantizar que en la
elaboración e importación de especialidades medicinales la eficacia, seguridad
y calidad de los productos quedará plenamente certificada de acuerdo con
estándares internacionales, mediante su registro ante la autoridad sanitaria
nacional.
Que el actual desarrollo de esos estándares
torna necesaria la adopción de lineamientos técnicos que posibiliten mantener
el nivel de fiscalización en los mismos parámetros internacionales con que el
sistema fue configurado.
Que con tal propósito corresponde adoptar
para la fiscalización de especialidades medicinales en nuestro país exigencias
de estudios de equivalencia, respecto de aquellos principios activos que en
países de alta vigilancia sanitaria son sometidos a tales estudios y que, por
su indicación terapéutica y condiciones de seguridad en el uso, deben ser
consideradas como sustancias de riesgo sanitario ponderable.
Que el grado de desarrollo alcanzado
actualmente por el sistema fiscalizador de nuestro país incluye el diseño de
los protocolos de investigación de ensayos clínicos cuyos requisitos están
impuestos por la
Disposición Nº
5330-ANMAT-97, encontrándose allí descriptos los procedimientos de buenas
prácticas de investigación en estudios de farmacología clínica sobre los que
pueden vehiculizarse las exigencias de estudios de bioequivlaencia "in vivo".
Que han tomado la intervención de su
competencia la comisión técnica ad-hoc conformada con
representantes de las áreas técnicas del organismo y la Dirección de Asuntos
Jurídicos.
Que se actúa en virtud de las facultades
conferidas por el Decreto 1490/92.
Por ello;
EL DIRECTOR NACIONAL DE LA ADMINISTRACION NACIONAL
DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MEDICA
DISPONE:
Artículo 1º — Apruébanse las recomendaciones técnicas para la
realización de estudios de equivalencia contenidas en el documento:
"Cronograma para exigencia de estudios de equivalencia entre medicamentos
de riesgo sanitario significativo" cuyo texto se reproduce como Anexo I de
la presente
Disposición formando parte de la misma.
Art. 2º — La implementación de la exigencia de estudios de equivalencia se
realizará de acuerdo con el cronograma operativo incluido en el documento
aprobado por el artículo precedente.
Art. 4º — Regístrese; dése a la Dirección Nacional
del Registro Oficial para su publicación en el Boletín Oficial. Cumplido,
archívese PERMANENTE. — Pablo M. Bazerque.
(Nota: por art.
1° de la Disposición 4132-2012 de la Administración Nacional
de Medicamentos, Alimentos y Tecnología Médica B.O.
24/07/2012 se incorpora a la exigencia de demostración de bioequivalencia
establecida en la
presente Disposición, a todas las concentraciones
comercializadas y/o a comercializarse de una especialidad medicinal, de forma
farmacéutica sólida oral, que contenga alguno de los Ingredientes Farmacéuticos
Activos incluidos en la normativa nacional mencionada en el VISTO de la norma
de referencia, y en disposiciones complementarias posteriores de exigencia de
bioequivalencia. Vigencia: a partir del día siguiente al de su publicación en
el Boletín Oficial)
(Nota: por art.
1° de la Disposición 3113-2010 de la Administración Nacional
de Medicamentos, Alimentos y Tecnología Médica B.O.
6/7/2010 se incorporan a la exigencia de realización de estudios de
Bioequivalencia / Biodisponibilidad, establecidos por la presente Disposición,
a los ingredientes farmacéuticos activos Lamotrigina
y Topiramato. Vigencia: a partir del día siguiente al
de su publicación en el Boletín Oficial)
(Nota: Por art.
1° de la Disposición 2446-2007 de la Administración Nacional
de Medicamentos, Alimentos y Tecnología Médica B.O.
30/4/2007, se incorpora a la exigencia de realización de estudios de
bioequivalencia / biodisponibilidad establecidos en la presente Disposición,
a los principios activos Serolimus, Everolimus, Tacrolimus y Micofenolato. Vigencia: a partir del día siguiente al de su
publicación en el Boletín Oficial.)
(Nota: Por art.
1° de la Disposición 2807-2002 de la Administración Nacional
de Medicamentos, Alimentos y Tecnología Médica B.O.
21/6/2002, se incorpora a la exigencia de realización de estudios de
bioequivalencia / biodisponibilidad establecidos en la presente Disposición,
al principio activo ISOTRETINOINA para uso oral. Vigencia: a partir del día
siguiente al de su publicación en el Boletín Oficial.)
CONTENIDO
CRONOGRAMA PARA EXIGENCIA DE ESTUDIOS DE
EQUIVALENCIA ENTRE MEDICAMENTOS CON RIESGO SANITARIO SIGNIFICATIVO
II) GUIA PARA LA REALIZACION DE ESTUDIOS
DE EQUIVALENCIA ENTRE MEDICAMENTOS CON RIESGO SANITARIO SIGNIFICATIVO
I-OBJETIVO
II-DEFINICIONES
Biodisponibilidad
III-DEMOSTRACION DE EQUIVALENCIA
TERAPEUTICA ENTRE MEDICAMENTOS CON RIESGO SANITARIO SIGNIFICATIVO
IV-REQUERIMIENTOS PARA LA REALIZACION DE ESTUDIOS
DE EQUIVALENCIA EN SERES HUMANOS
II) OBJETIVOS DEL PROYECTO
I-OBJETIVO GENERAL
II-OBJETIVOS INTERMEDIOS
III) CRITERIOS PRELIMINARES PARA
IMPLEMENTAR UN CRONOGRAMA PARA MEDICAMENTOS CON RIESGO SANITARIO SIGNIFICATIVO
QUE REQUIERAN ESTUDIOS DE EQUIVALENCIA
I-CATEGORIAS DE RIESGO SANITARIO
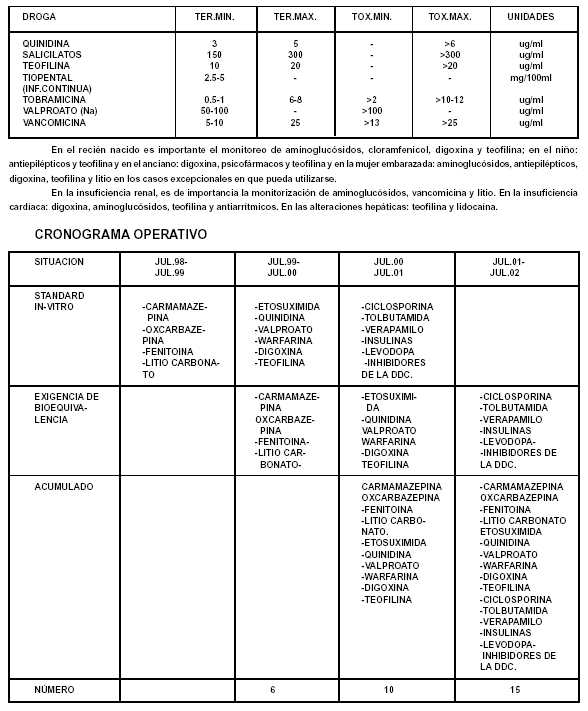
II-DROGAS ORDENADAS POR FORMA FARMACEUTICA
Y POR RIESGO.
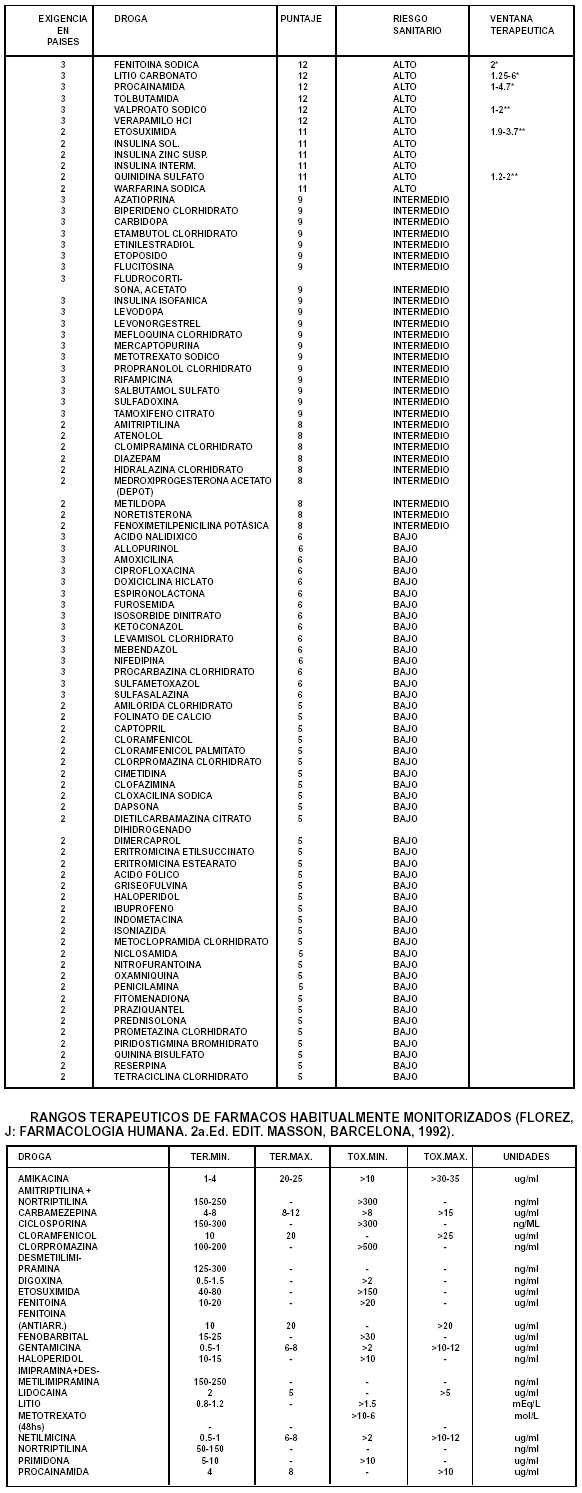
III-DROGAS ORDENADAS POR EXIGENCIA, RIESGO
Y VENTANA TERAPEUTICA.
ANEXO
I
CRONOGRAMA
PARA EXIGENCIA DE ESTUDIOS DE EQUIVALENCIA ENTRE MEDICAMENTOS CON ALTO RIESGO
SANITARIO.
CRONOGRAMA
PARA EXIGENCIA DE ESTUDIOS DE EQUIVALENCIA ENTRE MEDICAMENTOS CON RIESGO
SANITARIO SIGNIFICATIVO.
I.- GUIA PARA LA REALIZACION DE ESTUDIOS
DE EQUIVALENCIA ENTRE MEDICAMENTOS CON RIESGO SANITARIO SIGNIFICATIVO.
I.- OBJETIVO
El objetivo de esta guía es establecer
recomendaciones técnicas sobre la realización de estudios de equivalencia entre
medicamentos de riesgo sanitario significativo en concordancia con las pautas
internacionalmente vigentes.
II.- DEFINICIONES
A los efectos del presente documento se
adoptan las siguientes definiciones:
BIODISPONIBILIDAD
Es la cantidad y velocidad con las que el
principio activo contenido en una forma farmacéutica alcanza la circulación
sistémica, determinadas mediante la curva concentración/tiempo o la excreción
urinaria. (OMS 1996).
BIOEQUIVALENCIA
Dos especialidades medicinales son bioequivalentes cuando siendo equivalentes farmacéuticos o
alternativas farmacéuticas sus biodisponibilidades
después de la administración en la misma dosis molar son semejantes en tal
grado, que pueda esperarse que sus efectos sean esencialmente los mismos. (OMS
1996).
EQUIVALENCIA
Dos productos farmacéuticos son equivalentes
cuando son farmacéuticamente equivalentes y después
de administrados en la misma dosis molar sus efectos, con respecto a eficacia y
seguridad, son esencialmente los mismos (MERCOSUR) (Ver EQUIVALENCIA
TERAPEUTICA, OMS)
EQUIVALENTE FARMACEUTICO
Dos especialidades medicinales son
equivalentes farmacéuticos si contienen la misma cantidad de principio activo,
en la misma forma farmacéutica, están destinados a ser administrados por la
misma vía y cumplen con estándares de calidad idénticos o comparables. Sin
embargo, la equivalencia farmacéutica no necesariamente implica equivalencia
terapéutica ya que diferencias en los excipientes, en el proceso de
elaboración, u otras pueden determinar disparidades en el comportamiento de los
productos. (OMS).
EQUIVALENCIA TERAPEUTICA
Dos especialidades medicinales son
equivalentes terapéuticos cuando siendo alternativas o equivalentes
farmacéuticos y después de la administración en la misma dosis molar sus
efectos con respecto a la eficacia y seguridad resultan esencialmente los
mismos, luego de estudios apropiados (de bioequivalencia, farmacodinámicos,
clínicos o in-vitro). (OMS).
ALTERNATIVA FARMACEUTICA
Productos que dentro del concepto de producto
similar:
a) Contiene el mismo principio terapéutico,
siendo diferente la salificación, esterificación o complejación
del mismo, o
b) Se presentan en diferentes formas farmacéuticas
o concentraciones por unidad de administración, poseyendo la misma vía de
administración, la misma indicación terapéutica y la misma posología (CPM,
12/1998).
PRODUCTO DE REFERENCIA
Producto para el cual la eficacia y seguridad
han sido establecidas. Cuando el producto innovador no se encuentre disponible,
el líder del mercado puede ser utilizado como producto de referencia (OMS,
1996), o el que determine la autoridad sanitaria para cada caso.
PRODUCTO SIMILAR
A los fines de la presente norma se entiende
como tal al producto que contiene la(s) misma(s) sustancia(s) terapéuticamente
activas como base de su formulación, así como formas farmacéuticas, vías de
administración, posología, indicaciones, contraindicaciones, precauciones,
advertencias, reacciones adversas, pruebas de disolución y otros datos
correlativos semejantes al producto registrado en el país o países de los
Anexos correspondientes, pudiendo diferir en características tales como tamaño
y forma, excipientes, período de vida útil, envase primario.
III.- DEMOSTRACION DE EQUIVALENCIA
TERAPEUTICA ENTRE MEDICAMENTOS CON RIESGO SANITARIO SIGNIFICATIVO
1.- GENERALIDADES
Una vez cumplimentadas las buenas prácticas
de manufactura y control de calidad, para la demostración de equivalencia terapéutica
los métodos y muestras experimentales considerados por
orden decreciente de seguridad, sensibilidad y reproducibilidad son:
1.1. Estudios de bioequivalencia (Estudios Farmacocinéticos):
1.1.1. Determinación de la concentración del
principio activo o sus metabolitos en sangre total, plasma, suero o en otro
fluido biológico en función del tiempo o;
1.1.2. Determinación de la excreción urinaria
del principio activo o sus metabolitos en función del tiempo.
1.2. Estudios farmacodinámicos
"agudos"
1.2.1. Determinación de un efecto
farmacológico agudo producido por el producto problema y de referencia o sus
metabolitos en función del tiempo si dicho efecto puede ser determinado con
suficiente seguridad, sensibilidad y reproducibilidad. Esta metodología puede
ser aplicable cuando no existan métodos disponibles para la determinación de
los productos problema y de referencia en los fluidos biológicos o excretorios.
1.3. Ensayos clínicos comparativos.
1.4. Ensayos de disolución "in vitro".
1.4.1. Prueba/s de disolución u otras,
correlacionadas o no con estudios de biodisponibilidad, pero que se hallan
descriptas en las farmacopeas reconocidas internacionalmente o en la
bibliografía científica con evidencias suficientes de validación.
1.4.2. Prueba/s realizadas mediante métodos
(que produzcan resultados correlacionados con estudios en seres humanos, para
medicamentos con riesgo sanitario significativo), con evidencias suficientes de
validación.
1.4.3.- Indicadores básicos: Tiempo de
disolución de una determinada cantidad de principio activo; cantidad de
principio activo disuelto en un tiempo determinado, en medio o medios que se
hallen correlacionados con el empleo terapéutico del producto terminado.
2.- APLICACION DE LOS ESTUDIOS DE
EQUIVALENCIA ENTRE MEDICAMENTOS CON RIESGO SANITARIO SIGNIFICATIVO
2.1.- NO REQUIEREN ESTUDIOS DE
EQUIVALENCIA
2.1.1. Productos destinados a ser
administrados parenteralmente (por ejemplo: vías
intravenosa, intramuscular o intratecal) en
soluciones acussas que contengan el/los mismo/s
principio/s activo/s en la/s misma/s concentración/es (OMS, 1996).
2.1.2. Soluciones para utilización por vía
oral que contengan el/los mismo/s principios/s activo/s en la /s misma/s
concentraciones y no contengan un excipiente que se conozca o se sospeche que
afecta el tránsito gastrointestinal o la absorción del principio activo (OMS,
1996).
2.1.3. Gases o vapores (Res. 3784/91; OMS,
1996).
2.1.4. Polvos y/o granulados para
reconstitución como solución, cuando cumpla con los puntos 2.1.1. y 2.1.2.
2.1.5. Productos otológicos u oftalmológicos
que contengan el/los mismo/s principio/s activo/s en la/s misma/s
concentración/es y esencialmente los mismos excipientes (OMS, 1996).
2.1.6. Productos para empleo tópico,
líquidos, que contengan el/los mismos/s principio/s activo/s y esencialmente
el/los mismo/s excipiente/s (OMS,1996).
2.1.7. Formas farmacéuticas de aplicación
tópica (crema, pomada, gel, etc.), de uso externo, sólidas, que contengan
el/los mismos/s principio/s activo/s y esencialmente el/los mismo/s
excipiente/s.
2.1.8. Productos destinados a ser utilizados
por inhalación o aerosoles nasales que sean administrados con o sin
esencialmente el mismo dispositivo, sean preparados como soluciones acuosas y
que contengan el/los mismos/s principio/s activo/s y esencialmente el/los
mismo/s excipiente/s en concentraciones comparables (OMS, 1996).
2.1.9. Productos conteniendo principios
activos de administración oral que no deban absorberse (Res. 3784/91).
Se considera "Esencialmente los mismos
excipientes" a excipientes del mismo tipo en cuanto a que posean la misma
función en la formulación (dispersante, agregante,
espesante, etc.), aunque no se trate de la misma molécula.
3.- REQUIEREN SOLAMENTE ESTUDIOS DE
EQUIVALENCIA "IN-VITRO"
3.1. Comprimido de liberación simple.
3.2. Cápsula de liberación simple.
3.3. Diferentes concentraciones de un
producto cuando:
3.3.1.-La composición cualitativa de las
diferentes concentraciones es esencialmente la misma;
3.3.2.-La relación principio
activo-excipiente, para las diferentes concentraciones es esencialmente la
misma o para concentraciones bajas la relación entre los excipientes es la
misma;
3.3.3.- Se ha realizado un estudio apropiado
de equivalencia para al menos una de las concentraciones de la formulación
(usualmente la concentración mayor, a menos que se haya elegido la
concentración menor por razones de seguridad);
3.3.4.-En el caso que la disponibilidad
sistémica, haya demostrado una farmacocinética lineal dentro del rango
terapéutico.
De acuerdo a normas de la Unión Europea, serán
excepción a los estudios "In-vivo" cuando se haya demostrado una
aceptable correlación entre la tasa de disolución "In-vivo" e
"In-vitro" y la tasa de disolución
"In-vitro" del nuevo medicamento sea
equivalente a la del medicamento ya autorizado, en las mismas condiciones de
prueba utilizadas para establecer la correlación.
4.- REQUIEREN ESTUDIOS DE EQUIVALENCIA
"IN-VITRO" E "IN VIVO" (de bioequivalencia, farmacodinámico
o ensayo clínico controlado).
Para los medicamentos con riesgo sanitario
significativo se procederá a la realización de estudios "In-vivo" en
las siguientes situaciones:
4.1.-Formas farmacéuticas de liberación
modificada controlada, sostenida , programada, etc.
4.2. Sistemas terapéuticos.
4.3.- Formas farmacéuticas de liberación
simple que contengan principios activos que reúnan una o más de las siguientes
características:
4.3.1.- Propiedades fisicoquímicas
desfavorables:
- Escasa solubilidad en agua (menor a 0,1%).
- Variaciones cristalográficas metaestables.
- Baja humectabilidad.
4.3.2- Características farmacocinéticas:
- Farmacocinética No Lineal en todo el rango
terapéutico (de orden 0, no proporcional o dosis dependiente).
- Escasa tasa de absorción (menor del 30%).
- Estrecha ventana terapéutica
: definiéndose la misma como:
a) El cociente entre la Dosis letal media
(DL50) y la Dosis eficaz media (DE50), es menor de 2.
b) El cociente entre la concentración tóxica
mínima y la concentración eficaz mínima es menor de 2.
c) El uso eficaz y seguro de las especialidades
que contienen la droga en cuestión, requiere cuidadosa dosificación y monitoreo
del paciente.
- Elevado metabolismo de primer pasaje
hepático (mayor del 70%).
4.3.3.- Características farmacodinámicas
- Curva Dosis-Respuesta "empinada" (es
decir, pequeños cambios en la dosis determinan impor-tantes variaciones en los efectos).
- Estrecho margen de seguridad (cociente
DL50/DE50, menor a 2).
4.3.4.- Características clínicas
- Evidencia clínica de problemas relacionados
con la biodisponibilidad.
IV.- REQUERIMIENTOS PARA LA REALIZACION DE ESTUDIOS
DE EQUIVALENCIA EN SERES HUMANOS.
1.-GENERALIDADES
De acuerdo a lo establecido en la Disposición
5330/97 (Ensayos Clínicos), o la que en su caso la reemplace, en lo que se
refiere a:
-Ambito de aplicación
y de sus alcances.
-Autorización, seguimiento y controles del
estudio.
-Requisitos de los investigadores y de los
patrocinantes.
-Incumplimiento de la normativa.
-Los requisitos básicos.
-Los centros en donde se llevará a cabo el
estudio.
-Los requerimientos éticos.
2.- INFORMACION SOBRE LOS PRODUCTOS
UTILIZADOS EN EL ESTUDIO.
2.1. Las características
farmacocinéticas/dinámicas del producto de referencia y la forma farmacéutica a
utilizar en el ensayo y del producto problema si las hubiera. No será imprescindible
la presentación de información preclínica para los estudios de bioequivalencia
(Disp. 5330/97, Capítulo VII, Introducción).
2.2. La composición cualicuantitativa
del producto problema. El contenido de droga activa del producto problema con
respecto al producto de referencia no debe diferir en más de un 5%. Si ello
ocurriera, esta diferencia debe ser tenida en cuenta en el cálculo de los datos
de biodisponibilidad para facilitar la comparación de ambos productos
farmacéuticos.
2.3. Los test de disolución "in vitro" comparativos entre el lote del producto de
referencia y problema que serán utilizados en el ensayo o el test "in vitro" que corresponda según la forma farmacéutica a
utilizar durante el ensayo.
2.4. Drogas
2.4.1. Productos de referencia y en estudio:
Nombre aprobado. Nombre comercial. Fabricante. Forma farmacéutica. Dosis.
Número de lote.
2.4.2. Provisión, almacenamiento y
dispensación.
2.4.3. Acondicionamiento, etiquetado y
aleatorización.
2.5. (Punto derogado por art. 5° de la Disposición 1263-2012 de la Administración Nacional
de Medicamentos, Alimentos y Tecnología Médica B.O.
8/3/2012)
2.6. Reserva de muestras: se debe guardar cantidad suficiente de cada
lote bajo condiciones de almacenamiento apropiadas de los productos
farmacéuticos utilizados de los estudios de equivalencia en seres humanos, así
como sus protocolos de análisis y características. Estas muestras podrán ser
requeridas por las autoridades en caso de ser necesario.
3.- SUJETOS
3.1. Ensayo de bioequivalencia:
Los participantes deberán ser preferiblemente
voluntarios sanos de ambos sexos entre 18 a 55 años de edad y de peso acorde a los
rangos aceptados. No deben tener antecedentes de abuso de drogas o alcohol y
ser no-fumadores. Se establecerán criterios de inclusión / exclusión, de
acuerdo a las características de los productos en estudio. Se confeccionarán
historias clínicas detalladas las cuales incluirán: exámenes físico y de laboratorio.
Si el estudio fuera realizado en pacientes
esta alternativa deberá ser justificada.
Los participantes serán monitoreados durante
y con posterioridad al desarrollo del estudio con el objeto de tomar las
medidas adecuadas en caso de aparición de reacciones adversas, toxicidad o
alguna enfermedad intercurrente.
Tamaño de la muestra: De 18 a 24 voluntarios sanos y en
ningún caso menor de 12. El número de sujetos participantes deberá ser
justificado.
3.2. Ensayo farmacodinámico:
Seguirán los mismos lineamientos que para los
ensayos de bioequivalencia anteriormente descriptos y podrán participar tanto
voluntarios sanos como pacientes.
3.3. Ensayo clínico comparativo:
Seguirán los lineamientos establecidos en la
Disposición 5330/97, o la que en su caso la reemplace, siendo habitualmente el
número de pacientes participantes mucho mayor a los requeridos para los
estudios de bioequivalencia
El número de sujetos participantes deberá
justificarse.
4.- PRODUCTO DE REFERENCIA Y EN ESTUDIO
4.1. Producto de referencia (Ver II.-
DEFINICIONES).
4.2. Producto problema: Es la alternativa
farmacéutica o el equivalente farmacéutico del producto de referencia.
5.- METODOS ANALITICOS.
5.1.- Ensayo de bioequivalencia.
Los métodos analíticos usados para determinar
el principio activo y/o sus productos de biotransformación en plasma, suero,
sangre u orina u otro fluido biológico deberán cumplimentar los requerimientos
de especificidad, sensibilidad, precisión y seguridad.
Se deberán informar los resultados de
validación de los procedimientos a utilizar en el ensayo (p.e.:
curva standard, límite de detección del principio
activo y/o de su producto de biotransformación).
Se deberán informar los resultados de los
ensayos de estabilidad del principio activo y/o de su producto de
biotransformación en la muestra experimental.
5.2.- Ensayo farmacodinámico.
La metodología utilizada para determinar el
efecto farmacológico o terapéutico relevante deberá cumplimentar los
requerimientos de especificidad, sensibilidad, precisión y seguridad. Dichos
métodos incluyen: registros de los eventos mediante instrumental adecuado o
escalas analógicas visuales o categorización cualitativa de los datos.
5.3.- Ensayo clínico comparativo.
La metodología utilizada comprenderá todos aquellos
procedimientos clínicos adecuados que permitan determinar el comienzo y la
intensidad del efecto terapéutico relevante según Disposición 5330/97 o la que
en su caso la reemplace.
6.- DISEÑO EXPERIMENTAL
6.1. Dosis única del producto problema y de referencia:
6.1.1.Generalidades:
- Realizado en voluntarios sanos que
recibirán una única dosis tanto del producto problema como de referencia.
-El producto problema y de referencia deberá
ser administrado a sujetos en ayunas, a menos que otro método puede ser más
apropiado el cual deberá justificarse.
-El diseño será cruzado, a menos que un
diseño paralelo o de otro tipo resulte más apropiado el cual deberá
justificarse.
-A menos que otras razones lo justifiquen el
período de eliminación deberá ser determinado durante:
a- Por lo menos tres veces la vida media del
principio activo o su metabolito en sangre o en orina; o
b- Por lo menos tres veces la vida media de
desaparición del efecto farmacológico agudo.
6.1.2. Según la muestra experimental:
-Sangre
a- La colección de las muestras sanguíneas
serán realizadas con la suficiente frecuencia para permitir la determinación:
a.1. De la concentración máxima.
a.2. El área bajo la curva por un periodo de
tiempo de por lo menos tres veces la vida media del principio activo o su
metabolito.
b- Según la forma farmacéutica:
b.1. En un estudio en que se comparen las
formas orales del producto problema y de referencia la periodicidad de la
colección de las muestras debe ser idéntica.
- Orina
Cuando la comparación del producto problema y
de referencia se basa en la determinación de una curva acumulativa de excreción
urinaria en función de tiempo la colección de las muestras de orina deberá
realizarse con la suficiente frecuencia para permitir la determinación de la velocidad
y cantidad excretada de la droga o sus metabolismos.
6.2. Efecto farmacológico agudo
6.2.1. Cuando la comparación del producto
problema y de referencia se basa en la determinación de un efecto farmacológico
agudo en función del tiempo, las determinaciones de estos efectos deberán ser
realizadas con la suficiente frecuencia para permitir una razonable estimación
del área bajo la curva por un periodo de tiempo de por lo menos tres veces la
vida media de desaparición del efecto farmacológico, la respuesta máxima y el
tiempo en que esa respuesta máxima se manifiesta.
6.2.2. El uso de un efecto farmacológico
agudo para la determinación de la equivalencia puede requerir la realización de
una curva dosis-respuesta, en tales casos la equivalencia puede ser determinada
por comparación de la curva dosis-respuesta como así también del área bajo la
curva en función del tiempo para una dosis determinada.
6.3. Dosis múltiples del producto problema y
de referencia:
6.3.1. Generalidades
En determinadas circunstancias la comparación
del producto problema y de referencia requerirá la administración repetida de
los mismos con el objeto de obtener niveles estacionarios del principio activo
en el organismo.
6.3.2. Condiciones para la realización de
ensayos de bioequivalencia con dosis múltiple en medicamentos con riesgo
sanitario significativo.
Se requerirá un estudio empleando dosis
múltiples cuando:
- Existan diferencias en la velocidad de
absorción pero no en la cantidad absorbida.
- Haya una excesiva variabilidad en la biodisponibilidad
entre sujetos.
- La concentración del principio activo o sus
metabolismos en sangre resultante de la administración de una única dosis se
encuentran por debajo de los límites de detección del método analítico.
- El producto problema es una forma de
liberación controlada.
- Farmacocinética dosis o tiempo-dependiente.
6.3.3. Diseño experimental
- Será realizado en voluntarios sanos que
recibirán dosis múltiples tanto del producto problema como de referencia.
- El producto problema y de referencia deberá
ser administrado a sujetos en ayunas, a menos que otro método pueda ser más
apropiado el cual deberá justificarse.
- El producto problema y de referencia deberá
ser administrado de acuerdo a las recomendaciones usuales de posología.
- El diseño será cruzado, a menos que un
diseño paralelo o de otro tipo resulte más apropiado por razones científicas
válidas y deberá prever un período adecuado de eliminación de la droga si las
condiciones de equilibrio no se alcanzan.
- A menos que otras razones lo justifiquen el
período de eliminación deberá ser determinado durante:
a- Por lo menos cinco veces la vida media del
principio activo o su metabolito en sangre o en orina; o
b- Por lo menos cinco veces la vida media de
desaparición del efecto farmacológico agudo.
6.3.4. Según la muestra experimental
-Para el ensayo de dosis múltiple:
a-Sangre y Orina: Cuando la comparación entre
la droga problema y de referencia se base en curvas de concentración sanguínea o
en curvas acumulativas de excreción urinaria en función del tiempo en estado de
equilibrio las muestras de sangre u orina deberán ser tomadas con la suficiente
frecuencia durante dos o más días consecutivos para definir adecuadamente la
concentración plástica o urinaria máxima y mínima en equilibrio.
-Para el efecto farmacológico agudo:
Cuando la comparación entre la droga problema
y de referencia se base en la determinación de una curva efecto-tiempo las
mediciones de dicho efecto serán lo suficientemente frecuentes para demostrar
un efecto máximo y ausencia de diferencias significativas entre ambos
productos.
7.- VARIABLES FARMACOCINETICAS:
Según el diseño experimental y las muestras
biológicas: Cmax, Cmaxx, Cmaxr, Cmin, Cp,
Tmax, ABCt, ABC¥, ABCt, ABCx,
ABCr TMR, Aet, Ae¥, dAe / dt,
t 1/2.
Cmax: Concentración plasmática máxima.
Cmaxx: Concentración plasmática máxima del producto
problema.
Cmaxr: Concentración plasmática máxima del producto de
referencia.
Cmin: Concentración plasmática mínima.
Cp : Concentración plasmática promedio.
Tmax: tiempo en el cual se alcanza la Cmax.
ABCt: área bajo la curva de concentración plasmática en un
tiempo t.
ABC¥: área bajo la curva de concentración plasmática
extrapolada al infinito.
ABCt: área bajo la curva de concentración plasmática
durante un intervalo de dosis en estado deequilibrio.
ABCx: área bajo la curva del producto problema
ABCr: área bajo la curva del producto de referencia
TMR: tiempo medio de residencia.
Aet: excreción urinaria acumulativa a un tiempo t.
Ae¥: excreción urinaria acumulativa extrapolada al
infinito.
dAe / dt: velocidad de
excreción urinaria.
t1/2: vida media de concentración plasmática.
8.- ANALISIS ESTADISTICO.
Serán aceptados aquellos procedimientos
estadísticos que no excedan el nivel de significancia del 5% y entre ellos
aquellos con el menor riesgo de rechazar erróneamente equivalencia.
Podrán ser utilizados métodos paramétricos o no paramétricos
según corresponda.
9.- CRITERIOS DE EQUIVALENCIA:
9.1. Para Bioequivalencia:
ABCx / ABCr: El intervalo de
confianza 90% de la razón entre ambas ABC deberá estar contenido dentro de
rango de bioequivalencia de 0.8 - 1.25.
Cmax x / Cmax r : Debido a la variabilidad de este parámetro
los rangos serán más amplios que para la razón ABC, la elección del rango deberá ser
justificada.
El cálculo de cualquier otra variable
utilizada para declarar dos productos bioequivalentes
deberá ser justificada.
9.2. Para ensayo farmacodinámico agudo:
Debe tenerse en cuenta que los intervalos utilizados
en los ensayos de bioequivalencia son habitualmente muy amplios como para ser
aplicados a este tipo de ensayos, por esta razón deberán ser definidos caso por
caso y descriptos en el protocolo.
9.3. Para ensayos clínicos comparativos
De acuerdo a lo establecido en la Disposición
5330/97 o la que en su caso la reemplace.
II.- OBJETIVOS DEL PROYECTO
I.- OBJETIVO GENERAL:
Establecer un cronograma para la exigencia
progresiva de estudios de bioequivalencia para medicamentos o especialidades
medicinales similares.
II.- OBJETIVOS INTERMEDIOS:
1. Fijar criterios de selección de principios
activos a los cuales se les exigirá estudios de bioequivalencia.
2. Establecer standard
"In-vitro" para los principios activos
seleccionados, necesariamente previos a la exigencia de estudios de
Bioequivalencia.
El establecimiento del objetivo 2.2. encuentra su fundamentación en el hecho que es necesario
establecer un standard "In-vitro",
previo a la realización de estudios "In-vivo", a los efectos de
controlar las variables dependientes del medicamento, previas a la
administración "In-vivo".
III.-CRITERIOS PRELIMINARES PARA
IMPLEMENTAR UN CRONOGRAMA PARA MEDICAMENTOS CON RIESGO SANITARIO SIGNIFICATIVO
QUE REQUIERAN ESTUDIOS DE EQUIVALENCIA.
Para esta aproximación se partió del
documento: ‘‘WHO EXPERT COMMITTEE ON SPECIFICATIONS FOR PHARMACEUTICAL
PREPARATIONS." WHO Technical Report
Series Nº 863, Geneva,1996, del cual se extrajo de la tabla 1, pág. 142: "Examples of national requierments
studies".
En primer lugar se procedió a ensillar las
drogas que Canadá, Alemania y EE.UU. coinciden en que deben ser sometidas a
estudios de bioequivalencia, es decir, que las tres autoridades sanitarias
están contestes en que deben ser estudiadas in-vivo (categorización +b de la
tabla referida).
Posteriormente se clasificaron las drogas de
acuerdo al Riesgo Sanitario, tomando para la fijación del mismo, dos aspectos:
a.- Terapéutico: principios activos
utilizados en desórdenes serios ya sea porque ponen en peligro la vida (por ejemplo
algunos antiarrítmicos) o porque poseen complicaciones graves (por ejemplo
algunos antiepilépticos).
b.- Seguridad: principios activos que poseen
una estrecha relación entre su concentración máxima efectiva no tóxica y su
concentración mínima efectiva (por ejemplo las sales de litio o los preparados
de teofilina).
Luego se enlistaron las drogas con las que
poseen acuerdo 2 de los países de alta vigilancia sanitaria (EE.UU., Canadá y
Alemania), y dentro de estos principios activos, también se procedió a subclasificarlos de acuerdo al Riesgo Sanitario.
CATEGORIAS DE RIESGO SANITARIO
RIESGO SANITARIO ALTO: Es la probabilidad de aparición de complicaciones de
la enfermedad amenazantes para la vida o para la integridad psicofísica de la
persona y/o de reacciones adversas graves (OMS) cuando la concentración
sanguínea de la droga no se encuentra dentro de la ventana terapéutica.
RIESGO SANITARIO INTERMEDIO: Es la probabilidad de aparición de complicaciones de
la enfermedad no amenazantes para la vida o para la integridad psicofísica de
la persona y/o de reacciones adversas no necesariamente graves cuando la
concentración sanguínea de la droga no se encuentra dentro de la ventana
terapéutica.
RIESGO SANITARIO BAJO: Es la probabilidad de aparición de una complicación
menor de la enfermedad y/o de reacciones adversas leves cuando la concentración
sanguínea de la droga no se encuentra dentro de la ventana terapéutica.
Operativamente se asignó un puntaje
ponderado, consistente en lo siguiente:
(RIESGO X 3) + (EXIGENCIA PAIS X 1 )
RIESGO ALTO: 3 PUNTOS
RIESGO INTERMEDIO: 2 PUNTOS
RIESGO BAJO: 1 PUNTO
EXIGENCIA EN 3 PAISES: 3 PUNTOS
EXIGENCIA EN 2 PAISES: 2 PUNTOS

REFERENCIAS BIBLIOGRAFICAS
(1)- CFR. 320.1. 4.01.90.
(2)- FDA Home Page (Internet). 28.08.96.
(3)- Goodman Gilman, L. Las bases
farmacológicas de la terapéutica 8 va Ed. Médica Panamericana. Bs.
As. 1991.
(4)- OMS-OPS: Glosario de términos
especializados para la evaluación de medicamentos. Washington, 1990.
(5)- OMS. Consultative
document. Interchangeable multi-source pharmaceutical
products. 06.12.93.
(6)- WHOth.Technical
Report Series Nº 863. Expert Committee on Specifications for pharmaceutical preparations. 34 th Report.
Geneva,1996.
BIBLIOGRAFIA CONSULTADA
- Cid Cárcamo, E.: Introducción a la Farmacocinética.
Monografía Nº
25. Serie Billoogía. Secretaría General de la
Organización de los Estados Americanos. Programa Regional de Desarrollo
Científico y Tecnológico. Washington, 1982.
- Cid Cárcamo, E.: La cinética de disolución
de medicamentos. Monografía Nº 24. Serie Billoogía. Secretaría General de la Organización de los
Estados Americanos. Programa Regional de Desarrollo Científico y Tecnológico.
Washington, 1981.
- EEC Guidelines investigation of bioavalability and bioequivalence: Rules governing
medicinal products in the
European Community. Vol
III, 159-161(Cit. 5), 1990.
- FDA: Aprove drug products with therapeutic
equivalence evaluation-
11th De., 1991.
-Flórez, J:
Farmacología humana. 2a.Ed. Edit. Masson,
Barcelona, 1992.
- Glasser, AC: Aspects for bioavailability
and bioequivalence revision. Possible implications on clinical pharmacology. Meth. Find. Exptl.
Clin. Pharmacol. 1987, 9,4
49-452 (Cit. 5).
-Goodman Gilman’s
Las bases farmacológicas de la terapéutica. 9a. Ed. Interamericana. México,
1996.
- Greenblat, DJ: et
al.: Bioequivalence of generic drugs in clinical psychopharmacology. J. Clin. Psychopharmacology 1987,
A21-A23 (Cit. 5).
- Iannantuono, R; Tessler, J: Biodisponibilidad y Bioequivalencia. Revista
Argentina de Farmacología Clínica 1994,1,5,226-243.
- Koch-Wesser, J: Bioavailability of drugs (first of
two parts). N. Engl. J. Med. 1974,291,233-237.
- Marzo, A.: Bioequivalence.
Drugs made Germany. 1995,38,1,6-13.
- Noticias Farmacéuticas 1989,10,16-17.
-Steinijans, VW et
al.: Controversies in bioequivalence
studies. Clin. Pharmacokin. 1992, 22, 4,247- 253.
- Stromb, BL: Generic Drug Substitution revisited. N. Engl. J. Med. 1987,316, 1456-1462.
- WHO: Draft guidelines on marketing authorization requierements. Interchangeable multisarcepharmaceutical
products. Consultative document. December 6, 1993.