Resolución C. 19-2010
Oficialízase el método "Determinación de natamicina
en el vino por cromatografía líquida de ultra alta resolución masa/masa".
Mendoza,
31/5/2010
VISTO
el Expediente Nº S93:0002892/2010, del Registro del INSTITUTO NACIONAL DE
VITIVINICULTURA, y
CONSIDERANDO:
Que
por el expediente mencionado en el Visto se tramita la oficialización del
método de determinación de natamicina en vinos por
cromatografía líquida de ultra alta resolución y detección masa - masa.
Que
la adición de natamicina no constituye una práctica
permitida en la
REPUBLICA ARGENTINA, como tampoco en los países miembros de la UNION EUROPEA (UE) y
en otros países vitivinícolas.
Que
su uso tampoco es práctica recomendada por la ORGANIZACION
INTERNACIONAL DE LA
VIÑA Y EL VINO (OIV).
Que
por ello, se hace necesario proceder a su control tanto en los vinos argentinos
como en los importados.
Que
dicha determinación posibilita el control de la aptitud para el consumo de los
vinos en relación a este compuesto por Cromatografía Líquida de Ultra Alta
Resolución.
Que
el INSTITUTO NACIONAL DE VITIVINICULTURA (INV) ha incorporado recientemente
tecnología analítica de última generación para optimizar tal cometido, mediante
la adquisición de un Cromatógrafo Líquido de Ultra Alta Resolución Masa-Masa.
Que
durante el año en curso, se iniciaron las gestiones ante la OIV a los fines de oficializar
el método mediante el cual se establezca un límite de detección de la precitada
sustancia, vinculado a posibles contaminaciones indirectas.
Que
sobre el particular, la
REPUBLICA FEDERAL DE ALEMANIA y el REINO UNIDO, han aceptado
como criterio tecnológico un límite de CINCO MICROGRAMOS POR LITRO (5 µg.L-1).
Que
Subgerencia de Asuntos Jurídicos del INV ha tomado la intervención de su
competencia. Por ello, y en uso de las facultades conferidas por las Leyes Nros. 14.878 y 24.566 y el Decreto Nº 1306/08,
EL
PRESIDENTE DEL INSTITUTO NACIONAL DE VITIVINICULTURA
RESUELVE:
1º — Oficialízase el método "DETERMINACION DE NATAMICINA EN
EL VINO POR CROMATOGRAFIA LIQUIDA DE ULTRA ALTA RESOLUCION MASA / MASA"
que, junto a su VALIDACION, obra como ANEXO en la presente Resolución, en su
versión en idioma español.
2º — A
través de Subgerencia de Investigación para la Fiscalización
dependiente de Gerencia de Fiscalización, continúense las gestiones iniciadas
ante la
ORGANIZACION INTERNACIONAL DE LA VIÑA Y EL VINO (OIV) para
la adopción, por parte de dicha Organización, del método que por la presente se
oficializa para vinos, el cual fija el límite de detección de CINCO MICROGRAMOS
POR LITRO (5 µg.L-1), en previsión de
posibles contaminaciones indirectas.
3º —
Regístrese, comuníquese, publíquese, dése a la Dirección Nacional
del Registro Oficial para su publicación y cumplido, archívese. — Guillermo D.
García.
ANEXO
A LA RESOLUCION Nº
C. 19 /10
DETERMINACION
DE NATAMICINA EN VINOS POR CROMATOGRAFIA LIQUIDA DE ULTRA ALTA RESOLUCION
MASA/MASA
1.
AMBITO DE APLICACION:
Este
método se utiliza para la identificación y cuantificación de Natamicina en vinos blancos, rosados y tintos.
2.
PRINCIPIO:
El
método determina la presencia de natamicina en vinos,
mediante cromatografía líquida de Ultra Alta Resolución - MS/MS, basándose en
la identificación de la masa del ión molecular 666,3 y de sus transiciones
(hijos): 485,2 y 503,2.
3.
REACTIVOS Y SUSTANCIAS:
3.1
Productos Químicos:
3.1.1
Natamicina Marca Sigma P9703-25 mg
o equivalente.
3.1.2
Acetonitrilo f.d. HPLC, z.B. gradiente Fisher A 996-4 CAS
75-05-8 o equivalente.
3.1.3
Agua W 7-4 filtrada por 0,5 micrones CAS 7732-18-5 o equivalente.
3.1.4 Acido fórmico 98% - 100%,
z.B. P.A. Merck Art. Nr.: 1.11670 o equivalente.
3.1.5 Metanol f.d. HPLC, z.B. pro
análisis filtrado por 0,2 micrones Fisher A 454-4 CAS 7-56-1 o equivalente.
4. MATERIALES E INSTRUMENTAL:
4.1 Matraz aforado de 100 ml.
4.2 Matraz aforado de 50 ml.
4.3 Pipeta de doble aforo de 25
ml.
4.4 Pipeta de doble aforo de 10
ml.
4.5 Pipeta de doble aforo de 5 ml.
4.6
Pipeta de doble aforo de 1 ml.
4.7
Propipeta.
4.8
Sistema de Filtración al vacío Millipore o
equivalente.
4.9
Filtro de Nylon de poro de 0,22 µm xe diám xro7 mm
de marca µicroclar Y02047WPH o equivalente.
4.10
Membrana de nitrocelulosa blanca reticulada 0,45 µm x
47 mm
Gamafil N04-047 o equivalente.
4.11 Probeta de 1000 ml graduada.
4.12 Frasco Genna de 1000 ml o
equivalente.
4.13 Jeringa de volumen variable.
4.14 Filtro de jeringa para
soluciones hidroalcohólicas de 0,45 µm Pall preferred (PVDF) 13 mm
PG-4457 o equivalente.
4.15 Balanza de precisión + 0,01
mg.
4.16 Vial UPLC de 1,8 ml 12x32 Gls
Srw Cap VI w/Bnd pre-slt septa o equivalente.
4.17 Ultrasonido COLE - PALMER.
4.18 Columna: Acquity UPLC® BECH
C18 1.7 µm 2.1 x 50 mm.
4.19
Precolumna.
4.20
Cromatógrafo UPLC-MS/MS equipado con ionización electro spray marca Waters.
5.
PREPARACION DE SOLUCIONES:
5.1
Solución primaria de natamicina (100 mg.L.-1)
Pesar
10 mg (4.15) de sustancia estándar (3.1.1),
transferir a matraz de 100 ml y enrasar con metanol.
5.2
Solución secundaria de natamicina (5 mg.L-1)
Tomar
5 ml de la solución primaria (5.1), transferir a
matraz de 100 ml y enrasar con metanol.
5.3
Soluciones estándar de calibración en vino (5 µg.L-1
10 µg.L-1; 25 µg.L-1
y 50 µg.L-1). Utilizar vinos libre de natamicina.
Tabla
Nº 1: Descripción de Diluciones
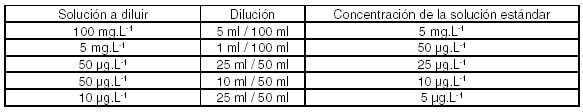
Filtrar
las soluciones estándar de calibración en vino antes de la inyección a través
de un filtro de jeringa (4.14).
5.4
Fase móvil:
5.4.1
Eluyente A: Agua, 0,1% de Acido Fórmico.
Medir
aproximadamente 1000 ml de agua (3.1.3) en probeta
graduada (4.11). Agregar 1 ml de ácido fórmico
(3.1.4) y enrasar con agua (3.1.3). Homogeneizar y filtrar con membrana de
nitrocelulosa (4.10) y sistema de filtración (4.8). Envasar en frasco Genna (4.12).
5.4.2
Eluyente B: Acetonitrilo +
0,1% de Acido Fórmico.
Medir
aproximadamente 1000 ml de acetonitrilo
(3.1.2) en probeta graduada (4.11). Agregar 1 ml de
ácido fórmico (3.1.4) y enrasar con acetonitrilo
(3.1.2). Homogeneizar y filtrar con filtro de nylon (4.9) y sistema de
filtración (4.8). Envasar en frasco Genna (4.12).
6.
PREPARACION DE LA MUESTRA:
Filtrar
el vino a través de filtro de jeringa (4.14), recibir en un vial (4.16) y
colocar en el inyector automático.
7.
PROCEDIMIENTO:
Establecer
los parámetros de trabajo:
Caudal:
0,3 ml/min.
Temperatura
de la columna: 30 °C.
Temperatura
de la muestra: 15 °C.
Volumen
de inyección: 10 µl.
Loop de inyección: 10 µl.
Tiempo
de retención: 4.3 minutos.
Tabla
Nº 2: Gradiente de Elución
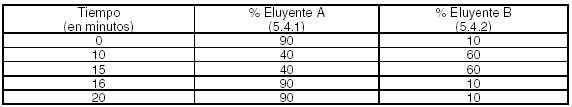
Tabla
Nº 3: Parámetros de Detección
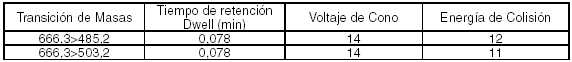
8.
EXPRESION DE LOS RESULTADOS:
Los
resultados se expresan en µg.L-1 con una
cifra significativa.
El
ión de confirmación es la transición (ión hijo) 485,2.
El
ión de cuantificación es la transición (ión hijo) 503,2.
9.
PARAMETROS DE VALIDACION INTERNA:
Tabla
Nº 4: Parámetros de validación
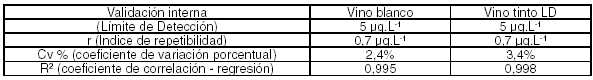
Tabla
Nº 5: Rango dinámico de natamicina en vino blanco
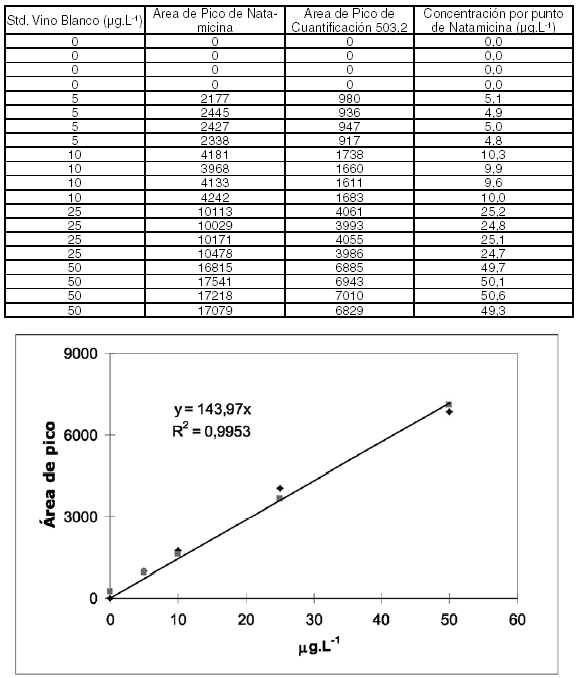
Gráfico
Nº 1: Rango Dinámico de Natamicina en Vino Blanco
hasta 50 µg.L-1.
Tabla
Nº 6: Rango dinámico de natamicina en vino tinto
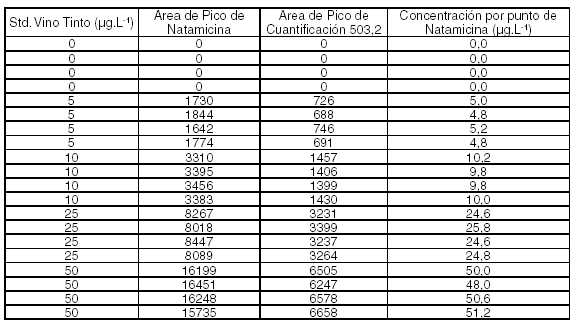
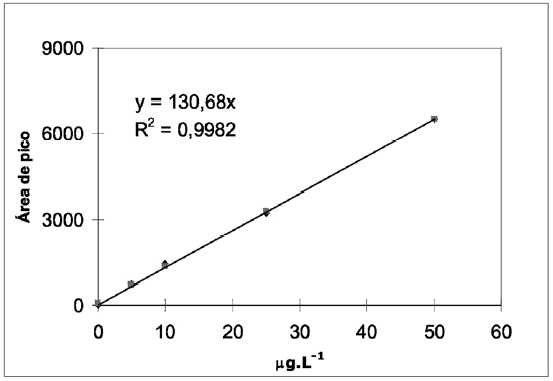
Gráfico
Nº 2: Rango Dinámico de Natamicina en Vino Tinto
hasta 50 µg.L-1.
10.
Cromatograma de vino con 25 µg.L-1
de Natamicina.
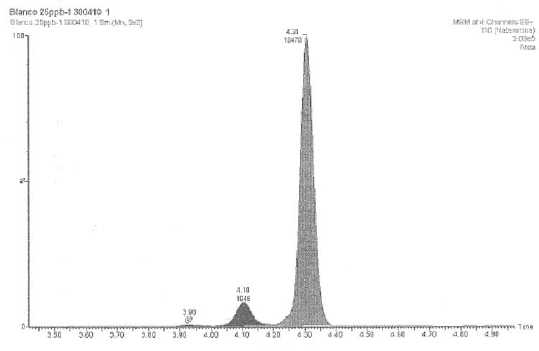
Figura
Nº 1: Ión molecular de natamicina.
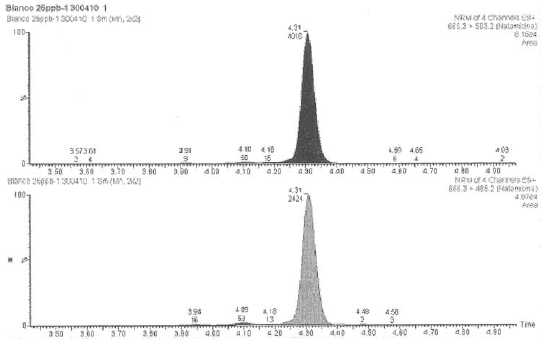
Figura
Nº 2: Iones de transición (hijos) de natamicina.
Nota
1: Tanto el equipamiento como las condiciones operativas se describen a modo de
ejemplo.
Nota
2: En caso que la muestra contenga más de 50 µg.L-1
se diluirá hasta que el valor ingrese dentro de la curva de calibración.
11. BIBLIOGRAFIA:
a) Perez, S; Barcelo,
D "Application of advanced MS techniques to analysis and identification of
human and microbial metabolites of pharmaceuticals in the aquatic
environment". Review TRACTRENDS IN ANALYTICAL CHEMISTRY.
Pages 494 -514. 2007.
b)
Jian Wang "Analysis of macrolide
antibiotics, using liquid chromatographymass
spectrometry, in food, biological and environmental matrices" Mass
Spectrometry ReviewsVolume 28 Issue 1: 50 - 92. Published Online: 2008.
c) S. Abuin,
R. Codony, R. Compañó
"Analysis of macrolide antibiotics in river
water by solidphase extraction and liquid
chromatography-mass spectrometry" Journal of Chromatography A. Volume
1114, Issue 1: 73-81. 2006.
d) Compendium of Internacional Methods of Wine and Must Análisis;
Edición 2003. Anexo B; Resolución OENO 6/99.
e)
Kennet Felrich, Detección
instrumental de antibióticos en alimentos; Edición 1990: AOAC.