Resolución 617-2002
Requisitos, condiciones y procedimientos para la habilitación
técnica de laboratorios que posean bioterios de
producción, mantenimiento y local de experimentación. Informe de ensayo de
residuos de productos fitosanitarios en matrices vegetales. Informe de campo.
Informe analítico.
Bs. As., 18/7/2002
VISTO el expediente Nº 13.890/2001 del
SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA, el Decreto Nº 1585 del
19 de diciembre de 1996, modificado por su similar Nº 394 del 1º de abril de
2001, el artículo 2º de la
Resolución Nº 230 del 24 de marzo de 2000 del citado Servicio
Nacional, y
CONSIDERANDO:
Que la Dirección de
Agroquímicos, Productos Farmacológicos y Veterinarios ha convocado a un Foro
Técnico Interdisciplinario de Expertos para el intercambio de conceptos sobre
las condiciones que deben reunir en nuestro país, los laboratorios que realizan
ensayos biológicos y químicos, con fines de producción de datos toxicológicos, ecotoxicológicos y de residuos de plaguicidas en matrices
vegetales y ambientales, para el registro, revalidación, revaluación
o monitoreo de productos fitosanitarios.
Que la reunión conjunta del mencionado
Foro de Expertos y de los laboratorios productores de datos ha concluido
satisfactoriamente, habiéndose identificado la necesidad de armonizar criterios
y procedimientos de trabajo en los ensayos toxicológicos, ecotoxicológicos
y de residuos de plaguicidas en las matrices vegetales y ambientales a
realizarse, como así también, la necesidad específica de regular la producción,
mantenimiento y uso de animales de laboratorio con los fines ante citados.
Que debe asegurarse el tratamiento humanitario
y responsable de los animales a ser empleados en ensayos para la producción de
información toxicológica y ecotoxicológica, utilizada
en la evaluación de seguridad de los productos fitosanitarios y veterinarios
antes, durante y después de cualquier procedimiento de importación, producción
o utilización de los mismos.
Que uno de los requisitos previos para
el empleo responsable de los animales es el conocimiento exhaustivo de las
características biológicas de la especie a ser utilizada en los estudios, así
como las condiciones necesarias para su alojamiento, alimentación y cuidado.
Que el bienestar y estado de salud de
los animales deben ser observados por personas competentes, entendiendo que la
preparación y formación adecuada proporcionan las premisas necesarias para
adoptar la actitud correcta y para evaluar los aspectos éticos del manejo de
los animales involucrados.
Que la estandarización del alojamiento
y cuidado de los animales experimentales es esencial para la fiabilidad y reproductibilidad de los resultados experimentales de los
estudios toxicológicos y ecotoxicológicos.
Que la Resolución Nº 350 del
30 de agosto de 1999 de la ex-SECRETARIA DE AGRICULTURA, GANADERIA, PESCA Y
ALIMENTACION, establece los requisitos de registro, revalidación y revaluación para los productos fitosanitarios, exigiendo el
desarrollo de estudios toxicológicos y ecotoxicológicos
a fin de cuantificar el riesgo del uso de estas sustancias para el hombre y las
especies no blanco.
Que la Resolución Nº 230 del
24 de marzo de 2000 del SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA
establece la necesidad de desarrollar requisitos y procedimientos para el
registro de laboratorios de toxicología y ecotoxicología idóneos, siendo la
provisión de animales de experimentación de importancia central para el buen
desarrollo de este tipo de estudios.
Que la Ley Nº 3959 de Policía Sanitaria Animal establece
el marco normativo para la fiscalización de la sanidad de los animales que se
importen al país.
Que la fiscalización a través de
inspecciones técnicas de los laboratorios y sus bioterios
de producción y mantenimiento de animales para experimentación, constituye un
mecanismo idóneo que contribuye a garantizar los resultados de los estudios con
ellos efectuados.
Que la predictibilidad
y transparencia que debe signar el accionar de la autoridad fiscalizadora torna
necesario establecer los requisitos técnicos y de procedimiento a que se verán
sujetos la instalación y el funcionamiento de los bioterios.
Que la Dirección de Laboratorio
y Control Técnico, la
Dirección de Agroquímicos, Productos Farmacológicos y
Veterinarios y la Dirección
de Asuntos Jurídicos han tomado la intervención que les compete.
Que el suscripto es competente para
dictar el presente acto, en virtud de lo dispuesto por el artículo 8º, inciso
m) del Decreto Nº 1585 del 19 de diciembre de 1996, sustituido por su similar
el Decreto Nº 394 del 1º de abril de 2001.
Por ello,
EL PRESIDENTE DEL SERVICIO NACIONAL DE
SANIDAD Y CALIDAD AGROALIMENTARIA
RESUELVE:
Artículo 1º — Los laboratorios que realicen estudios biológicos para la
producción de datos toxicológicos y ecotoxicológicos
y los laboratorios que realicen determinaciones analíticas de residuos de
principios activos químicos y biológicos en matrices vegetales y ambientales
con fines de registro, revalidación, revaluación o
monitoreo de productos fitosanitarios deberán registrarse en el SERVICIO
NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA, de acuerdo a lo establecido por
las Resoluciones Nros. 279 del
20 de diciembre de 1993 del ex-INSTITUTO ARGENTINO DE SANIDAD Y CALIDAD
VEGETAL, 209 del 8 de marzo de 1994 de la ex-SECRETARIA DE AGRICULTURA,
GANADERIA Y PESCA, 301 del 8 de julio de 1994 del ex-INSTITUTO ARGENTINO DE
SANIDAD Y CALIDAD VEGETAL, 230 del 24 de marzo de 2000 del SERVICIO NACIONAL DE
SANIDAD Y CALIDAD AGROALIMENTARIA y la presente Resolución.
Art. 2º — Los protocolos de los estudios biológicos y de residuos a
realizarse, son los establecidos en el capítulo 20, apartado "Listado de
Organismos y Cuerpos Normativos que Protocolizan Ensayos y Procedimientos de
Laboratorio para la
Obtención de Datos con Fines de Registro" de la Resolución Nº 350 de
fecha 30 de agosto de 1999 de la ex-SECRETARIA DE AGRICULTURA, GANADERIA, PESCA
Y ALIMENTACION.
Art. 3º — Los laboratorios que realicen los estudios aludidos en el
artículo precedente deberán cumplir, para el desarrollo de los mismos, las
recomendaciones de Buenas Prácticas de Laboratorio desarrolladas por la Organización para la Cooperación Económica
y el Desarrollo (OCDE) que a continuación se mencionan.
—Principios generales de Buenas
Prácticas de Laboratorio (BPL): Nº 45, 1993.
—Aseguramiento de la calidad y Buenas
Prácticas de Laboratorio: Nº 48, 1993.
—Cumplimiento de proveedores de
laboratorio con los principios de las BPL: Nº 49, 1993.
—La aplicación de las BPL para los
estudios de corta duración: Nº 73, 1993.
—La aplicación de las BPL para los
estudios de campo: Nº 50, 1993.
—El papel y responsabilidad del
director del estudio en BPL: Nº 74, 1993.
Las enmiendas posteriores de las
directrices OCDE precitadas y las nuevas directrices OCDE que pudieran
generarse vinculadas a las preexistentes serán de aplicación automática.
Art. 4º — Los informes finales de los estudios indicados en el artículo 2º
de la presente resolución, deberán cumplimentar la totalidad de los apartados
indicados en los protocolos desarrollados, siguiendo las directrices
establecidas por la OCDE
para este fin.
Art. 5º — Los animales de laboratorio utilizados en los estudios de toxicología
y ecotoxicología mencionados en el artículo 2º deberán producirse, mantenerse y
utilizarse de acuerdo a las condiciones establecidas en el Anexo I, que forma
parte de la presente resolución.
Las condiciones indicadas en el
mencionado Anexo, son de aplicación para todas las especies que se importen,
críen y utilicen en nuestro país en las pruebas biológicas indicadas en el
artículo 1º de la presente.
Art. 6º — La importación de animales para ensayos biológicos queda sujeta
a lo establecido por la Ley Nº
3959 de Policía Sanitaria Animal y a las condiciones establecidas en la
presente resolución.
Art. 7º — Para su habilitación los laboratorios aspirantes deberán cumplir
con lo siguiente:
—La normativa que se menciona en el
artículo 1º.
—Contar con un Director Técnico
Titular, profesional vinculado a las áreas temáticas del laboratorio,
debidamente matriculado.
—Contar con las habilitaciones
edilicias y ambientales en los órdenes municipal, provincial y nacional según
correspondan.
—Los laboratorios aspirantes serán
inspeccionados previamente a la emisión del registro por DOS (2) profesionales
del SERVICIO NACIONAL DE SANIDAD Y CALIDAD AGROALIMENTARIA, pudiendo ser
acompañados por un tercer profesional experto externo.
—Se someterá a los laboratorios aspirantes
a una prueba interlaboratorios.
—Los gastos que demande la inspección y
el envío de muestras estarán a cargo de laboratorio solicitante del registro.
—Cumplidos los requisitos precitados en
forma satisfactoria se procederá al registro del laboratorio solicitante.
—Los laboratorios habilitados serán
periódicamente inspeccionados por profesionales del SERVICIO NACIONAL DE
SANIDAD Y CALIDAD AGROALIMENTARIA en los términos establecidos por la Resolución Nº 279 de
fecha 20 de marzo de 1993 del ex-INSTITUTO ARGENTINO DE SANIDAD Y CALIDAD
VEGETAL.
Art. 8º — Los laboratorios en los que se efectúen las determinaciones
analíticas de residuos de principios activos químicos y biológicos
experimentales o para ampliación de uso de los ya registrados, deberán participar
previamente en las pruebas interlaboratorios
organizadas por la
Coordinación General de Laboratorio Vegetal dependiente de la Dirección de
Laboratorios y Control Técnico de este Organismo.
Art. 9º — Los ensayos de residuos de principios activos químicos y
biológicos mencionados en el artículo 7º, deberán encuadrarse en la Directiva OCDE
sobre aplicación de las BPL para los estudios de campo, debiendo incluirse en
el informe final el protocolo que se adjunta en el Anexo II, que forma parte de
la presente resolución.
Art. 10. — Los laboratorios que realicen estudios de toxicidad inhalatoria aguda en ratas, deberán realizar los estudios
de validación de los métodos empleados, en función de los equipos de que
disponen.
Art. 11. — Los datos producidos por laboratorios del exterior deberán
cumplimentar las consideraciones indicadas en la Resolución Nº 230 de
fecha 24 de marzo de 2000 del SERVICIO NACIONAL DE SANIDAD Y CALIDAD
AGROALIMENTARIA.
Art. 12. — Los infractores a las normas previstas en la presente resolución
serán pasibles de las sanciones establecidas por el artículo 18º del Decreto Nº
1585 del 19 de diciembre de 1996.
Art. 13. — Comuníquese, publíquese, dése a la Dirección Nacional
del Registro Oficial y archívese. — Bernardo G. Cané.
ANEXO I
REQUISITOS, CONDICIONES Y
PROCEDIMIENTOS PARA LA
HABILITACION TECNICA
DE LABORATORIOS QUE POSEAN BIOTERIOS DE
PRODUCCION,
MANTENIMIENTO Y LOCAL DE
EXPERIMENTACION
1 — UBICACION Y CARACTERISTICAS
EDILICIAS GENERALES
1.1 — Los locales de producción,
mantenimiento y/o experimentación animal no podrán estar en relación directa
con áreas administrativas, de elaboración o analíticas.
1.2 — Los sistemas de aire
acondicionado y/o ventilación no podrán ser compartidos con otras áreas. Serán
exclusivos para el sector bioterio.
1.3 — En la construcción de los locales
del área bioterio, deberán tenerse en cuenta todos
aquellos factores físicos que puedan afectar la salud y calidad de los
animales.
Los locales deben construirse a prueba
de roedores salvajes e insectos.
Las superficies interiores (paredes,
suelos y techo) deben ser lisas y sin grietas, no han de desprender partículas
y deben ser fáciles de limpiar y desinfectar.
Las rejillas de desagüe dentro de los
locales deben poseer tapas de seguridad a fin de evitar la entrada de roedores
e insectos.
1.4 — Los recintos deben ser lo
suficientemente espaciosos como para permitir el trabajo cómodo de los
operarios en sus tareas y evitar la sobrecarga animal.
1.5 — La ubicación y plano de detalle
de las instalaciones deben presentarse con la documentación general solicitada
al laboratorio registrante.
A — LABORATORIOS QUE POSEEN BIOTERIO DE
PRODUCCION, MANTENIMIENTO Y LOCAL DE EXPERIMENTACION
A.1 — AREA DE PRODUCCION Y
MANTENIMIENTO:
A.1.1 — Local de cría o producción
Será destinado únicamente a los
animales en apareo o reproducción y a sus crías. Los reproductores deberán
estar perfectamente identificados (tatuaje/anillo/otro según especie),
llevándose registros donde se especifiquen como mínimo el sistema de apareo
utilizado; fecha de parto/nacimiento/período de incubación; fechas de destete;
cantidad de crías destetadas/separadas; destino de las mismas.
A.1.2 — Local de mantenimiento o stock
Será destinado exclusivamente a los
animales en mantenimiento, a la espera de su utilización posterior. Los
animales deberán estar perfectamente identificados, llevándose registro como
mínimo de muertes espontáneas o por eutanasia, resultado de las necropsias y
causa probable de muerte, destino de los animales.
Por razones insalvables de espacio o
cuando la magnitud de producción de animales no justificara locales
independientes, la cría y el mantenimiento de una especie podrá realizarse en
el mismo local, con sectorización adecuada.
A.1.3 — Local de experimentación animal
Será destinado a alojar a los animales
de experimentación durante el transcurso de una experiencia.
Una vez finalizada la
misma dichos animales deberán ser descartados no pudiendo regresar a
salas de mantenimiento para ser reutilizados, salvo que las características del
estudio así lo permitan.
Deberá llevarse un registro donde
conste como mínimo la fecha de iniciación y finalización del ensayo, los
animales destinados al mismo debidamente identificados y el destino final de
dichos animales.
Tanto en los locales de cría como en
los de mantenimiento no podrán albergarse especies diferentes con fines
reproductivos, salvo que compartan características biológicas similares que no
alteren su respuesta biológica, no obstante deberá existir sectorización por
especie.
A.1.4 — Local de cuarentenas
Será destinado al mantenimiento de los
animales introducidos durante un tiempo prudencial hasta descartar posibles
patologías. Deberá llevarse un registro de la fecha de ingreso de los animales,
las enfermedades, tratamientos y controles realizados y su fecha de liberación.
A.2 — AREA DE DEPOSITO
A.2.1 — Depósito material limpio.
Se almacenarán jaulas, bebederos,
peceras y otros implementos destinados al uso de los animales.
A.2.2 — Depósito de alimentos
Se almacenarán adecuadamente estibados,
los alimentos recibidos del proveedor. El depósito deberá poseer un sistema de
renovación y acondicionamiento del aire que asegure la temperatura y humedad adecuados para su conservación.
A.2.3 — Depósito de material estéril
Se almacenará el material autoclavado destinado al animal
A.3 — AREA DE LAVADERO
Deberá ser independiente de los locales
de cría, mantenimiento y experimentación.
B — LABORATORIOS QUE NO PRODUCEN SUS
PROPIOS ANIMALES
Deben poseer las mismas instalaciones
de mantenimiento y experimentación que los anteriores, excepto el sector de
cría.
2 — CONDICIONES GENERALES DE LIMPIEZA Y
MANTENIMIENTO DE LOS ANIMALES
La limpieza general de locales,
corredores, depósitos y otras áreas relacionadas al bioterio
será diaria, debiendo usarse productos detergentes y desinfectantes registrados
en SENASA.
No deben emplearse productos
desodorantes de ambientes u otros agentes químicos para cubrir olores
producidos por los animales.
El cambio de jaulas, peceras, la
renovación de lechos/aguas y el retiro de excretas deberán tener una
periodicidad tal que impida la acumulación de amoníaco y otras sustancias o
elementos perjudiciales, permitiendo que los animales se mantengan limpios y en
buenas condiciones sanitarias.
Los lechos para animales terrestres
deben ser de materiales absorbentes, libres de sustancias químicas tóxicas que
puedan dañar a los animales y/o interferir en las respuestas biológicas. Deben
evitarse los lechos que puedan ser fácilmente ingeridos. De usar viruta de
madera, la misma será de maderas blancas no resinosas.
Los lechos deben esterilizarse dado que
pueden estar contaminados con gérmenes patógenos.
Los lechos sucios deben ser vaciados de
las jaulas/peceras fuera de los locales con animales, de forma tal de evitar la
contaminación del ambiente.
Las jaulas/peceras deben ser lavadas y
desinfectadas antes de colocarse el material de lecho limpio.
El suministro de agua para animales
terrestres será diario y no debe restringirse la alimentación a menos que el
ensayo así lo requiera.
Deben conocerse las condiciones
específicas de alimentación para cada especie, debiendo llevarse registro de
las mismas.
3 — ALIMENTACION
El alimento que se suministre a los
animales debe reunir las exigencias específicas para la correcta crianza y
mantenimiento de la especie en cuestión, debiendo estar registrado en el SENASA
como alimento para animales de laboratorio.
Si se tratara de una fórmula magistral
deberá reunir los requisitos establecidos por el SENASA para dicho tópico.
El almacenamiento del alimento debe
ordenarse de tal forma que se consuma en primer término aquel que más tiempo
lleve en depósito. Debe llevarse registro de fecha de ingreso y ubicación de la
partida.
El alimento no podrá tener más de TRES
(3) meses.
4 — DISPOSICION DE EXCRETAS Y OTROS
CONTAMINANTES
La disposición de las excretas
animales, de los animales muertos, de los remanentes de sustancias empleadas en
la experimentación, de lechos u otros contaminantes que pudieran generarse se
ajustarán a las reglamentaciones nacionales, provinciales y municipales
vigentes para la disposición de residuos patológicos y peligrosos que
correspondan.
5 — CALIDAD GENETICA
Debe acreditarse la calidad y
definición genética de las cepas animales que se utilicen. Tal acreditación
deberá ser avalada por institución o profesional reconocidos por el SENASA.
De poseer cría propia, es necesario un
control genético periódico que asegure la pureza.
De adquirirse los animales, debe
exigírsele al vendedor dicha acreditación.
Para los ensayos de rutina toxicológica
o ecotoxicológica no pueden usarse animales
capturados en la naturaleza o vagabundos. Cuando una circunstancia particular
así lo exigiera debe solicitarse autorización a la Dirección de Fauna y
Flora Silvestre de la
Secretaría de Ambiente y Desarrollo Sustentable, debiendo
ajustarse en un todo a las normas de su competencia y a las establecidas por el
SENASA.
6 — CALIDAD SANITARIA
Debe acreditarse la calidad sanitaria
de los animales, producidos o adquiridos, mediante estudios adecuados que
certifiquen la ausencia de enfermedades bacterianas, virales o parasitarias,
clínicas o subclínicas, que pudieran interferir con los resultados
experimentales. Tal acreditación deberá ser avalada por institución o
profesional responsable de acuerdo a la modalidad establecida por el SENASA
quien establecerá el listado de enfermedades por especie que deberán
controlarse y el procedimiento el control sanitario.
7 — PERSONAL AFECTADO AL BIOTERIO
Deberá contar con el asesoramiento de
un profesional médico veterinario, de acuerdo a las incumbencias establecidas
por el Ministerio de Educación, debidamente matriculado. Asimismo deberá contar
con personal que demuestre capacitación fehaciente en el manejo específico de
los animales de laboratorio.
8 — CONDICIONES GENERALES DEL MEDIO
AMBIENTE PARA CRIA Y MANTENIMIENTO DE ROEDORES Y PECES
8.1 — AIRE
8.1.1 — La inyección de aire en los
locales debe hacerse a la altura de los ángulos superiores de los mismos y la
extracción en los inferiores.
8.1.2 — Los locales en su interior
deben poseer presión positiva de aire respecto de los pasillos y/o áreas
exteriores, por medio de la regulación apropiada del caudal inyectado y
extraído.
De poseer el bioerio
doble pasillo con locales centrales (circulación limpia y sucia) el gradiente
de presión será desde el corredor limpio al suelo.
8.1.3 — Debe contar con medidores de
presión de aire dentro de los locales, que permitan el control de la presión
positiva.
8.1.4 — El aire de las instalaciones
animales no debe ser recirculado a menos que se hayan eliminado las partículas
nocivas o contaminantes y los gases tóxicos.
8.1.5 — Si se utilizan los sistemas recirculantes, los mismos deben tener un mantenimiento
cuidadoso en lo referente a limpieza y/o cambio de filtros, debiendo llevarse
un registro de las fechas de recambio o limpieza de los mismos.
8.2 — TEMPERATURA Y HUMEDAD
8.2.1 — Debe contar con sistemas de
control de temperaturas y humedad relativa, mediante el uso de termómetros de
máxima y de mínima e higrómetros en cada habitación. Debe llevarse un registro
diario continuo de sus variaciones.
8.3 — FOTOPERIODO
8.3.1 — La luz debe ser artificial,
provista por tubos fluorescentes, tipo luz día, con incidencia oblicua de la
misma a los fines de que todas las jaulas/peceras independientemente de su
ubicación, reciban intensidades similares. Debe realizarse control de fotoperíodo.
8.3.2 — No deben existir fuentes de luz
externas ni ruidos.
8.4 — AGUA
8.4.1 — Para la producción de peces,
además debe contarse con equipo de control de temperatura del agua, con sistema
de alarma automático variación de DOS (2° C) grados centígrados.
8.4.2 — Debe realizarse un control de
calidad del agua de dilución dos veces al año, como mínimo.
9 — CONDICIONES GENERALES DEL MEDIO
AMBIENTE PARA CRIA Y MANTENIMIENTO DE AVES Y CONEJOS
9.1 — TEMPERATURA Y HUMEDAD
9.1.1 — Debe contar con sistemas de
control de temperaturas y humedad relativa, mediante el uso de termómetros de
máxima y de mínima e higrómetros en cada sector del criadero.
Debe llevarse un registro diario
continuo de sus variaciones.
9.1.2 — Durante la cría y mantenimiento
de conejos no deben producirse corrientes de aire ni temperaturas mayores de
TREINTA GRADOS CENTIGRADOS (30° C). Si deben transportarse, las cajas deben
poseer espacio suficiente y buenas aberturas para la ventilación.
9.1.3 — Durante la cría y mantenimiento
de pollos la ventilación necesaria depende del número de animales, de su tamaño
y de la temperatura ambiental. La temperatura óptima para los polluelos que
tienen entre UNO (1) y TRES (3) días es de TREINTA Y CINCO GRADOS CENTIGRADOS
(35° C), la cual se alcanza con lámparas de calor. Después debe disminuirse de
forma gradual: durante los siguientes CUATRO (4) días debe disminuirse a razón
de CERO COMA CINCO GRADOS CENTIGRADOS (0,5° C) por día y posteriormente a razón
de UN GRADO CENTIGRADO (1° C) por día hasta alcanzar los DIECIOCHO-VEINTIUN
GRADOS CENTIGRADOS (18-21° C).
10 — CONDICIONES AMBIENTALES PARA CADA
ESPECIE
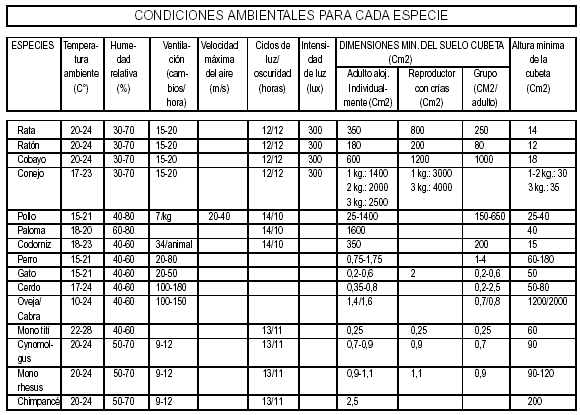
11 — CONDICIONES BASICAS QUE DEBERAN
REUNIR LAS COLONIAS DE ABEJAS DESTINADAS A ENSAYOS BIOLOGICOS
11.1 — COMPOSICION DE LA COLONIA
Se utilizarán abejas Apis melífera. La colonia de abejas que se vaya a utilizar
para cualquier ensayo biológico, debe estar conformada por todos los
integrantes de una colonia: abejas obreras adultas y nodrizas; UNA (1) reina y
dependiendo de la época del año se exigirá o no la presencia de zánganos.
También dependerá de la época del año y del uso que se le vaya a dar, la
presencia de cría en todos sus estadíos.
En caso de que se utilice un grupo de
abejas, debe ser extraído de colonias con las mismas características. Las
abejas destinadas a estudio de toxicidad deberán ser hermanas de madre y tener
entre DIEZ (10) y VEINTE (20) días de edad. Esta situación debe certificarse
para cada estudio.
11.2 — CONDICIONES AMBIENTALES Y ALIMENTACION
Se permitirá la libación libre de las
abejas pero asegurando la no aplicación de productos agroquímicos en la zona
circundante.
Las colmenas deberán ubicarse en una
zona en la que en el área de libación de las abejas no haya residuos de ningún
tipo, ya sean basurales o instalaciones de alguna industria. La zona no podrá
ser urbana, salvo que se mantengan las colmenas bajo condiciones controladas
mediante carpas o ambiente cerrado de cualquier tipo.
La colonia podrá alimentarse de manea
artificial con miel de origen conocido o con glucosa de maíz o jarabe de alta
fructuosa, en última instancia, con jarabe de azúcar. El aporte proteico puede
estar dado por polen natural correctamente conservado o por la administración
de suplementos polínicos cuyo uso y comercialización esté autorizado
por SENASA. La colonia no deberá sufrir carencias alimenticias en ningún
momento.
11.3 — SANIDAD DE LA COLONIA
Las abejas utilizadas deberán provenir
de colonias sanas, sin signología clínica de las
enfermedades bacterianas Loque Americana y Loque Europea. Con respecto a nosemosis
se deberá someter una muestra de entre TREINTA Y CINCO (35) y SESENTA (60)
abejas adultas a análisis, tomadas preferentemente de la piquera y enviándola a
un laboratorio de diagnóstico de enfermedades apícolas
para someterla a un test cuantitativo de nosemosis. Más allá de la época en que se realice el
diagnóstico, el nivel de infectación deberá ser igual
o menor de UNO (1) (método cuantitativo de Rossi-Cornejo).
En caso de que se deba utilizar toda la colonia, inclusive la cría, no deberá
haber nomias producto de la contaminación con Ascophaera apis, ni signología clínica de cualquier enfermedad viral.
Respecto de Varroasis,
se requerirá que la colonia haya sito tratada con algún producto autorizado por
SENASA, pero deberán transcurrir TREINTA (30) días desde la finalización del
período de acción del producto autorizado. En caso de que la colonia no haya
sido tratada, no debe presentar signología clínica de
esta enfermedad ectoparasitaria, ni visualizarse
individuos de Varroa jacobsoni.
Aquellas colmenas que se enfermen deberán recibir el tratamiento
correspondiente y quedarán automáticamente rechazadas como proveedoras de
abejas destinadas a ensayos. Deben llevarse registros de las enfermedades
detectadas, cantidad de colmenas afectadas y tratamientos efectuados.
11.4 — LABORATORIOS QUE CRIEN O RECRIEN
COLMENAS PARA EL AUTOABASTECIMIENTO DE ABEJAS. CONDICIONES PARA
ESTABLECIMIENTOS PROVEEDORES
Además de las condiciones ambientales,
propias de la colonia y de las sanitarias, deberán cumplir los siguientes
requisitos:
11.4.1 — CONDICIONES EDILICIAS
GENERALES
Sala de depósito de material inerte:
Se conservarán los materiales de
madera, alambres, utensilios para el armado del material, la cera y cualquier
otro tipo de material inerte.
Sala de depósito de productos
contaminantes:
Se conservarán debidamente
identificados los productos de la limpieza y los utilizados para tratamientos
sanitarios en las colonias.
11.4.2 — AREA DE PRODUCCION Y MANTENIMIENTO
Esta área estará dividida en una de
cría, producción y mantenimiento que deberá cumplir las condiciones de medio
ambiente establecidas anteriormente y un local de experimentación que deberá
reunir las características generales establecidas para las demás especies y las
propias de cada ensayo de acuerdo a la norma internacional que se tome como
referencia.
Los laboratorios que incorporen
material apícola vivo para destinarlo directamente a ensayos biologicos, deberán seguir los lineamientos establecidos en
las normas internacionales de acuerdo al ensayo a realizar. Deberán además,
exigir una CERTIFICACION al proveedor en la que constará:
• Número de habilitación de
establecimiento proveedor extendido por SENASA
• Que las abejas provienen de colonias
de abejas Apis melífera.
• Que las abejas comparten la misma
ascendencia materna.
• Que las colonias donantes de
individuos o la colonia misma en caso de que se solicite completa está sana,
sin signología clínica de enfermedades bacterianas,
con niveles iguales o inferiores a UNO (1) como resultado del diagnóstico
cuantitativo de nosema, que fueron tratadas contra Varroa con algún producto autorizado por SENASA, que no
presentan signología clínica de cualquier enfermedad
viral.
• Que las abejas tienen entre DIEZ (10)
y VEINTE (20) días de edad.
12 — CONDICIONES AMBIENTALES PARA OTRAS
ESPECIES NO CONTEMPLADAS EN ESTA NORMA
Condiciones ambientales, de
alimentación y de sanidad para otras especies podrán ser establecidas por el
SENASA a solicitud del laboratorio registrante, para
los fines experimentales establecidos por la Resolución ex SAGPyA Nº 350/99.
ANEXO II
INFORME DE ENSAYO DE RESIDUOS DE
PRODUCTOS FITOSANITARIOS
EN MATRICES VEGETALES
INFORME DE CAMPO: PARTE A
RESPONSABILIDAD
1 — Año
2 — Identificación o número de ensayo.
3 — Compañía u organización. Nombre y
dirección.
4 — Persona/s responsable/s (director
del estudio, coordinadores según responsabilidades tales como responsables del
plan de ensayo, de la aplicación, del muestreo y envío del material, del
análisis).
IDENTIFICACION E INFORMACION GENERAL
DEL ENSAYO
1 — Principio/s activo/s.
2 — Clase de plaguicida o uso agrícola.
3 — Marca comercial o número de código.
4 — Formulación (tipo, concentración en
unidades internacionales).
5 — Cultivo/producto agrícola (tipo,
variedad/cultivar).
6 — Localidad (país/región, lugar o
referencia cartográfica).
7 — Plagas/enfermedades.
8 — Información general del ensayo.
9 — Datos de la parcela (dimensión,
número de parcelas por tratamiento, número de parcelas control, espaciado del
cultivo, número de plantas por parcela, número de hileras por parcela).
10 — Tratamientos con plaguicidas en el
año anterior.
11 — Otros plaguicidas aplicados a la
parcela (dosis, momento, lugar).
12 — Tratamientos culturales
(riesgo/fertilizantes).
13 — Resumen de las condiciones
meteorológicas (antes, durante y después de la aplicación).
DATOS DE LA APLICACION
1 — Método/equipo de aplicación.
2 — Dosis.
3 — Dilución o concentración del
pulverizado en unidades del sistema internacional.
4 — Número de aplicaciones.
5 — Fecha de las aplicaciones.
6 — Fase del desarrollo al hacer el
último tratamiento (escalas reconocidas internacionalmente).
MUESTREO
1 — Parte de la cosecha de que se han
tomado muestras.
2 — Fase del desarrollo al hacer el
muestreo.
3 — Método de muestreo.
4 — Número de muestras por parcela.
5 — Número de unidades en la muestra
primaria.
6 — Peso de la muestra.
7 — Fechas (muestreo, congelación,
recibo en laboratorio).
8 — Intervalos (último
tratamiento/cosecha, muestreo/congelación, muestreo/recibo en el laboratorio).
ENVIO Y CONSERVACION DE LAS MUESTRAS
Hoja de ruta de las muestras, indicando
cadena de frío y conservación (temperatura, características de envases),
responsable/s y fechas.
INFORME ANALITICO, PARTE B
1 — Persona/s responsable/s del
análisis.
IDENTIFICACION DE LA MUESTRA
1 — Cultivo (producto agrícola).
2 — Identificación o número de la
muestra.
3 — Plaguicida empleado.
ESTADO Y TRATAMIENTO DE LA/S MUESTRA/S
1 —Fecha de recibo en el laboratorio.
2 —Fecha de análisis.
3 — Porción de muestra que se va a
analizar.
ANALISIS - REQUERIMIENTOS ANALITICOS
PARA LA DETERMINACION
DE LOS RESIDUOS
Presentación del método analítico
utilizado que incluya extracción, limpieza y la determinación propiamente dicha
Los métodos utilizados deberán ser
validados por el laboratorio que realiza el trabajo.
Los parámetros a incluir en los
protocolos de validación son: Precisión, Exactitud, Linealidad,
Límite de detección (LD) y Límite de
Cuantificación (LC).
El procedimiento a utilizarse será el
siguiente:
Procesar blanco de matriz y muestras
fortificadas a TRES (3) niveles de concentración: 0,5 LMR, LMR y 2 LMR cada una
por triplicado (LMR = Límite Máximo de Residuo, en los casos que no exista se
deberá reemplazar por el valor esperado, lo importante es que los resultados
informados estén dentro del rango validado).
Se determinará:
EXACTITUD: recuperación porcentual para
cada fortificado R%.
PRECISION: desviación Estándar Relativa
para el blanco y para cada fortificado DSR%.
LINEALIDAD: graficando Conc. Hallada vs. Conc. Nominal
se determina el coeficiente de correlación. (De la pendiente de este gráfico se
determina la recuperación porcentual promedio).
Estimación de LD y LC para efectuar
dichas estimaciones se graficará Respuesta en función de Concentración para
cada fortificado, utilizando un análisis de regresión lineal, se calcula la
ordenada al origen y su desviación estándar.
Para estimar el LD se considera un
valor de Respuesta igual a la ordenada al origen más TRES (3) veces su
desviación estándar. Interpolando con la recta se obtiene la concentración
buscada. Para el LC se procede de la misma forma pero sumando DIEZ (10) veces
la desviación estándar.
Una vez estimados LD y LC se procederá
a confirmarlos experimentalmente fortificando un blanco a la concentración de
LD y verificando que de señal diferenciada del fondo y fortificando blancos por
triplicado a la concentración LC y verificando que presentan exactitud y
precisión aceptables.
VALORES RECOMENDADOS
El límite de cuantificación de un
método debe ser menor o igual al 50% del LMR.
Se considera buena exactitud y
precisión a aquellas que dan recuperaciones en el rango de 70 a 110% (con recuperación
media del rango de 80 a
100%) con una Desviación Estándar Relativa de ± 10%.
Se pueden aceptar Desviaciones Estándar
Relativas mayores a medida que disminuyen las concentraciones.
En análisis de trazas es frecuente
encontrar rangos de recuperaciones medias fuera del rango 80 y 100%. No se
deben aplicar métodos que presenten recuperaciones medias <50% y DSR
>30%.
El coeficiente de correlación no debe
ser inferior a 0,975.
RESULTADOS
1 — Dosis.
2 —Intervalo (tratamiento hasta
muestreo).
3 — Residuo y control (incluida la
desviación estándar).
4 —Estabilidad de los residuos en las
condiciones del almacenamiento.